Clear Sky Science · he
מחקר על ביומרקרים של המרה המוחמצת-הומוציסטאין של תאי השריר החלק של כלי הדם לתאי קצף
מדוע הסתימות בעורקים מתחילות מצד שינויים מיקרוסקופיים בתאים
אטרוסקלרוזיס — ההסתמות והקשחת העורקים ההדרגתית — הוא גורם עיקרי למחלות לב ושבץ. אנו לרוב שומעים על כולסטרול ותזונה, אך פחות על הדרך שבה תאים בודדים בדופן הכלי משתנים כאשר המחלה מתפתחת. מחקר זה בוחן מקרוב טריגר אחד כזה, מולקולה בדם הנקראת הומוציסטאין, ומראה כיצד היא יכולה לדחוף תאי שריר כליליים בדרך כלל להתנהג כחולקים שומרים, לאגור שומן ולהפוך למה שמכונה תאי קצף, אבני הבניין של פלאקים מסוכנים.
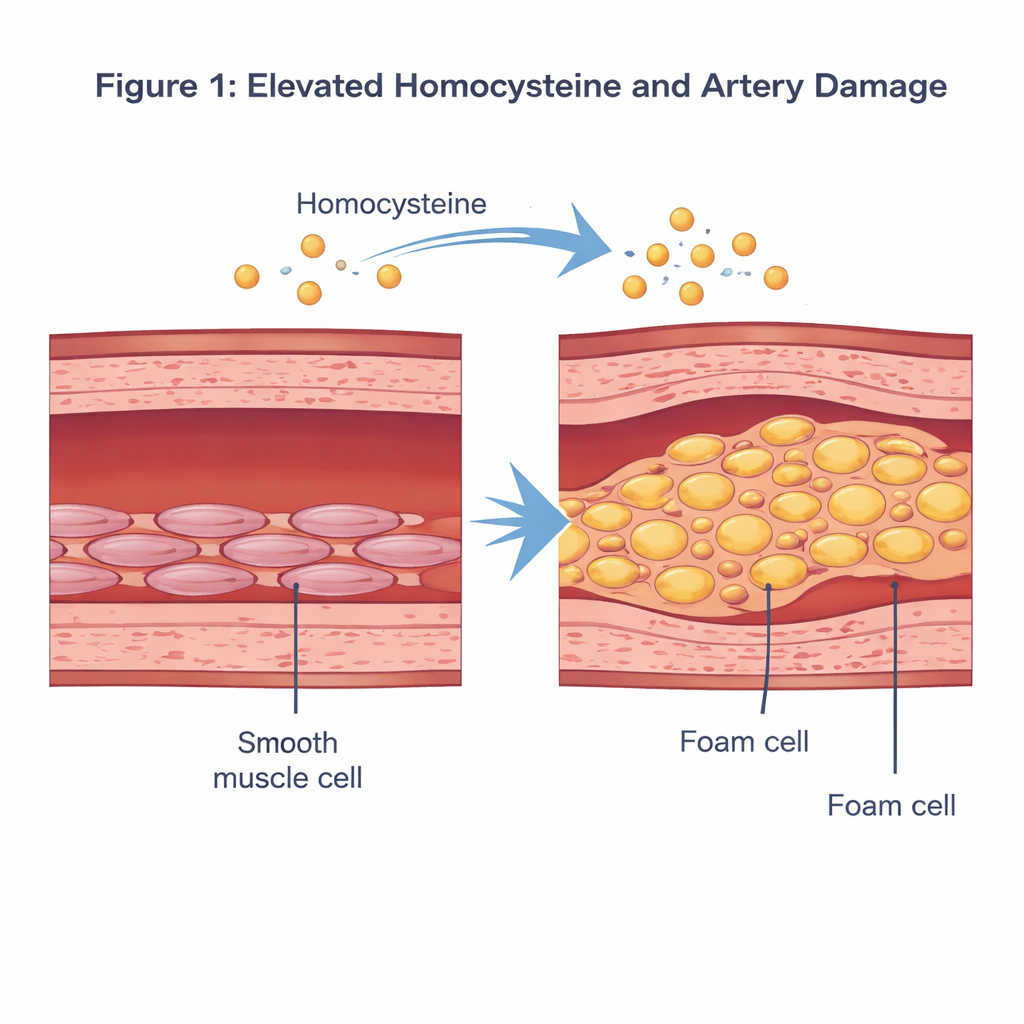
חומצת אמינו מטרידה בזרם הדם
הומוציסטאין היא חומצת אמינו הכוללת גופרית, שנוצרת כשהגוף מעבד את הנוטריאנט התזונתי מתיונין. במצב תקין, הרמה שלה בדם נמוכה. כאשר היא עולה מעל כ-15 מיקרומול לליטר — מצב הקרוי היפר-הומוציסטאין-מיה — מחקרים אפידמיולוגיים קישרו זאת לסיכון גבוה יותר למחלות קרדיו-ווסקולריות. מחקרים קודמים הציעו כי עודף הומוציסטאין עלול לפגוע בציפוי הפנימי של העורקים, לעורר דלקת ולשנות את התנהגותם של תאי השריר החלק של כלי הדם, השוכנים בשכבה האמצעית של דופן הכלי ועוזרים לווסת לחץ דם על ידי כיווץ והרפיה.
כיצד תאי שריר עורקי הופכים לתאי קצף רוויי שומן
החוקרים התמקדו באופן שבו הומוציסטאין מעצב מחדש את תאי השריר החלקים הללו. במעבדה חשפו הם תאי שריר חלק של כלי דם אנושיים למנה של הומוציסטאין שנועדה לדמות מצב דמוי-מחלה והשוו אותם לתאים שלא טופלו. בעזרת צביעות מבוססות ובדיקות ביוכימיות סטנדרטיות ראו שהתאים המטופלים בהומוציסטאין התמלאו בטיפות שומן צבועות באדום, ורמות הכולסטרול והטריגליצרידים עלו באופן חד. באותו זמן, סמני חלבון המזוהים עם זהותם ה"כיווצית" הרגילה ירדו, בעוד שסמני מצב סינתטי יותר, המתקשר להיווצרות פלאקים, עלו. יחד, שינויים אלה מראים שהומוציסטאין יכול לדחוף תאי שריר חלק להתרחק מתפקידם הרגיל ולעבור לפנוטיפ דמוי תאי קצף, רווי שומן, התורם ישירות להיווצרות פלאקים.
ציד טביעות אצבע מולקולריות בתוך התאים
כדי להבין אילו חלבונים משתנים במהלך ההמרה הזו, הצוות פנה לפרוטאומיקה מודרנית, טכנולוגיה שיכולה למדוד אלפי חלבונים בבת אחת. הם השוו רמות חלבונים בתאים שטופלו בהומוציסטאין מול הביקורת וכמתו באופן מהימן כמעט 4,800 חלבונים. מתוך אלה, 54 בלטו כשונה באופן משמעותי: 13 עלו ו-41 ירדו. רבים מהחלבונים המשתנים מעורבים בטיפול בליפידים, שיקומי תאים, מתח חמצוני ושחזור מבני של התאים. המחברים השתמשו בכלי ביו-אינפורמטיים כדי לקבץ חלבונים אלה למסלולים פונקציונליים ולמפות איך הם מתקשרים זה עם זה, תוך הדגשת רשתות המקושרות למטבוליזמוס הכולסטרול ולתגובות לחץ בדופן הכלי.
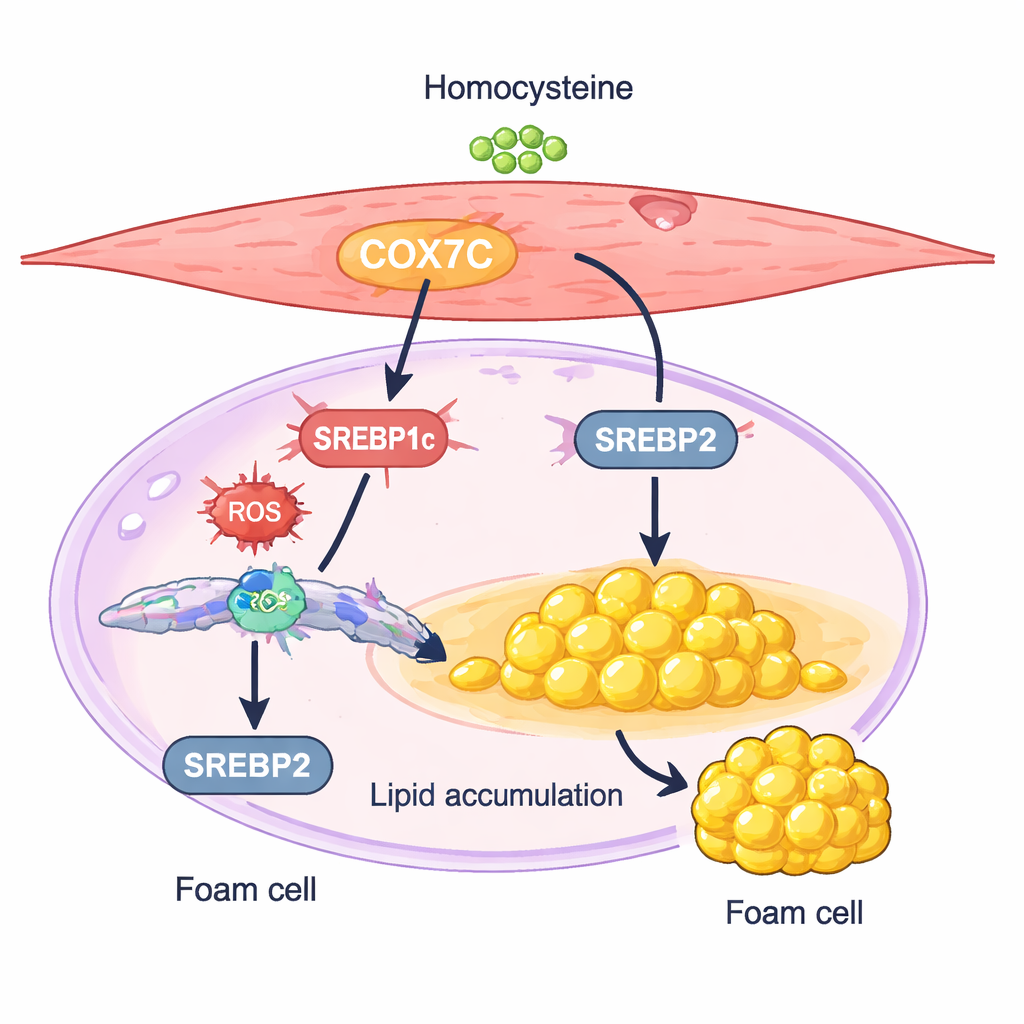
מתג מיטוכונדריאלי שדוחף תאים לאגור שומן
חלבון אחד, הנקרא COX7C, בלט כחשוד מעניין במיוחד. COX7C הוא מרכיב של תחנות הכוח של התא, המיטוכונדריה, שם הוא מסייע בניהול ייצור האנרגיה. בתאי השריר החלק שטופלו בהומוציסטאין, רמות COX7C היו גבוהות יותר מבביקורת. החוקרים הראו שהגברה נוספת של COX7C גרמה לתאים לאגור עוד יותר שומן ולהביע רמות גבוהות יותר של שני ויסותים מרכזיים של ייצור ליפידים, SREBP1c ו-SREBP2. השתקת COX7C הביאה לאפקט ההפוך: היא החלישה את פעילות ה-SREBP, צמצמה את הצטברות הכולסטרול והטריגליצרידים ופחתו השינויים הדמויי תאי הקצף. תוצאות אלו תומכות במודל שבו הומוציסטאין מעלה את COX7C במיטוכונדריה, מגדיל אותות מתח תאיים, וכתוצאה מפעיל את סינתזת השומנים המונחית על ידי SREBP, מה שמטה את תאי השריר החלק למצב של אגירת ליפידים.
מה משמעות הדבר לבריאות הלב ולטיפולים עתידיים
עבודה זו אינה מוכיחה עדיין מה קורה בעורקים אנושיים, והיא נערכה בתאים מושרים במעבדה במקום בחולים. עם זאת, היא מציעה מבט מפורט על האופן שבו הומוציסטאין מוגבר עשוי לסייע בהמרת תאי שריר עורקיים תומכים לתאי קצף מזיקים, ומזהה את COX7C וחלבונים קשורים כביו-מרקרים פוטנציאליים או מטרות לתרופות. עבור הקורא הכללי, המסר המרכזי הוא שמעבר ל"כולסטרול טוב" ו"כולסטרול רע", שינויים קטנים בכימיה של הדם — כמו עודף הומוציסטאין — יכולים לתכנת מחדש את דופן הכלי מבפנים. בזיהוי שחקנים מולקולריים כ-COX7C ונתיב ה-SREBP, מחקר זה מניח יסודות לאסטרטגיות עתידיות שמטרתן לעצור את היווצרות הפלאקים לפני שהם מופיעים, על ידי מניעת ממירי תאי העורק למחסני שומן מיקרוסקופיים.
ציטוט: Wang, X., Ma, X., Zhang, X. et al. Study on biomarkers of homocysteine-induced transformation of vascular smooth muscle cells into foam cells. Sci Rep 16, 7411 (2026). https://doi.org/10.1038/s41598-026-38763-6
מילות מפתח: אטרוסקלרוזיס, הומוציסטאין, תאי קצף, תאי שריר חלק של כלי דם, COX7C