Clear Sky Science · he
סינתזה כימית של נגזרות חדשות של aminopyrimidin-4-yl-1H-pyrazole כמעכבי טירוזין קינאז של הטחול (SYK)
למה חסימת אנזים בודד יכולה לעזור במאבק בסרטן ובדלקת
מערכת החיסון שלנו סומכת על תקשורת פנימית מהירה כדי ליידע תאים מתי לתקוף פולשים ומתי להרגיע. כשאותות אלה משתבשים, הם יכולים להזין מחלות אוטואימוניות וסרטן. המחקר הזה חוקר דרך מבטיחה להשתיק אותות תקולים אלה על ידי עיצוב מולקולות קטנות בדמות תרופה החוסמות באופן סלקטיבי אנזים מרכזי, טירוזין קינאז של הטחול (SYK), שנמצא קרוב לליבת תגובות חיסוניות רבות.
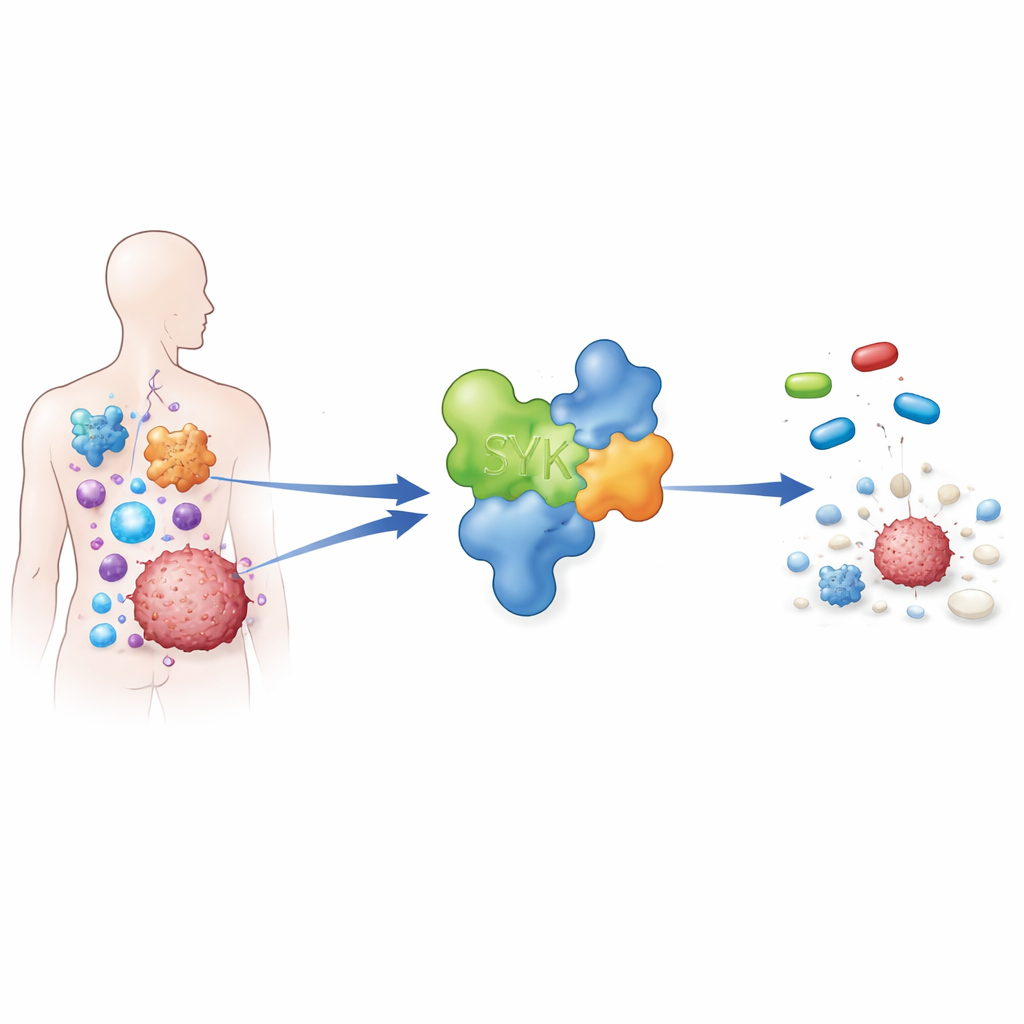
מנגנון איתות במרכזן של מחלות רבות
SYK פועל כמו מתג ראשי בתוך סוגים מסוימים של תאי חיסון. כאשר הוא מופעל, הוא מסייע לקדם דלקת, ייצור נוגדנים וצמיחת תאים. בסיטואציות בריאותיות זה מועיל במאבק בזיהומים. אך במצבים כגון דלקת מפרקים שגרונית, אסתמה וכמה סוגי סרטן בדם ובאורגניזם מוצק, פעילות SYK עלולה להפוך מופרזת, לשמור על תאי החיסון במצב פעיל ולתמוך בהישרדות הגידול. בשל תפקידו המרכזי הזה, חוקרים ברחבי העולם מפתחים תרופות חוסמות SYK שיהיו חזקות מספיק כדי לפעול אך מדויקות דיו כדי לא לפגוע בהרבה אנזימים אחרים ולמנוע תופעות לוואי.
בניית משפחה של מולקולות מותאמות
המחברים יצרו סדרה חדשה של מולקולות קרובות זו לזו המבוססות על שלד כימי משותף הנקרא aminopyrimidin-4-yl-1H-pyrazole. מתוך אבני בניין פשוטות הם חיברו את החלקים הללו שלב אחר שלב ולאחר מכן שינו חלק אחד במבנה כדי להפיק תשעה מועמדים סופיים. כל מולקולה נבדקה בקפידה באמצעי אנליזה סטנדרטיים כדי לאשר שמבנהה וטוהרה הם כמתוכנן. הגישה המודולרית איפשרה לצוות לחקור כיצד שינויים עדינים בצורה ובגמישות משפיעים על האינטראקציה של תרכובות אלה עם SYK.
צפייה כיצד התרכובות מתחבקות עם המטרה שלהן
לפני המעבדה, החוקרים השתמשו בסימולציות ממוחשבות כדי לראות כמה חזק כל מולקולה עשויה להידבק ל־SYK. חישובי docking העריכו עד כמה התרכובות מתאימות לכיס הקשירה של האנזים, והדגישו מועמד אחד, שמסומן כ־44, כבטוח במיוחד. סימולציות דינמיקת מולקולות מפורטות יותר, שבהן המורכב חלבון–תרופה נסקר על פני מאות ננו־שניות, הראו כי 44 יוצר שותפות יציבה במיוחד עם SYK. החלבון נשאר קומפקטי, מגעים מרכזיים שמרו על מקומם, והמערכת התייצבה לצורה אנרגטית נמוכה אחת עם רשת של קשרי מימן חזקים, במיוחד הכרוכים בחומצות אמינו כמו טריפטופן וסרין שמסייעות לשאת את המולקולה.
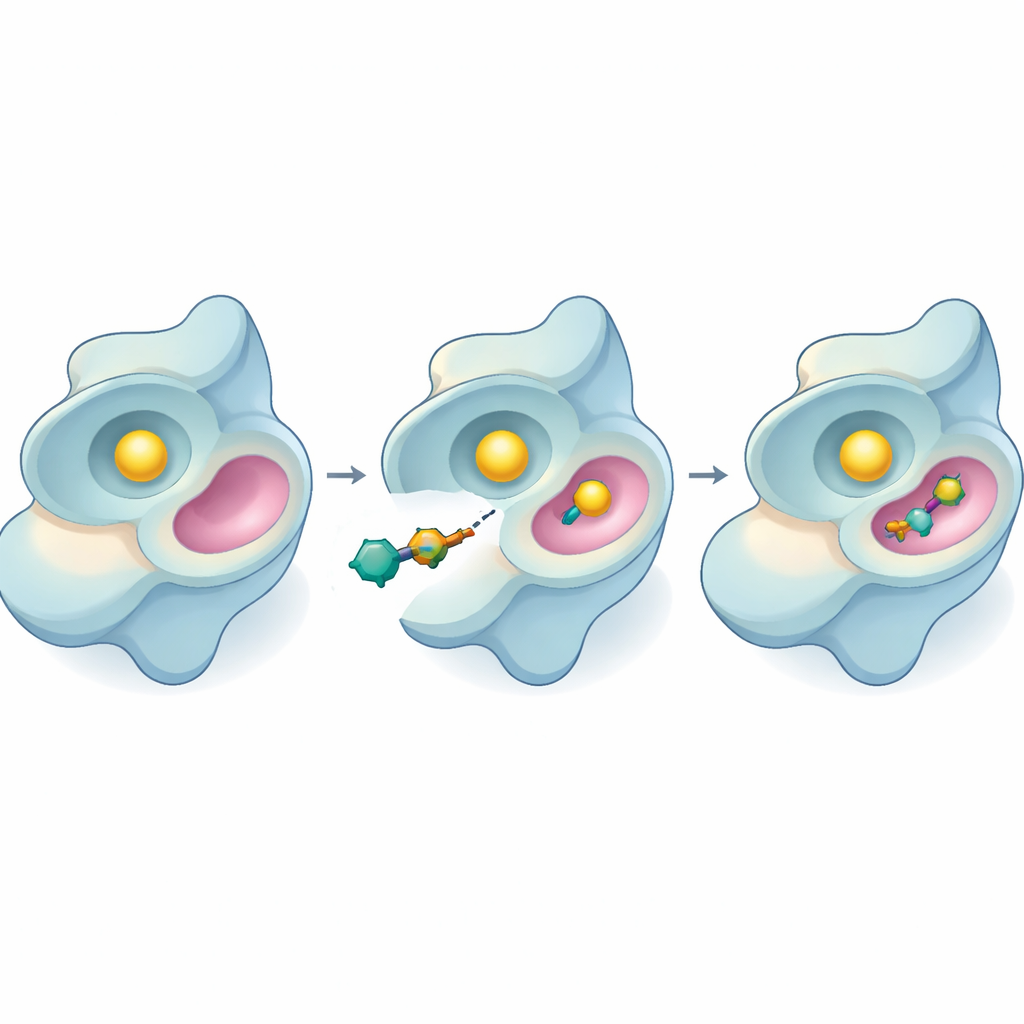
בדיקה של המעכבים החדשים
הצוות עבר לאחר מכן לניסויי מעבדה באמצעות מבחן מבוסס אור שמודד עד כמה באופן פעיל SYK צורך את מולקולת האנרגיה שלו, ATP. כמה מן התרכובות החדשות האטו את פעילות האנזים, אך שוב 44 בלטה. היא עיכבה את SYK בריכוזים נמוכים מאוד והפכה ליעילה יותר ככל שהייתה במגע עם האנזים זמן רב יותר. על ידי שינוי כמות התת־סטרטום הזמין, החוקרים יכלו להסיק כיצד 44 פועלת: במקום להתחרות ישירות עם ATP באתר הפעיל הראשי, נראה שהיא נקשרת לאתר שונה, אלוסטרי, ומשנה את התנהגות האנזים מרחוק. זה חשוב כי מעכבים אלוסטריים לעתים שומרים על האפקט שלהם גם כאשר רמות ATP גבוהות או כששינויים מוטציוניים משנים את האתר הראשי.
מה זה עלול להשפיע על טיפולים עתידיים
בצירוף, המודלים הממוחשבים והמדידות במעבדה מציירים תמונה עקבית: המולקולה 44 נקשרת בחוזקה ל־SYK, מחזיקה את האנזים במצב יציב ופחות גמיש, ומכבה את פעולתו באמצעות מנגנון עקיף שאינו תחרותי. עבור קורא שאינו מומחה, משמעות הדבר היא שהחוקרים זיהו מפתח כימי מתואם היטב שמתאים למנעול שחשוב במגוון מחלות מונעות חיסון, מבלי פשוט לחסום את הפתח הראשי. למרות שעוד נדרשת עבודה רבה—ובכלל זה ניסויים בתאים, בחיות ובפאנלים רחבים יותר של אנזימים קרובים—שלד זה מציע נקודת פתיחה מבטיחה לתרופות עתידיות שמטרתן להרגיע דלקת מזיקה ולעכב סוגים מסוימים של סרטן על ידי מיקוד ב־SYK.
ציטוט: Rajasheker, K.V., Pallavi, M.S., Singh, P. et al. Chemical synthesis of novel aminopyrimidin-4-yl-1H-pyrazole derivatives as spleen tyrosine kinase (SYK) inhibitors. Sci Rep 16, 8323 (2026). https://doi.org/10.1038/s41598-026-38719-w
מילות מפתח: טירוזין קינאז של הטחול, מעכבי קינאז, תרופות נגד סרטן, מחלות אוטואימוניות, תרופות אלוסטריות