Clear Sky Science · he
RNA ארוך (LncRNA) FTX מקדם פיברוזיס של שריר הלב על ידי ספיחת miR-335-3p לוויסות איתות TFEC/ILK
מדוע צלקת הלב חשובה
אי ספיקת לב משפיעה על עשרות מיליוני אנשים ברחבי העולם ולעתים מתפתחת בשקט במשך שנים. מניע מרכזי של הדרדרות זו הוא פיברוזיס של שריר הלב — הצטברות איטית ומתמשכת של רקמת צלקת שהופכת את הלב נוקשה ופחות מסוגל לשאוב דם. המחקר הזה חופר במעגל המולקולרי שמורה לתאי הלב להפקיד יותר מדי רקמת צלקת, ומזהה שרשרת מולקולרית חדשה שעשויה להוות מטרה להאטה או אפילו להפיכה של התהליך המזיק הזה.
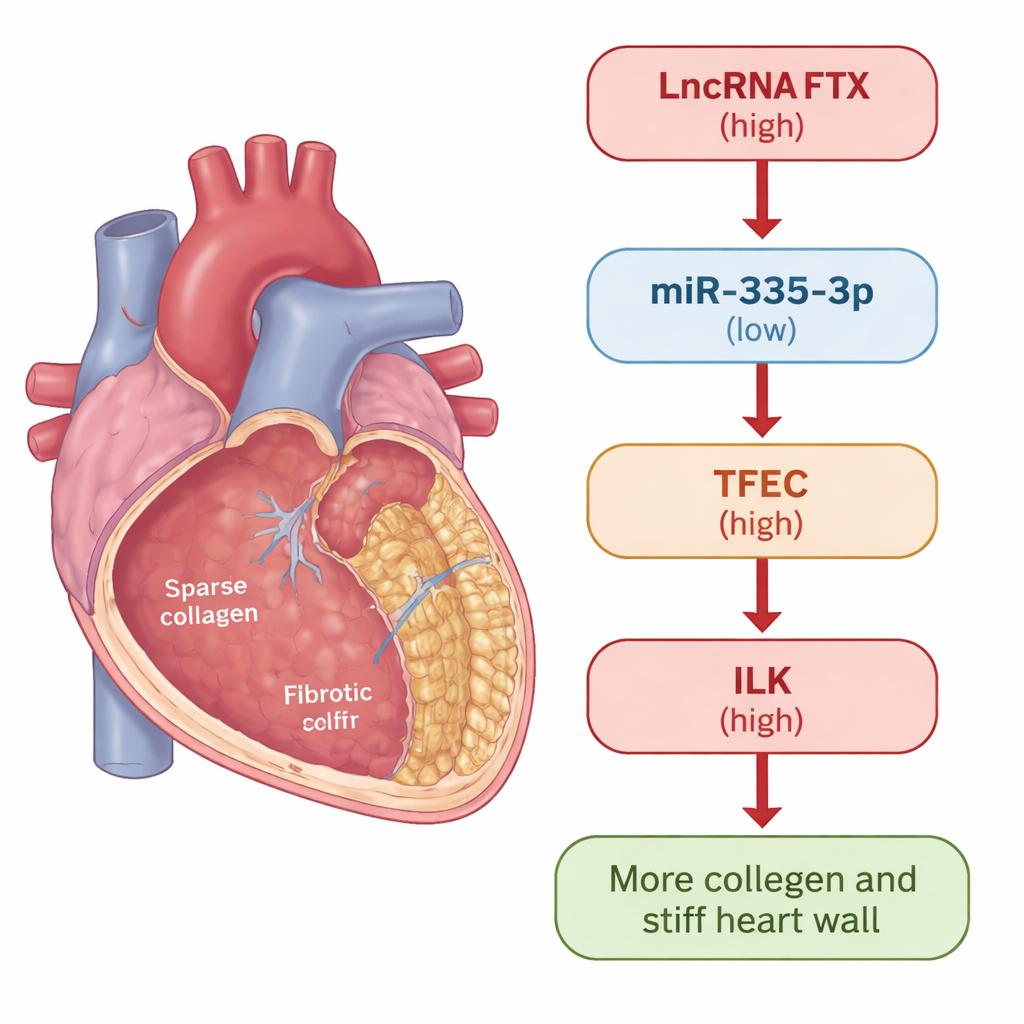
מבט קרוב יותר על צלקת הלב
כשמתרחשת פגיעה או עקה בלב, תאי תמיכה שנקראים פיברובלסטים קרדיאלים נכנסים לפעולה. בתיקון בריא הם מסייעים לטפל בנזק. אך במחלות כרוניות הם עלולים לעבור למצב פעיל מדי, לייצר עודף של קולגן ורכיבים אחרים של המטריקס החוץ‑תאי ולגרום בסופו של דבר להקשחת דפנות הלב. החוקרים השתמשו בשני מודלים כדי לחקור את התהליך: עכברים שטופלו באיזופרנטרול, שמעורר אמין פיברוזיס בלב, ופיברובלסטים קרדיאלים אנושיים שנחשפו למולקולת האיתות TGF-β1, שמפעילה צלקת ידועה. בשני המודלים מדדו כיצד גנים וחלבונים ספציפיים משתנים ככל שהפיברוזיס מתפתח.
תגובה שרשרת מזיקה בתוך התאים
הקבוצה התמקדה בגורם שעתוק בשם TFEC, חלבון שנמצא בגרעין התא ומפעיל גנים אחרים. הם מצאו ש‑TFEC, יחד עם חלבון נוסף שנקרא אינטגרין‑לינקד קינאז (ILK), עלו באופן עקבי כאשר הפיברובלסטים נדחקו למצב פיברוטי ויוצר צלקת. השתקת TFEC או ILK צמצמה באופן חד סמני של פיברוזיס, כולל סמנים קלאסיים כמו α‑smooth muscle actin וקולגנים I ו‑III, וכן דיכאה מסלול בקרת גדילה (Akt/GSK3β ואיתות Hippo) הידועים בקידום צלקת רקמה. ניסויים שמיפו קשירת DNA הראו ש‑TFEC נקשר ישירות לפרומוטור של גן ILK ומגביר את פעילותו, כך ש‑TFEC ממוקם בבירור מעל ILK בשרשרת האיתות הפרו‑פיברוטית.
מתגים של RNA ששולטים במפעיל הראשי
כדי להבין מה שולט ב‑TFEC עצמו, החוקרים פנו ל‑RNA שאינו מקודד — מולקולות RNA שאינן מייצרות חלבונים אך מווסתות פעילות גנים בדייקנות. הם זיהו RNA קטן, miR‑335‑3p, שהתקבל ברמות נמוכות בלב ובתאים פיברוטיים. העלאת רמות miR‑335‑3p הורידה את TFEC, בזמן שחסימתו הגיעה לעלייה ב‑TFEC, וניסויי מדווח הראו ש‑miR‑335‑3p נקשר ישירות להודעות ה‑TFEC ומשכך את ביטויין. לאחר מכן מצאו RNA ארוך שאינו מקודד בשם FTX, שהתגבר בפיברוזיס ויצר אינטראקציה פיזית עם miR‑335‑3p. FTX פעל כמו ספוג מולקולרי: הוא ספג את miR‑335‑3p ומנע מה‑miRNA הקטן להגביל את TFEC. כתוצאה מכך TFEC ו‑ILK עלו, והפיברובלסטים ייצרו יותר קולגן יוצר צלקת.
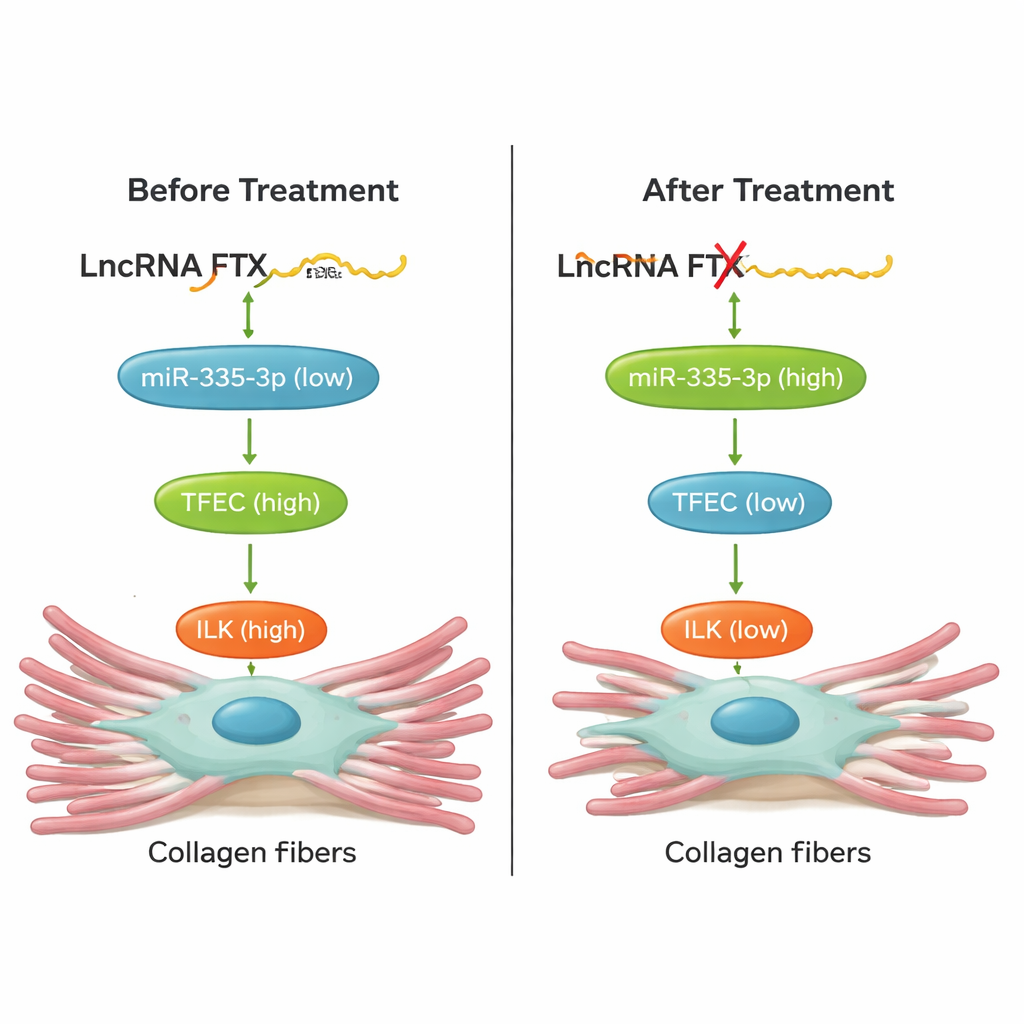
מתרבית תאים ללב חי
בחשיבותה, הקבוצה בחנה האם שיבוש השרשרת הזו יכול באמת להגן על לבבות בחיות. בעכברים שנחשפו לאיזופרנטרול, דיכוי TFEC, השתקת FTX בלב באמצעות וקטור תרפיה גנטית AAV9, או חיזוק miR‑335‑3p בעזרת "אגומיר" כימית‑מייצבת — כל אלה הביאו לפחות משק קולגן ולרמות נמוכות יותר של סמני פיברוזיס ברקמת הלב. ההתערבויות גם ישרו את תפקוד הלב: נפח פעימה ושבר פליטה התקרבו לנורמה וקפיצות מזיקות בדופק הוקטנו. ניסויי הצלה בתרבית תאים הראו ששינוי ברכיב אחד בציר FTX/miR‑335‑3p/TFEC/ILK שינה בצורה צפויה את הרכיבים האחרים, ואישרו שמדובר במסלול מקושר בקרת ולא בקורלציה רופפת.
מה משמעות הממצאים לטיפולים עתידיים
ללא‑מומחה, המסר המרכזי הוא שהמחברים זיהו "יגל שליטה" חדש לצלקת הלב. RNA ארוך בשם FTX מסיר את הבלמים (miR‑335‑3p) ממפסק ראשי (TFEC), שמפעיל אז את ILK ואת איתותי הפרו‑צלקת מטה, ומוביל להצטברות קולגן מופרזת ולהקשחת הלב. על ידי הקטנת FTX, שיקום miR‑335‑3p או חסימת TFEC ישירות, הצליחו בעכברים להפחית את הצלקת ולשפר את יכולת השאיבה. למרות שנדרשים עוד מחקרים כדי לאשר את המסלול הזה בחולים אנושיים ולפתח טיפולים בטוחים, שרשרת ויסות מבוססת RNA זו מציעה מספר נקודות מתבטחות להתערבות באי‑ספיקת לב המונעת על‑ידי פיברוזיס.
ציטוט: Yao, F., He, Z., Zheng, C. et al. LncRNA FTX promotes myocardial fibrosis by sponging miR-335-3p to regulate TFEC/ILK signaling. Sci Rep 16, 7340 (2026). https://doi.org/10.1038/s41598-026-38615-3
מילות מפתח: צלקת של שריר הלב, אי ספיקת לב, RNA שאינו מקודד, פיברובלסטים קרדיאלים, איתות פיברוטי