Clear Sky Science · he
תאי T מופעלים גורמים לאפופטוזה בתאי אדנוקרצינומה של הריאה A549 באמצעות כניסת סידן מתווכת על‑ידי TRPV4
מדוע מחקר זה חשוב עבור סרטן הריאה
סרטן הריאה נותר אחד הסוגים הקטלניים ביותר של סרטן, בין היתר משום שהגידולים לעתים קרובות מפתחים עמידות לטיפולים סטנדרטיים כמו כימותרפיה והקרנה. בשנים האחרונות, ניצול מערכת החיסון של הגוף הציע תקווה חדשה. מחקר זה בוחן אספקט חדש של הרעיון: הוא מראה כיצד סוג מסוים של תא חיסון, תאי T מופעלים, יכולים לדחוף תאי סרטן ריאה לכיוון ההשמדה העצמית על‑ידי כפייה עליהם לקלוט סידן דרך ״שער״ מולקולרי הידוע כ‑TRPV4. הבנת הנתיב הזה עשויה לסייע למדענים לתכנן אימונותרפיות חזקות ומדויקות יותר.
לוחמי מערכת החיסון פוגשים תאי גידול ריאה
החוקרים התרכזו בתאי אדנוקרצינומה של הריאה מהאדם הידועים כ‑A549, מודל נפוץ לסרטן ריאות שאינו מסוג תאים זעירים. הם שילבו תאי סרטן אלה עם תאי Jurkat, תחליף לתאי T קטלניים בגוף שהמטרה שלהם בדרך כלל היא לזהות ולהשמיד תאים נגועים או ממאירים. על‑ידי הפעלת תאי Jurkat כימית, הצוות חיקה את מצב הערנות הגבוה של תאים מעורבים בתגובה חיסונית אמיתית. לאחר מכן הם עירבו תאי T מופעלים או לא מופעלים עם תאי סרטן הריאה ביחסים שונים וצפו בהתנהגותם לאורך יום עד שלושה ימים, כששימו לב במיוחד כמה תאי סרטן שורדים וכמה עוברים מוות מתוכנן של תאים, כלומר אפופטוזה.
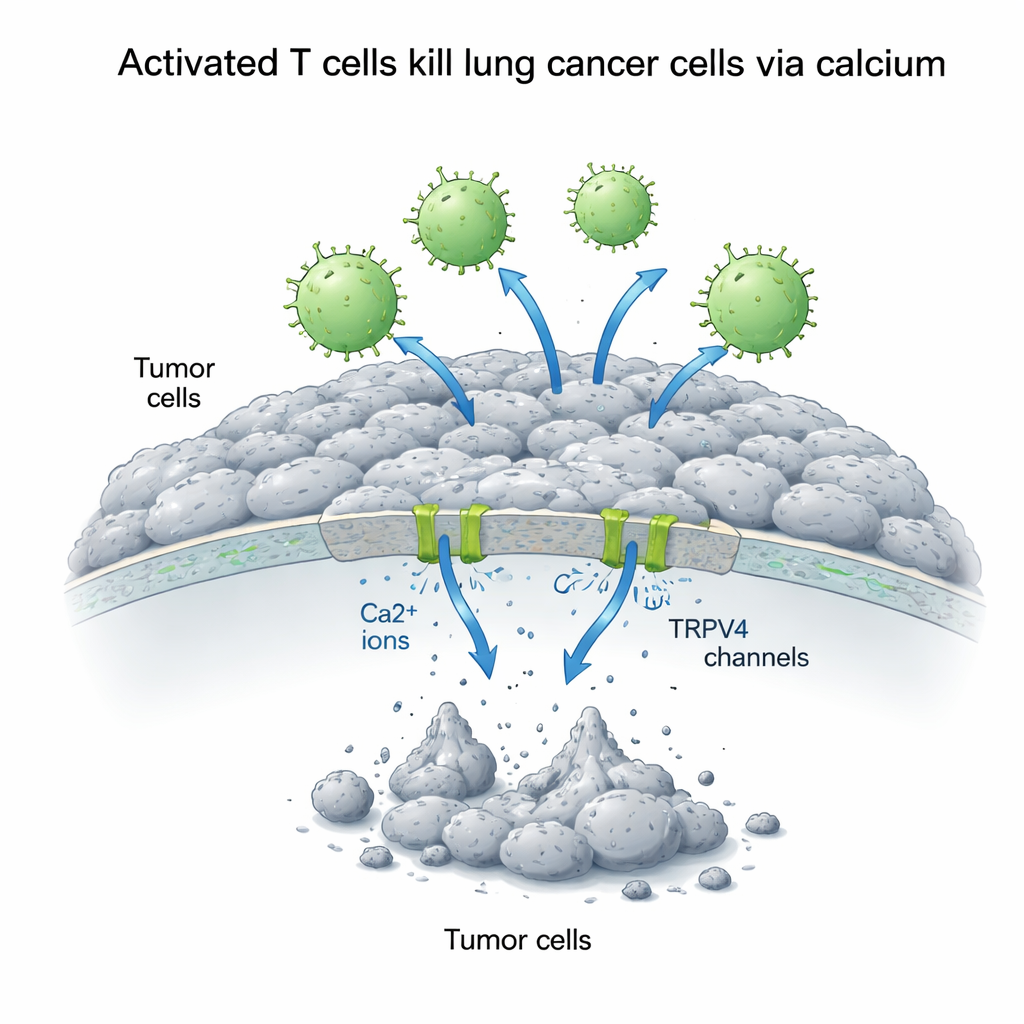
הסידן כאות דו‑חיובי לתאי סרטן
הסידן בתוך התאים מתפקד כמתג אות רב‑תכליתי שיכול לעודד צמיחה או לעורר מוות, בהתאם לאופן שבו הוא מטופל. המדענים הגדילו את כמות הסידן מחוץ לתאי A549 ומדדו כיצד הדבר משפיע על המאבק בין תאי T לגידול. להפתעתם, תוספת סידן לבדה שיפרה את גדילת תאי הסרטן, מה שמצביע על כך שבתנאים שקטים הסידן מזין מסלולי הישרדות. אך כאשר תאי T מופעלים היו נוכחים, התמונה הופכת: סידן חיצוני גבוה הגביר באופן דרמטי את ההרג המונע על‑ידי תאי T. במשך 72 שעות, הישרדות תאי הסרטן ירדה לפחות משליש מהרמה הרגילה כאשר שילבו תאי T מופעלים וסידן נוסף, בעוד שתאי T לא מופעלים השפיעו מעט ואף יכלו לתמוך בצמיחה כאשר נוסף סידן.
"שער" סידן המקושר ללחץ חמצוני ומוות תאי
כדי להבין כיצד המתג הזה מחליף צמיחה למוות, הצוות בחן את TRPV4, תעלת חלבון בממברנת התא המאפשרת לסידן לזרום פנימה. באמצעות ניתוח חלבונים הם מצאו שרמות TRPV4 עלו בחדות כאשר תאי A549 נחשפו לסידן נוסף, בין אם נוכחות תאי T ובין אם לאו, והיו הגבוהות ביותר כאשר סידן ותאי T מופעלים הופעלו יחד. באותו זמן, תאי הסרטן הראו סימני מתח חמצוני ברורים: המאזן הטהה הרחק מאנטיאוקסידנטים מגנים (קיבולת אנטיאוקסידנט כוללת נמוכה יותר) וכיוון החלק לעבר חמצונים מזיקים (מצב חמצון כולל גבוה יותר). ציטומטריית זרימה, טכניקה המסמנת תאים בצביעות פלורסנטיות, אישרה שתאי T מופעלים גרמו לזינוק הן בשלבים מוקדמים והן בשלבים מאוחרים של אפופטוזה, במיוחד כשהסידן היה בשפע. יחד, תצפיות אלה מצביעות על שרשרת אירועים שבה תעלות TRPV4 מקבלות יותר סידן, מה שמניע מתח כימי בתוך התא ודוחף אותו לעבר מוות.
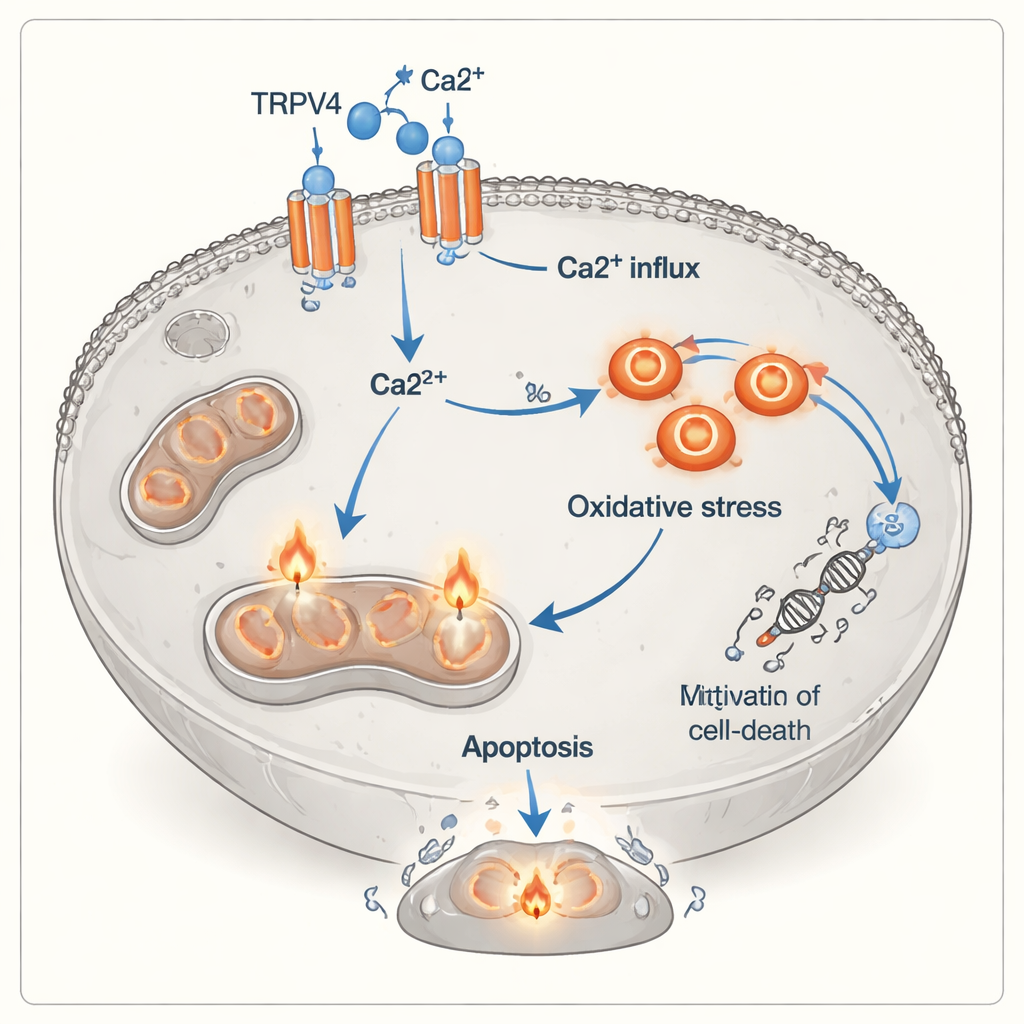
שכבה חדשה בדרך שבה תאי חיסון הורגים גידולים
באופן קלאסי, תאי T קטלניים הורסים את מטרותיהם על‑ידי שחרור חלבונים רעלניים או על‑ידי הפעלת קולטני מוות על פני התא הסרטני. מחקר זה מציע שיש נתיב נוסף, עקיף יותר: אותות מתאי T מופעלים — כולל מולקולות דלקתיות ומגע תאי‑תאי צמוד — נראים כגורמים לכך שתאי סרטן הריאה נעשים תלויים יותר ב‑TRPV4 ופגיעים יותר לעומס סידן ולנזק חמצוני. במבט זה TRPV4 פועל כמתג המעלות את הרגישות, שהופך סידן שבתנאים אחרים מקדם צמיחה לאות קטלני. למרות שהניסויים נערכו בכלים ובשורה תאית יחידה, הם מדגישים גשר פוטנציאלי חשוב בין התקפת החיסון, תעלת יונים ומכונת הלחץ התוך‑תאית של תאי הגידול.
מה זה עשוי ללמד על טיפולים עתידיים
ללא מומחיות מיוחדת, המסקנה היא שהצלחת אימונותרפיה עשויה להיות תלויה לא רק בחיזוק תאי T, אלא גם בהפיכת תאי הסרטן לקלים יותר להריסה. על‑ידי מיקוד ב‑TRPV4 או בתעלות סידן דומות, יתכן שבעתיד ניתן יהיה להגביר את יכולת תאי T להכחיד גידולי ריאה או לכוונן טיפולים כך שלא יפגעו ברקמות בריאות. העבודה עדיין נמצאת בשלבים מוקדמים, והמחברים מדגישים את הצורך בניסויים נוספים בחיות ובמודלים מורכבים יותר. כך או כך, גילוי ציר TRPV4–סידן–מתח חמצוני מוסיף יעד מבטיח חדש לארגז הכלים לשיפור טיפולים מבוססי חיסון נגד סרטן הריאה.
ציטוט: Alavi, F., Kazemi-Lomedasht, F., Eftekhari, Z. et al. Activated T cells induce apoptosis in A549 lung adenocarcinoma cells via TRPV4-mediated calcium influx. Sci Rep 16, 7155 (2026). https://doi.org/10.1038/s41598-026-38589-2
מילות מפתח: אימונותרפיה בסרטן הריאה, תאי T, אותות סידן, תעלת TRPV4, מתח חמצוני