Clear Sky Science · he
אופטימיזציה של זמרי קשירה לגלקטין‑3 באמצעות סינתזה מקומית של רכיבים מרובים ומסה במצב טבעי
מדוע זה חשוב לרפואה של העתיד
תרופות מודרניות רבות פועלות על ידי הידוק אל חלבונים בגופנו, אך מציאת מולקולה קטנה שנצמדת בחוזקה ובסלקטיביות לנקודה הנכונה היא תהליך איטי, יקר ולעתים מתסכל. המחקר הזה מציג דרך מהירה יותר לכוונן מולקולות כאלה ישירות בנוכחות חלבון המטרה, ולאחר מכן לזהות את המנצחות באמצעות שיטת שבח רגישת‑משקל. הכותבים מדגימים את השיטה על גלקטין‑3, חלבון המקושר לצמיחת סרטן, ומגיעים למולקולת מועמדת בעלת מאפיינים של תרופה שנקשרת בעוצמה השוותה לזו של כמה מהתרכובות הטובות הקיימות — אך בכיס בלתי צפוי על פני שטח החלבון.

לתכנן מחדש את הציד אחרי מולקולות מובילות
אופטימיזציה מסורתית של תרופה דומה למשחק ניחושים יקר. כימאים משנים מולקולה מוצא שלב אחר שלב, בודקים כל גרסה ומקווים לשפר את חוזק הקשירה לחלבון המטרה. אך פני החלבון גמישות, מולקולות מים מכשילות את הקשר, ואירוע הקשירה עצמו עלול לעצב מחדש את החלבון — מה שהופך חיזויים ממחשב ללא מהימנים. גם כאשר יש מבנה ברזולוציה גבוהה, אין ערובה ששינוי מוצע ישפר את התוצאה. שיטות "מונחות‑מטרה" קיימות מנסות לאפשר לחלבון לבחור לעצמו שותפים מתוך מאגר אבני בניין, אך שיטות אלה עדיין תלויות בניתוחים מורכבים ובאותות עקיפים כדי להסיק איזו תרכובת אכן נקשרת בצורה הטובה ביותר.
תנו לחלבון לבחור — ואז שקלו את המנצחות
החוקרים שילבו שתי רעיונות לזרימת עבודה אחידה. ראשית, הם השתמשו בתגובה כימית הפיכה שמקשרת ליבה מבוססת סוכר להרבה קבוצות צד שונות במבחנה אחת, ויוצרת תערובת של מולקולות קרובות זו לזו. על‑ידי כוונון היחסים ההתחלתיים בקפידה, המוצרים הסופיים מגיעים למצב מאוזן הנשלט על‑ידי כללי ריכוז פשוטים, מה שמסייע להסתנכרן בכמויות למרות הבדלים בריאקטיביות הגולמית. שנית, הם חשפו את התערובת לגלקטין‑3 ובחנו אותה באמצעות מסת מסה במצב טבעי — גרסה של ספקטרומטריית מסה ששומרת על זוגות חלבון–מולקולה שלמים בתמיסה עדינה הדומה למים. מכיוון שלכל מועמד יש מסה מובחנת, הכלי יכול לזהות ישירות אילו מולקולות קשורות באמת לחלבון, ללא תגיות או סמנים חיצוניים.
מתערובות צפופות לאלוף בולט
בעזרת הגדרות אלה יצר הצוות עשרות קושרים לגלקטין‑3 על ידי הצמדה של קבוצות צד שונות לליבת סוכר בהשראת מעכב מוכר, GB1107. הם חילקו 35 יחידות הידראזיד שונות לקבוצות ניהול, יצרו את כל הצירופים in situ, ואז הוסיפו את גלקטין‑3. מסת המסה במצב טבעי הדגישה את התרכובות שנראו נוסקות לעתים קרובות יחד עם החלבון, וסימנה אותן כזיהויים ראשוניים. בדיקת יציבות תרמית לאחר מכן, שמודדת כיצד תרכובת מייצבת את החלבון בחימום, סיננה חיוביים שווא שנבעו מאקצנטי מדידה בגז. נשארו שלושה מועמדים מובילים, ומדידות קשירה מפורטות המבוססות חום הראו שלאחד מהם, שנקרא GalAldBZ20, היה קשירה חזקה במיוחד לגלקטין‑3, בטווח תת‑מיקרומולרי.
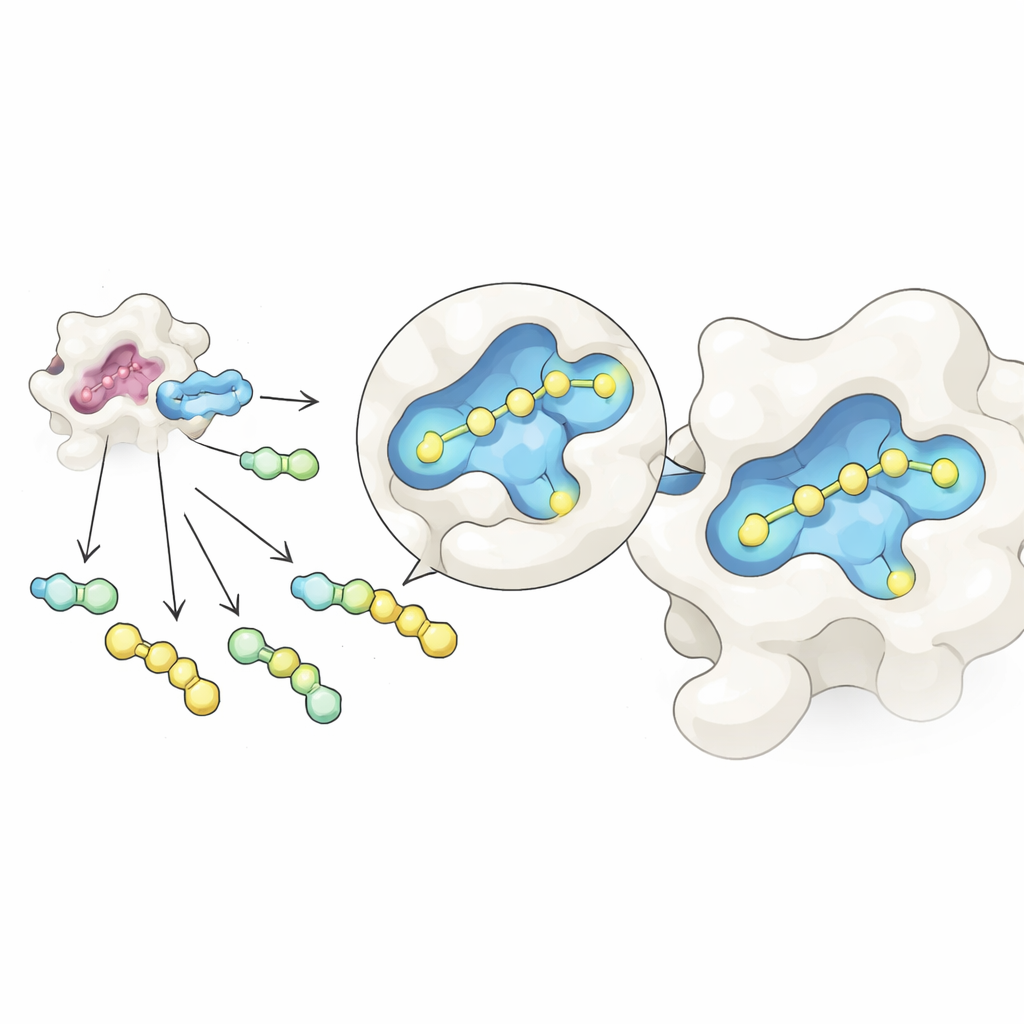
גילוי כיס חבוי וחיזוקו
ההפתעה הבאה התרחשה כשצפו החוקרים כיצד GalAldBZ20 ישב על פני שטח גלקטין‑3. רוב הקושרים הידועים משתמשים בכיס "אלפא" הסמוך לאתר קשירת הסוכר, אך שיטות מבניות וסימולציות מחשב הראו כי GalAldBZ20 העדיף במקום זאת כיס שכונתי "בטא". קריסטלוגרפיית קרני‑X הצביעה על כך, תהודה מגנטית גרעינית בתמיסה גילתה קונפורמציות מקומיות מרובות בקרבת הכיס, וסימולציות דינמיקת מולקולות תמכו במודל שבו טבעת נושאת ניטרו על המולקולה מתמקמת בתוך אתר הבטא. מתוך הנחה שניתן לייצב סידור זה ביתר חוסן, הכימאים עיצבו מחדש את הקושר הכימי בין הסוכר לטבעת הניטרו כדי לעודד אינטראקציות פולריות חדשות עם החלבון ולהפחית גמישות.
הפיכת מסך חכם למועמד חזק
עם התובנה הזו, הצוות סינתז סט קטן של מולקולות המשך קשיחות יותר ששמרו על אותו סוכר וטבעת ניטרו אך שינו את המחבר ביניהם. גרסה אחת, N‑גלקטוסיד (תרכובת 5), בלטה: היא נקשרה לגלקטין‑3 בערך פי עשרה חזק יותר מהזיהוי המקורי, והגיעה לחוזק קשירה השווה ל‑GB1107, ועדיין העדיפה את כיס הבטא. מבנה גבישי ברזולוציה גבוהה מאוד הראה צפיפות ברורה לטבעת הניטרו המתמקמת בכיס, נתמכת על‑ידי מספר קשרי מימן ומגע קטיון‑π עם חומצות אמינו מרכזיות. כשהקבוצה הניטרו הוסרה או הוחלפה במתיל פשוט, הקשירה הוחלשה בצורה ניכרת, מה שמדגיש את חשיבותה. מכיוון שגלקטין‑1, חלבון קרוב, חסר את כיס הבטא הזה, התרכובת החדשה עשויה בסופו של דבר להציע סלקטיביות טובה יותר — תכונה חשובה בעיצוב תרופות.
מסקנות לעתיד גילוי התרופות
במונחים נגישים, עבודה זו מראה שאפשר לערבב יחד רבים של מולקולות קרובות, לתת לחלבון רלוונטי למחלה "לבחור" את המועדפות עליו, ואז לשקול ישירות את זוגות החלבון–מולקולה כדי לראות מהן הנצמדות ביותר. כשהוחלה על גלקטין‑3, האסטרטגיה גילתה באופן בלתי צפוי וחיזקה קשירה לכיס פחות מחוקר, והניבה תרכובת שמתחרה בכמה המעכבים הטובים הקיימים ואף עשויה לשמש כמולקולה מובילה לתרופות אנטי‑סרטן חדשות. ברמה הרחבה יותר, שילוב סינתזה in situ עם מסת מסה במצב טבעי מציע קיצור דרך כללי לכיול מולקולות מובילות נגד חלבונים עם אתרי קשירה מרובים אפשריים, וחוסך זמן, חומרים ומאמצים בשלבי הגילוי המוקדמים של תרופות.
ציטוט: Hoshi, K., Konuma, T., Taguchi, R. et al. Optimization of galectin-3 binding agents by in situ multiple compound synthesis and native mass spectrometry. Sci Rep 16, 8453 (2026). https://doi.org/10.1038/s41598-026-38570-z
מילות מפתח: מעכבי גלקטין‑3, מסת מסה במצב טבעי, גילוי תרופות מבוסס שבירה, סינתזה מונחית‑מטרה, מולקולות מובילות לסרטן