Clear Sky Science · he
עיכוב ממוקד של HDAC8 באמצעות תרכובות [1,2,4]triazolo[4,3-a]quinoline שאינן הידרוקסאמט
תקווה חדשה לסרטן ילדים
נוירובלסטומה היא סרטן ילדים אגרסיבי שמקורו בתאי עצב ולעיתים קרובות קשה לטיפול לאחר התפשטותו. המחקר הזה חוקר גישה חדשה להאטה או להשמדה של תאי נוירובלסטומה על־ידי כיבוי מתג תאי מרכזי בשם HDAC8. על‑ידי פיתוח משפחה חדשה של מולקולות בעלות מאפיינים דמויי־תרופה הפועלות במדויק על המתג הזה, החוקרים שואפים ליצור טיפולים שיהיו גם יעילים יותר נגד הגידול וגם עדינים יותר כלפי שאר הגוף.
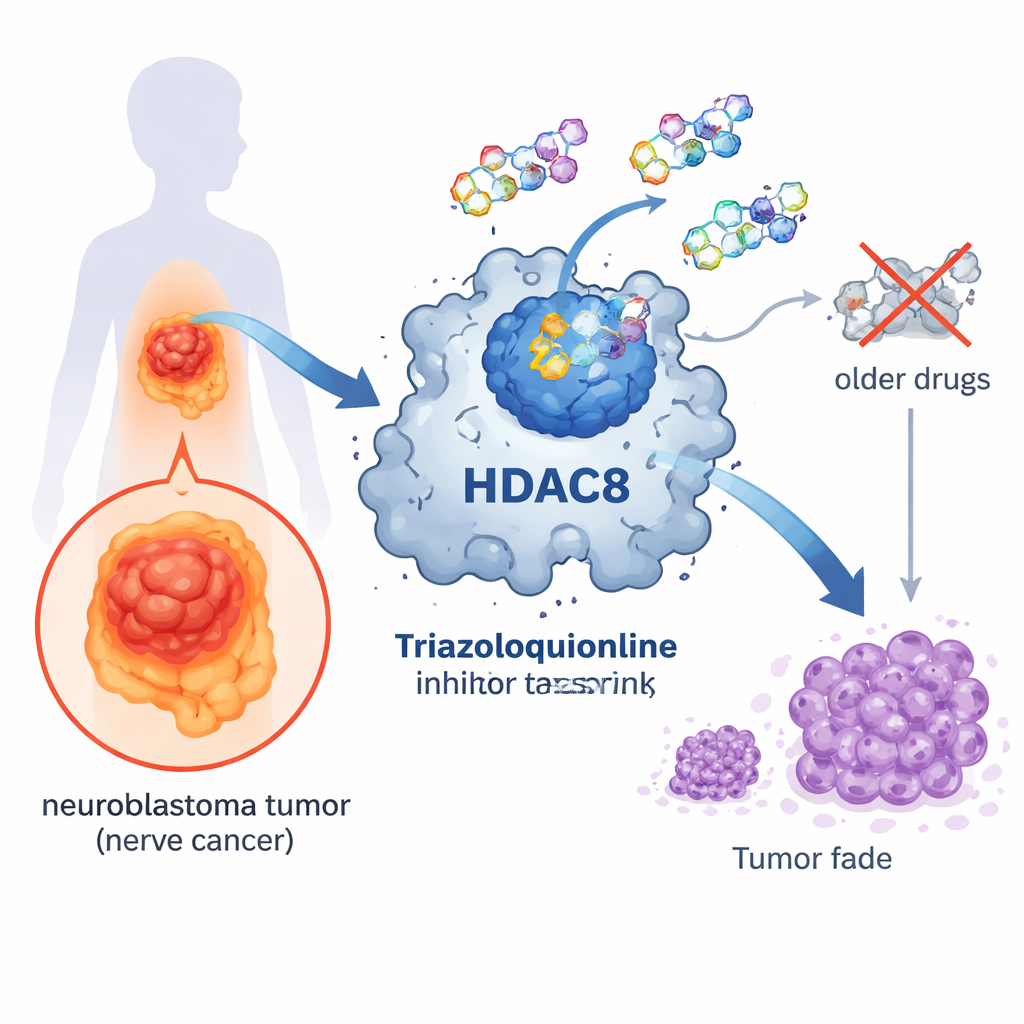
מתג מולקולרי במרכז הסרטן
בתאים שלנו, גנים נדלקים וכבים כל הזמן. מערכת בקרה חשובה נשענת על תגיות כימיות קטנות שנקראות קבוצות אצטיל שמתחברות לחלבונים המשויכים ל‑DNA. אנזימים שנקראים היסטון דאצטילאזות (HDACים) מסירים תגיות אלה, מה שדוחס את ה‑DNA ומטה את פעילות הגנים ברוב המקרים. HDAC8 הוא אחד מחברי משפחת האנזימים הזו וקושר למספר סוגי סרטן, כולל נוירובלסטומה. כאשר HDAC8 פעיל יתר על המידה, תאי סרטן יכולים לגדול, לשרוד ולהתפשט ביתר קלות, מה שהופך אותו למטרה אטרקטיבית לתרופות חדשות.
מגבלות של תרופות HDAC ישנות
מספר תרופות החוסמות HDAC כבר מותרות לשימוש בחלק מסוגי סרטן הדם, אך הן נוטות לפגוע בכמה סוגי HDAC בו‑זמנית. רוב התרופות הללו משתמשות בקבוצת הידרוקסאמט כדי לאחוז ביון מתכת באתר הפעיל של האנזים. אף על פי שהקבוצה יעילה, היא נקשרת למתכות בעוצמה רבה, מה שעלול לגרום לתופעות לוואי ולהגביל את היכולת של התרופה להבחין בין HDACים שונים. כתוצאה מכך עלולים להופיע רעילות ופגיעה בתאים נורמליים לצד תאי הסרטן. לכן חיפשו החוקרים עיצובים כימיים חלופיים שישמרו על היתרונות האנטי‑סרטן תוך הפחתת הנזקים הבלתי רצויים.
עיצוב כיתה חדשה של מעכבים ממוקדים
בעבודה זו תכננה וסינתזה הקבוצה 21 תרכובות חדשות המבוססות על שלד טריאזולוקינולין, המחובר דרך מחבר גמיש לאזור "+alpha‑amino amide" שיכול לקשור את אטום אבץ באתר הפעיל של HDAC8. באמצעות עיצוב מונחה מחשב בחרו במבנה זה כדי להתאים לתעלת "שחרור אצטט" צרה הייחודית ל‑HDAC8, תכונה מבנית המסייעת להשגת ספציפיות גבוהה. מחקרי דוקינג מפורטים וסימולציות דינמיקה מולקולרית הראו שמספר מהמולקולות החדשות — במיוחד אלה המסומנות 9m ו‑9r — יוצרות אינטראקציות יציבות ומתמשכות בתוך כיס ה‑HDAC8 ונקשרות בחוזקה זהה או חזקה יותר ממעכב ייחוס ידוע. חשוב מכך, בדיקות ביוכימיות אישרו שהתרכובות הטובות ביותר חוסמות בעוצמה את HDAC8 ומשאירות את שאר חברי משפחת ה‑HDAC במידה רבה ללא שינוי.
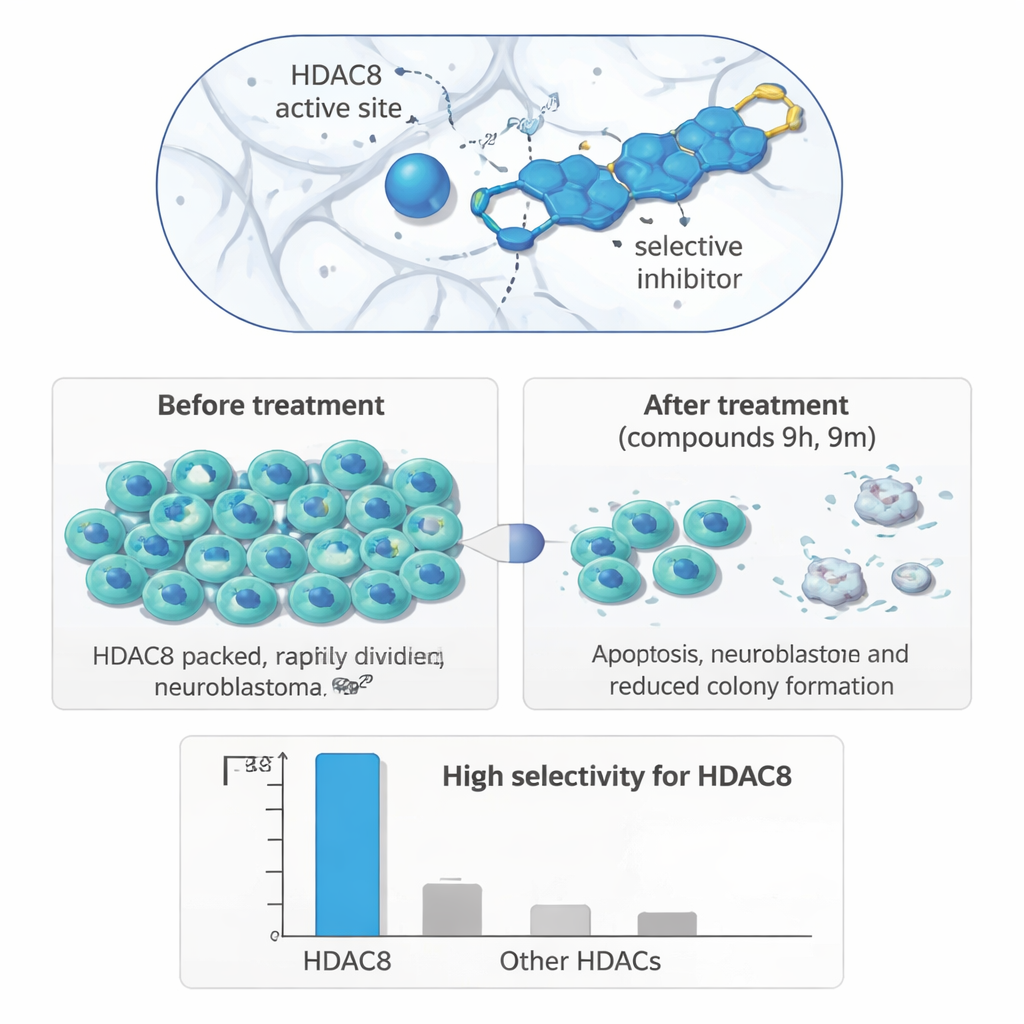
מצטפק לנוזל מבחנה לתאי גידול
כדי לבדוק האם המיקוד המדויק הזה באנזים מתורגם לאפקטים ביולוגיים שימושיים, החוקרים בדקו את תרכובותיהם על סדרה של תאי אדם. בתאי נוירובלסטומה (IMR‑32) בלטו במיוחד שתי מולקולות, 9h ו‑9m: הן צמצמו את גדילת התאים בריכוזים מיקרומולריים ועשו זאת בעוצמה רבה יותר בניורובלסטומה מאשר בתאי סרטן שד או המעי וכן בתאי כליה שאינם סרטניים. ניסויי היווצרות מושבות לטווח ארוך הראו שתאי נוירובלסטומה שטופלו איבדו חלק גדול מיכולת החידוש שלהם לאחר חשיפה לתרופות. במבחן ריפוי פצע, שבודק כמה מהר תאים נודדים לסגור שריטה בשכבת תאים, שתי התרכובות האטו את תנועת תאי הנוירובלסטומה, מרמז על פוטנציאל מופחת להתפשטות גרורתית.
בחינת המנגנון שבו התרכובות הורגות תאי סרטן
ניסויים בזרימת תאים גילו ש‑9h ו‑9m מעוררות מוות מתוכנת של תאים (אפופטוזיס) בתאי נוירובלסטומה וגורמות לצבירה של תאים בשלב של מחזור התא המקושר לנזק ב‑DNA או למוות (Sub‑G1). כדי לאשר שההשפעות האלה באות באמת מחסימת HDAC8, הצוות מדד את מצב האצטילציה של חלבון בשם SMC3, מטרה ידועה של HDAC8 המעורבת בשמירה על תקשורת כרומוזומים אחיות בזמן חלוקת התא. כאשר HDAC8 מעוכב, רמות SMC3 אצטילטי מצטברות. לאחר טיפול ב‑9h או 9m רמות ה‑SMC3 המאצטל עלו באופן חד, בעוד שסך חלבון SMC3 לא השתנה — ראיה חזקה לכך שהתרכובות הללו פוגעות ישירות ב‑HDAC8 בתאים חיים ומפריעות לתפקודו התקין בשליטה על הכרומוזומים.
מה המשמעות של זה לטיפולים עתידיים
במבט כולל, הכימיה, המודלים הממוחשבים, בדיקות האנזים והניסויים בתאים מציירים תמונה עקבית: התרכובות הטריאזולוקינוליניות החדשות הן חוסמות חזקות ובעלות ספציפיות גבוהה ל‑HDAC8 שיכולות לעצור את הגדילה והפיזור של תאי נוירובלסטומה תוך שמירה על שאר אנזימי ה‑HDAC. מכיוון שהן נמנעות מקבוצת ההידרוקסאמט המסורתית, ייתכן שהן יציעו דרך בטוחה יותר לרתום את HDAC8 כמטרה טיפולית. למרות שעדיין דרוש עבודה רבה — במיוחד ניסויים בחיות וניסויים קליניים עתידיים — המחקר הזה מניח בסיס איתן לפיתוח תרופות מדויקות יותר נגד נוירובלסטומה של ילדים ואולי גם נגד מחלות נוספות המונעות על‑ידי HDAC8.
ציטוט: Bandaru, N.V.M.R., Fathima, A., Sengar, S. et al. Targeted HDAC8 inhibition with non-hydroxamate [1,2,4]triazolo[4,3-a] quinoline compounds. Sci Rep 16, 7472 (2026). https://doi.org/10.1038/s41598-026-38490-y
מילות מפתח: מעכבי HDAC8, נוירובלסטומה, טיפול אפיגנטי, טריאזולוקינולין, תרופות ממוקדות בסרטן