Clear Sky Science · he
CNOT2 /c-Myc/STAT3 סיגנלינג מעורב באופן קריטי בגליקוליזה מתווכת אפופטוזה של בנזיל איזותיוציאנט בחסר-תא כבד
מרכיב לוחם‑סרטן על הצלחת שלכם
בנזיל איזותיוציאנט, או BITC בקיצור, הוא חומר טבעי המצוי בירקות מוכרים כמו ברוקולי, כרוב וקייל. הרופאים ידעו לאורך זמן שאנשים שאוכלים יותר מהמזונות האלה נוטים לסבול פחות ממחלת סרטן, אך מנגנוני הפעולה של רכיבי הצמחים הספציפיים האלה — כיצד הם מאטים או הורגים תאי סרטן — עדיין נחקרים. מחקר זה בוחן כיצד BITC משפיע על תאי סרטן כבד במעבדה ומחשף קישור מפתיע בין האופן שבו תאי הסרטן ‘‘שרפים’’ סוכר לבין האופן שבו נדחפים להרס עצמי.
מדוע סרטן הכבד צריך אופציות טובות יותר
סרטן הכבד הוא אחד מסוגי הסרטן הקטלניים ביותר ברחבי העולם, וההפטוצלולר קרצינומה הוא הצורה הנפוצה ביותר שלו. גם עם ניתוח, כימותרפיה ותרופות ממוקדות, גידולים רבים חוזרים או מפסיקים להגיב לטיפול. סיבה אחת היא שתאי סרטן משנים את דרכי השימוש שלהם באנרגיה: במקום להסתמך בעיקר על חמצן במיטוכונדריה, הם שורפים כמויות גדולות של סוכר במהירות בתהליך שמכונה לעתים קרובות «אפקט וורבורג». שימוש מעוות זה בסוכר מסייע לתאי הסרטן לגדול מהר יותר ולהיות עמידים יותר למוות. מציאת דרכים בטוחות להפריע לאספקת האנרגיה הזו, ובמיוחד שימוש במולקולות שמקורן במזון, היא אסטרטגיה אטרקטיבית.
בדיקת כימיקל מצמח על תאי סרטן כבד
החוקרים טיפלו בשתי שורות תאים של סרטן כבד אנושי, SK-Hep1 ו‑Huh7, במינונים עולים של BITC. ככל שהמינון עלה, פחות תאים שרדו, מה שמעיד על רעילות של BITC לתאי סרטן כבד בתנאים אלה. כאשר בחנו ביתר פירוט מה קורה בתוך התאים, הם מצאו סימני מפתח של ת programmed cell death, או אפופטוזה. חלבונים מרכזיים שבדרך כלל קיימים בצורתם ה‘‘לא־פעילה’’ לפני חיתוך במהלך האפופטוזה, כגון PARP וקספאז‑3, הופחתו בצורתם השלמה, או ה‘‘פרו‑’’ שלהם. בדיקות פלואורוציטומטריה הראו גם יותר תאים בחלקה sub‑G1 של מחזור התא ויותר תאים חיוביים ל‑Annexin V — שניהם סימנים שהתאים עברו אפופטוזה באופן פעיל ולא רק ניזוקו.
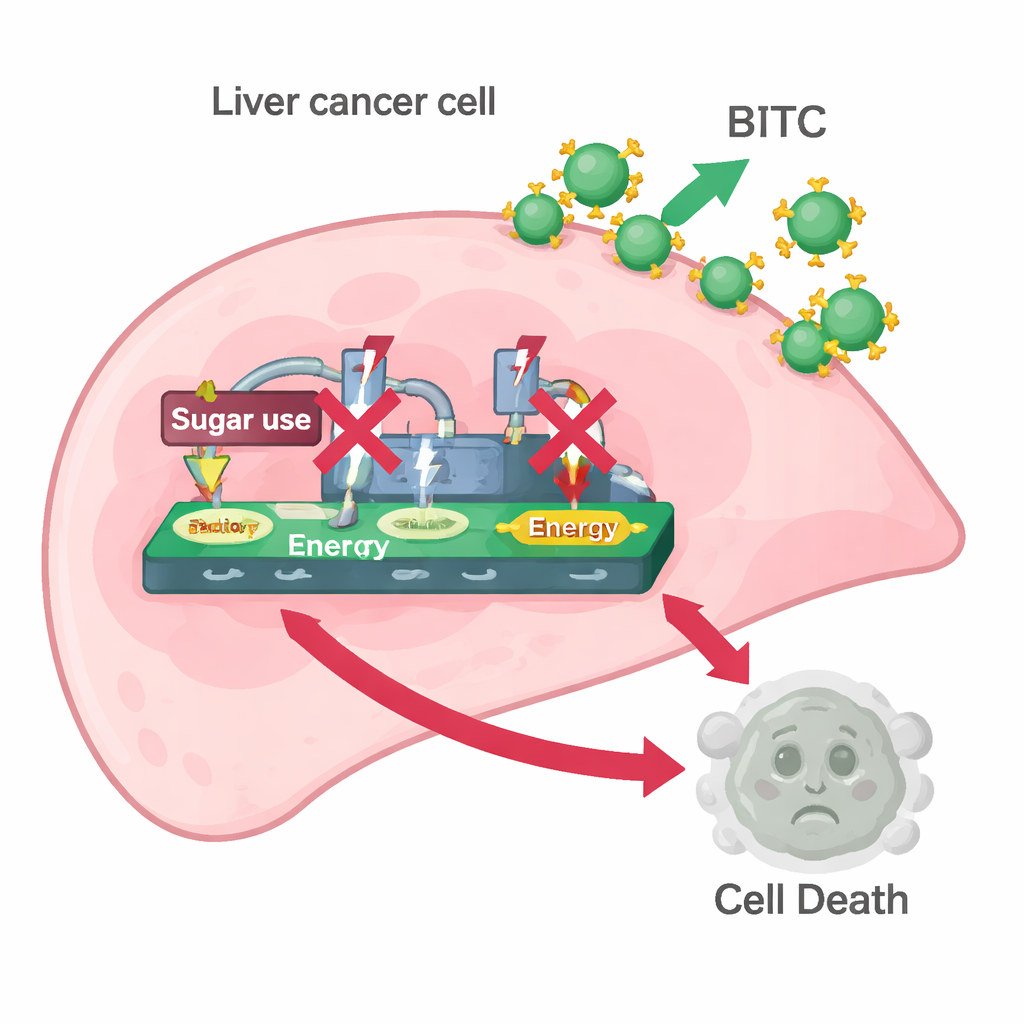
כיבוי ה״תיאבון״ של הסרטן לסוכר
הצוות חקר אז האם BITC משפיע על אפקט וורבורג. הם מדדו חלבונים המעודדים תאי סרטן לבלוע סוכר ולהפוך אותו לאנרגיה וללקטט — במיוחד HK2, PKM2 ו‑LDH. טיפול ב‑BITC הוריד את רמות כל השלושה בשתי שורות התאים והפחית את כמות הלקטט שהתאים שחררו וכמות הגלוקוז שהתאים צרכו מהמדיה. במילים אחרות, BITC הפך את תאי סרטן הכבד לפחות מסוגלים להפעיל את מערכת שריפת הסוכר במהירות גבוהה. כאשר המדענים הוסיפו פירובאט, תוצר מטבולי נמוך יותר של פירוק הסוכר שעדיין יכול להזין את המטבוליזם התאי, רבים מהאפקטים של BITC הועברו בחזרה: התאים החזירו רמות גבוהות יותר של PARP, קספאז‑3 ושל אנזימי הגליקוליזה. ההצלה הזו מרמזת שהתערבות בעיבוד הסוכר היא חלק מרכזי באופן שבו BITC מעורר מוות תאי.
פיצוח מתגי הבקרה בתוך התא
כדי להבין שכבות בקרתיות עמוקות יותר, החוקרים התמקדו בשלישיית סיגנלינג: CNOT2, c‑Myc ו‑STAT3. חלבונים אלה מסייעים בקידום גדילה, הישרדות ושינויי מטבוליזם ברבים מהגידולים. נתונים ממטופלי סרטן כבד הראו כי CNOT2 נוטה להיות גבוה יותר אצל אנשים עם תוצאות גרועות יותר. במעבדה, טיפול ב‑BITC הוריד את הצורה הפעילה המזרחנת של STAT3, את המפעיל ה־upstream שלו JAK1, את חלבון קידום הגדילה c‑Myc ואת CNOT2 עצמו. שימוש בכלים גנטיים להפחתת CNOT2 או STAT3 החזיק את אפקט ההרג של BITC חזק יותר, והפחית עוד יותר את PARP וקספאז‑3. ניסויי קשירת חלבונים גילו ש‑BITC שיבש גם את השותפויות הפיזיות בין CNOT2 ל‑STAT3 ובין CNOT2 ל‑c‑Myc. כאשר CNOT2 או c‑Myc הוגברו באופן מלאכותי, BITC איבד חלק גדול מיכולתו לכבות את אנזימי הגליקוליזה ולגרום לאפופטוזה, מה שמדגיש שמישור הסיגנלינג הזה פועל כמסטר‑סוויץ' המקשר בין מטבוליזם הסוכר וההישרדות.
מה זה עשוי להעיד על טיפולים עתידיים
במבט כולל, הממצאים מציירים תמונה קוהרנטית: BITC תוקף תאי סרטן כבד על‑ידי ניתוק קו הדלק המבוסס‑סוכר המועדף עליהם והפיכת מתגים של מוות תאי התלויים בציר CNOT2/c‑Myc/STAT3. על ידי חסימת גם אותות הגדילה וגם שימוש הסוכר, BITC דוחף את תאי הסרטן מעבר לנקודת אל־חזור מטבולית לתוך אפופטוזה. תוצאות אלה מבוססות על ניסויים בתרבית תאים, לא על מטופלים, ונחקרו רק שתי שורות של סרטן כבד, כך שנדרש עוד מחקר בבעלי חיים ובאדם. עם זאת, המחקר מחזק את הרעיון כי תרכובות מסוימות מירקות יומיומיים יכולות להיעגל או לשולב עם טיפולים אחרים כדי לרעב באופן מדויק יותר גידולי כבד תוך עידודם להרס עצמי.
ציטוט: Koh, W., Park, SY., Kim, B. et al. CNOT2 /c-Myc/STAT3 signaling is critically involved in glycolysis mediated apoptosis of benzyl isothiocyanate in hepatocellular carcinoma. Sci Rep 16, 7000 (2026). https://doi.org/10.1038/s41598-026-38416-8
מילות מפתח: סרטן הכבד, בנזיל איזותיוציאנט, מטבוליזם של סרטן, אפופטוזה, ירקות מהמשפחת המצליבים