Clear Sky Science · he
מודל פרוגנוסטי מבוסס למידת מכונה לגנים הקשורים ל"שִׁרש־דמוּת" ולאנגיוגנזה לחיזוי פרוגנוזה והחדרת חיסון בחולי HCC
מדוע המחקר הזה חשוב לחולי סרטן כבד
סרקומה המהווה את הצורה השכיחה ביותר של סרטן הכבד נוטה לשוב או להתפשט גם לאחר טיפול. מחקר זה בוחן מדוע זה קורה וכיצד ניתן לשפר את היכולת לחזות אילו מטופלים נמצאים בסיכון הגבוה ביותר. על‑ידי שילוב מאגרי נתונים גנטיים גדולים עם כלים מודרניים של למידת מכונה, בנו החוקרים כלי שמקשר שני תכונות מרכזיות של סרטן — "שִׁרש‑דמוּת" (תאים שמתנהגים כזרעים עקשניים) וצמיחת כלי דם חדשים — עם סיכויי ההישרדות של המטופלים והסבירות לתגובה לטיפולים מבוססי חיסון.
"תאי זרע" סרטניים וכלי דם חדשים
ברבים מן הגידולים קיימת קבוצה קטנה של תאים שמתנהגים כזרעים. תאי גזע סרטניים אלה יכולים להתחדש, להיות עמידים לטיפול ולהפעיל מחדש את הגידול לאחר ניתוח או כימותרפיה. במקביל, גידולים צריכים לבנות כלי דם חדשים כדי להביא חמצן וחומרי תזונה שיאפשרו להם לגדול ולהתפשט. עבודות עדכניות מראות ששני התהליכים האלה קשורים זה בזה: תאים בעלי מאפיינים שִׁרש‑דמיים משחררים אותות שמעודדים אנגיוגנזה, וסביבת כלי הדם העשירה תורמת להישרדות אותם תאים. הבנת שיתוף הפעולה הזה וכיווני מטרה משותפים חשובה במיוחד בסרטן הכבד, שהוא מאוד ועיר מבחינת כלי דם ורגיש לשיעורי חזרה גבוהים.
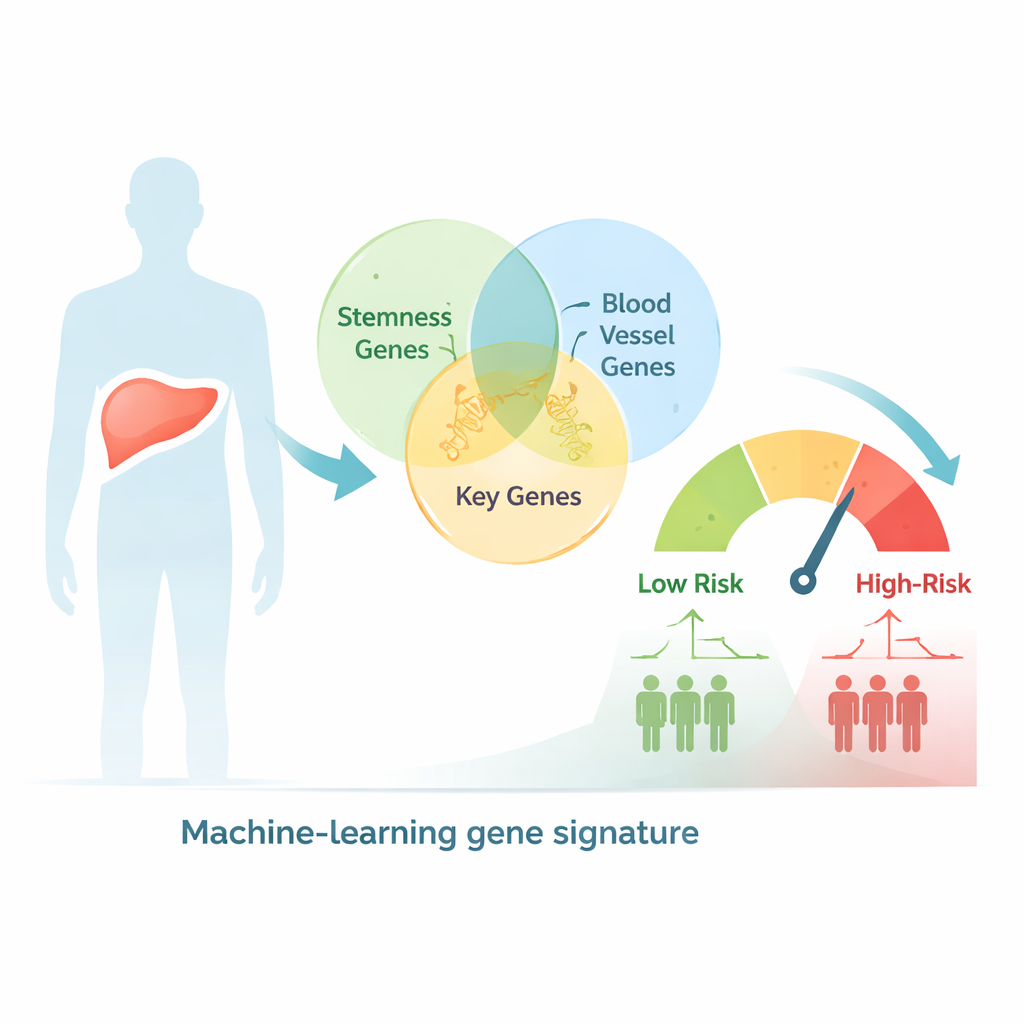
שימוש בנתונים רחבי היקף למיון מטופלים לפי סיכון
תחילה חיפשו החוקרים במאגר גנים אנושי גדול גנים המקושרים הן להתנהגות שִׁרש‑דמית והן להיווצרות כלי דם, ומצאו למעלה מ‑2,600 מועמדים חופפים. לאחר מכן בדקו דגימות סרטן כבד ממאות מטופלים שלפעילות הגנים בגידוליהם ותוצאותיהם הקליניות נרשמו בבסיסי נתונים ציבוריים. באמצעות מבחנים סטטיסטיים ושיטות אשכולות קיבצו את המטופלים לשני תת‑סוגים גנטיים שהראו הבדלים ברורים בשלבי המחלה, בגודל הגידול ובהישרדות, מה שמרמז שהאותות המשולבים של שִׁרש‑דמיות ואנגיוגנזה משקפים ביולוגיה משמעותית במחלה זו.
בניית ציון סיכון בת תשעה גנים
מקבוצת הגנים הרחבה הזו השתמשה הקבוצה בגישת למידת מכונה לצמצום לתשעה גנים מרכזיים בלבד, שפעילותם המשולבת חזו בצורה הטובה ביותר את אורך החיים של המטופלים. תשעה גנים אלה שימשו לחישוב ציון סיכון לכל מטופל. מטופלים עם ציון גבוה הציגו הישרדות כוללת משמעותית קצרה יותר, הן במאגר הנתונים המקורי והן בקבוצת אימות עצמאית של חולי סרטן כבד. הדיוק של המודל התחרה או עלה על כלים קיימים רבים, וכאשר הציון שולב עם מידע קליני פשוט כגון שלב הגידול בתרשים הנומוגרמה, החיזוי להישרדות של שנה, שלוש שנים וחמש שנים השתפר עוד יותר.
קשרים למערכת החיסון ולתגובה לטיפול
החוקרים גם בדקו מה מגלה ציון התשעה‑גנים על סביבה חיסונית של הגידול. גידולים בסיכון נמוך נטו להיות "מודלקים" יותר, עם רמות גבוהות יותר של תאי חיסון שונים ואותות חזקים יותר של מסלולי התקפה. לעומת זאת, גידולים בסיכון גבוה הראו דפוסים התואמים התחמקות חיסונית ושיעורי מוטציה גבוהים יותר בגנים חשובים כגון TP53. באמצעות כלים ממוחשבים מבוססים שמעריכים איך גידולים עשויים להגיב לתרופות אימונותרפיות מודרניות, המחקר רמז שמטופלים בסיכון נמוך עשויים להגיב טוב יותר לחסמי נקודות בדיקה חיסוניות מאשר מטופלים בסיכון גבוה. אמנם תחזיות אלה עדיין צריכות להיבדק בהקשרי טיפול אמיתיים, אך הן מצביעות על דרך מעשית לזיהוי מטופלים שעשויים להפיק את התועלת הרבה ביותר מתרופות כאלה.
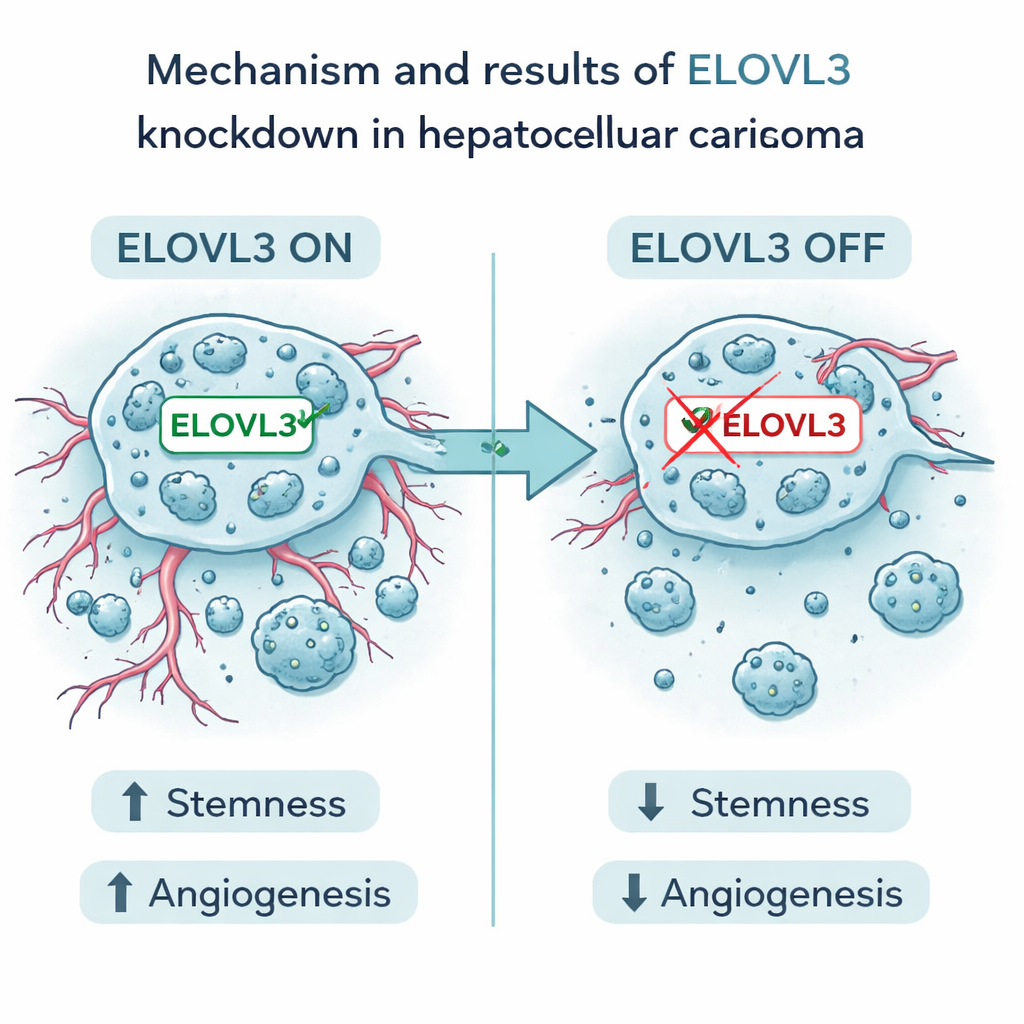
מיקוד בגורם מבטיח אחד
מתוך תשעת הגנים בלט גן אחד בשם ELOVL3. רמות גבוהות של גן זה נקשרו להישרדות גרועה יותר. בניסויים במעבדה הפחיתו החוקרים את ביטוי ELOVL3 בתאי סרטן כבד אנושיים. הדבר הפחית את יכולת התאים ליצור אשכולות בעלי מאפיינים שִׁרש‑דמיים והפחית את רמותם של סמני שִׁרשנות ידועים. בנוסף, ירדה הייצור וההפרשה של שני גורמים עיקריים המעודדים כלי דם, VEGFA ו‑FGF2. תאי הסרטן גדלו, נדדו וחדרו פחות, ובמודלים בעכברים היו הגידולים עם ELOVL3 מופחת קטנים יותר והציגו פחות תכונות של מחלה אגרסיבית. ממצאים אלה תומכים ברעיון ש‑ELOVL3 מסייע להניע הן את התנהגות ה"זרע" של תאי סרטן הכבד והן את יכולתם לבנות כלי דם תומכים.
מה משמעות הדבר לטיפול עתידי
במילים פשוטות, עבודה זו מספקת שני מסרים מרכזיים. ראשית, ציון פשוט המבוסס על תשעה גנים המופק מדגימות הגידול יכול למיין מטופלים עם סרטן כבד לקבוצות סיכון גבוהות ונמוכות ולהצביע על האופן שבו הם עשויים להגיב לטיפולים מבוססי חיסון. שנית, אחד הגנים בציון הזה, ELOVL3, נראה כעומד בצומת בין יכולת הסרטון להתחדש לבין יכולתו לגרום לצמיחת כלי דם חדשים, מה שהופך אותו למטרה תרופתית מבטיחה לעתיד. אף על פי שהמודל והמטרה צריכים אישור בניסויים קליניים פרוספקטיביים, הם פותחים דלת לטיפול מותאם אישית בסרטן הכבד ולאסטרטגיות משולבות החוסמות הן את "תאי הזרע" והן את אספקת הדם שלהם.
ציטוט: Cheng, F., Shi, Y., Gao, X. et al. Machine learning-based prognostic model of stemness and angiogenesis-related genes for predicting prognosis and immune infiltration in patients with HCC. Sci Rep 16, 7271 (2026). https://doi.org/10.1038/s41598-026-38379-w
מילות מפתח: סרקומה הכבד ההפטוצלולרית, תאי גזע סרטניים, אנגיוגנזה, חתימת גנים פרוגנוסטית, ELOVL3