Clear Sky Science · he
אובינוטוזומאב גורם לחוסר יציבות של הליזוזום באמצעות עיכוב תלוּי ספינגומיאלין של TRPML2
מדוע הסיפור של הנוגדן הזה חשוב
בעבור רבים החולים בלימפומות תאי B, תרופות נוגדנים מודרניות הפכו אבחנה שהייתה פעם קטלנית באופן אחיד למצב שניתן לטיפול. עם זאת לא כל הנוגדנים זהים: חלקם הורגים תאי סרטן בעוצמה ובמהימנות רבה יותר מאחרים. מאמר זה חוקר מדוע תרופה אחת כזו, אובינוטוזומאב, טובה יותר בהרג ישיר של תאי לימפומה מאשר קודמתה ריטוקסימב, על‑ידי התמקדות בפושע בלתי צפוי עמוק בתוך התא — מרכזי המיון והמחזור של התא, הליזוזומים, ובאיזון העדין של שומנים ותעלות יונים בממברנותיהם.
מטרה על המשטח להתאבדות פנימית
גם ריטוקסימב וגם אובינוטוזומאב מזהים את אותה מטרה על תאי B, חלבון בשם CD20. אבל החוקרים מראים שאובינוטוזומאב נלקח אל תוך התא מהר יותר ויעיל יותר. לאחר שהנוגדן נקשר ל‑CD20 על פני תא הסרטן, קומפלקסי הנוגדן‑קולטן נבלעים פנימה בתהליך אנדוציטי ומועברים למחלקות חומציות, כולל ליזוזומים. שם, אובינוטוזומאב גורם לפרמביליזציה של ממברנת הליזוזום: ממברנת הליזוזום, שלרוב חזקה, נעשית דליפה, ומאפשרת לאנזימי עיכול כמו קטפסינים לצאת ולדרבן מסלולי מוות תאיים. שינויים במאזן המלח והמים של מחלקות אלה, הגורמים לנפיחות הליזוזומים, הוכחו כמגבירים במידה רבה את האפקט ההורג הזה.
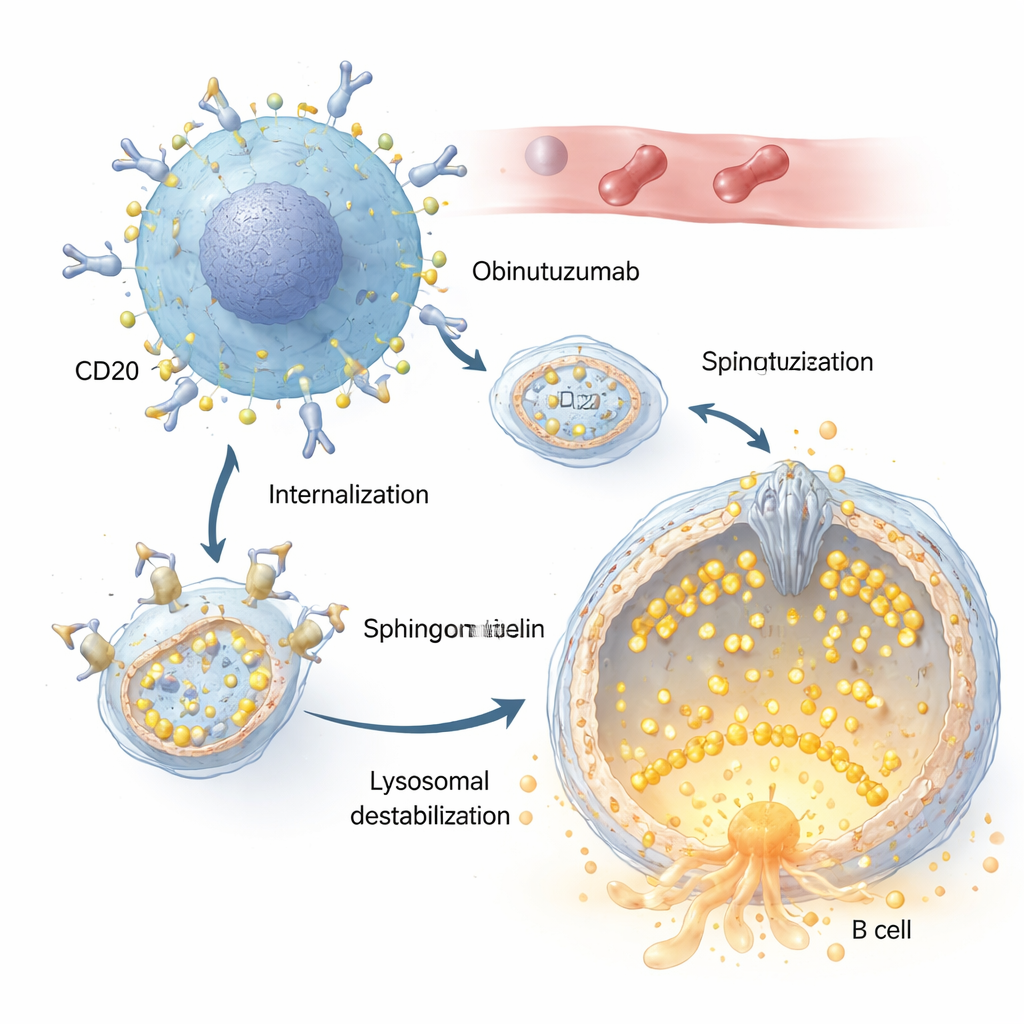
התפקיד של שער קטן
מרכזי בסיפור זה הוא TRPML2, תעלת סידן המוטמנת בממברנת הליזוזום. בתנאים רגילים, TRPML2 מסייעת לליזוזומים להתמודד עם מתח מכני ואוסמוטי על‑ידי שחרור סידן, המאפשר תיקון ממברנה, תנועתיות ושליטה בנפח. באמצעות שילוב של צבעי סידן זוהרים וגרסאות מהונדסות של TRPML2 החושפות סידן, החוקרים מציגים שאובינוטוזומאב סוגרת במהירות את התעלה הזאת: בתוך דקות מהטיפול, תרופה שבאופן רגיל פותחת תעלות TRPML כבר לא מייצרת פרץ סידן. גישות גנטיות שמפחיתות את רמות TRPML2, או מולקולות קטנות שמעכבות את פעילות TRPML, מגדילות את הרגישות של תאי הלימפומה לאובינוטוזומאב, ומובילות ליותר דליפה ליזוזומלית ולשיעורי מוות ישיר גבוהים יותר.
כיצד שומני הממברנה מזיזים את המאזן
בהמשך המחקר בודק מה מקשר בין קליטת הנוגדן לסגירת התעלה. תשומת הלב מופנית לספינגומיאלין, ליפיד (שומן) השכיח בממברנות תאים וידוע כמפריע לתעלות TRPML. באמצעות זיהוי פלואורסנטי הקושר ספינגומיאלין, המחברים מגלים שוויקולות המכילות אובינוטוזומאב עשירות בספינגומיאלין כאשר הן מגיעות למחלקות חומציות, הרבה יותר מאשר וויקולות שמכילות ריטוקסימב. כאשר מטפלים בתאים בספינגומיאלינאז, אנזים שמקצץ ספינגומיאלין, פעילות שחרור הסידן של TRPML2 משוחזרת אפילו בנוכחות אובינוטוזומאב. בתנאים אלה, הליזוזומים נוטים פחות לדלוף ומתוּי פחות תאים מתים, מה שמרמז בחוזקה שספינגומיאלין מצטבר ומנטרל את TRPML2 ומכין את הליזוזומים לקריעה.
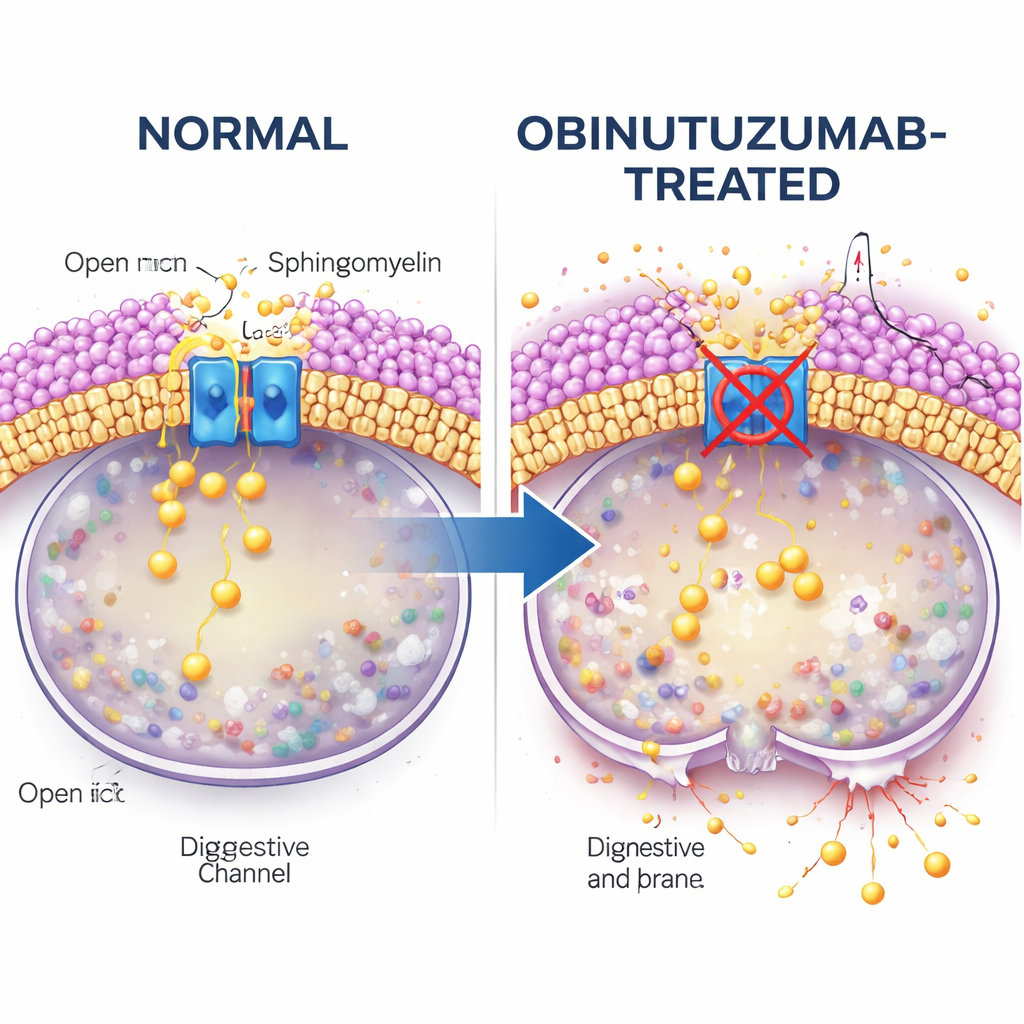
נתיבי תנועה וצמתים של כולסטרול
הנתיב שאובינוטוזומאב עובר אל תוך התא גם הוא משמעותי. מיקרוסקופ אלקטרוני וסימון נוגדנים רגיש ל‑pH מגלים שאובינוטוזומאב עוזב את פני התא ונכנס לוויקולות תוך‑תאיות מהר יותר מריטוקסימב. כאשר החוקרים מתערבים בנתיבי קליטה ספציפיים, הם מגלים שחסימת צורה של אנדוציטוזה התלויה בכולסטרול (עם תרכובת בשם פיליפין) מונעת מאובינוטוזומאב לכבות את TRPML2, ומפחיתה באופן חלקי את נזקי הליזוזום ואת מוות התא. מעכבים אחרים של אנדוציטוזה אינם מפגינים אפקט מגן זה. ממצאים אלה מצביעים על מסלול מיוחד, עשיר בכולסטרול ובספינגומיאלין, שמנגיש את אובינוטוזומאב לליזוזומים בצורה שמכינה את הקרקע לעיכוב TRPML2 ולהתפרקות הממברנה.
מה משמעות הדבר לטיפולים עתידיים בסרטן
פשטות הדברים: עבודה זו מראה שאובינוטוזומאב הורג לימפומות תאי B ביעילות כיוון שהוא מכניס את הליזוזומים שלהן למצב שביר. על‑ידי בחינת קומפלקסי הנוגדן‑CD20 למחלקות עשירות בספינגומיאלין, התרופה מכבה בעקיפין תעלת סידן מגן, TRPML2. ברגע שהמנגנון המגן הזה נעלם, הליזוזומים נוטים יותר להתפוצץ תחת מתח, לשפוך אנזימים קורוזיביים ולהרוס את תא הסרטן מבפנים. הבנת ציר השומן–תעלות היונים הזה אינה רק מסבירה מדוע אובינוטוזומאב עוקף את ריטוקסימב; היא גם מציעה אסטרטגיות חדשות לחזק טיפולי נוגדנים — למשל על‑ידי צמדם עם תרופות שמשנות סרינגולפידים או מגבירות פעילות TRPML2 כדי לכוונן בדיוק מתי ואיך ליזוזומי תאי הגידול יעברו התפרקות עצמית.
ציטוט: Oh, J., Jin, N., Kwon, S. et al. Obinutuzumab induces lysosomal destabilization via sphingomyelin-dependent inhibition of TRPML2. Sci Rep 16, 7079 (2026). https://doi.org/10.1038/s41598-026-38087-5
מילות מפתח: אובינוטוזומאב, לימפומת תאי B, ליזוזום, ספינגומיאלין, TRPML2