Clear Sky Science · he
תכונות פונקציונליות של וניקולות חוץ־תאיות שמקורן בסיבי שריר שלד על בסיס פרופילי microRNA: ניתוח השוואתי מול וניקולות חוץ־תאיות שמקורן בתאי גזע מזנכימליים
הודעות השריר בחבילות זעירות
השרירים שלנו עושים הרבה יותר מאשר להזיז אותנו—הם שולחים באופן קבוע "הודעות טקסט" מולקולריות ברחבי הגוף. במחקר זה נבדק כיצד חלקיקים זעירים שמשתחררים מתאים שריר משתווים לחלקיקים דומים שמקורם בתאי גזע נפוצים לשימוש טיפולי עתידי. על ידי פענוח האותות הגנטיים שהחלקיקים האלה נושאים, החוקרים שואלים שאלה מעשית: באילו סוגי מחלות עשויים חלקיקים שמקורם בשריר להיות עדיפים על אלה שמקורם בתאי גזע?
שליחים זעירים הנעים בגוף
כל התאים משחררים בועיות מיקרוסקופיות המכונות וניקולות חוץ־תאיות, או EVs. אלה חבילות בגודל נגיפי עטופות בשומן, העמוסות במטען מולקולרי. סוג מטען מרכזי הוא microRNA—קטעי RNA קצרים שעוזרים לכוון ביטוי גנים מעלה או מטה ולעצב את התנהגות התאים. שריר השלד, רקמת ההנעה של התנועה, מתגלה כארגון ההפרשה הגדול ביותר בגוף ויכול לשחרר כמויות גדולות של EVs, במיוחד כאשר מעוררים אותו באמצעים לא פולשניים כגון אולטרסאונד. לעומת זאת, תאי הגזע המזנכימליים משמשים כבר עבודה סיזיפית בניסויים קליניים, וה-EVs שלהם נחקרים לשיקום רקמות ולהרגעת דלקת.
קריאת הקוד הגנטי של המטען
במקום לבדוק EVs ישירות בחיות או בבני אדם, החוקרים ניתחו מחדש מערכי נתוני ריצוף קיימים שממפים אילו microRNA נוכחים ב-EVs שמקורם במיוטיובים של שריר שלד של עכבר (סיבים שריריים שגודלו במעבדה) וב-EVs שמקורם בתאי גזע מזנכימליים שמקורם מחיבור עצם. ל-EVs שמקורם בשריר היו כמה microRNA דומיננטיים, כגון miR-206-3p ו-miR-378a-3p, שהיוו יותר מ‑60 אחוז מהמטען שלהם, בעוד ש-EVs של תאי הגזע נשאו תמהיל מאוזן יותר, כולל את משפחת let-7 בעלת פעולה רחבה. מאחר שכל microRNA יכול להשפיע על גנים רבים והרבה microRNA יכולים להתמקד באותו מסלול, הצוות פיתח שיטות חישוביות להבנה איך פרופילים שלמים—ולא מולקולה בודדת—עשויים לעצב תוכניות תאיות.
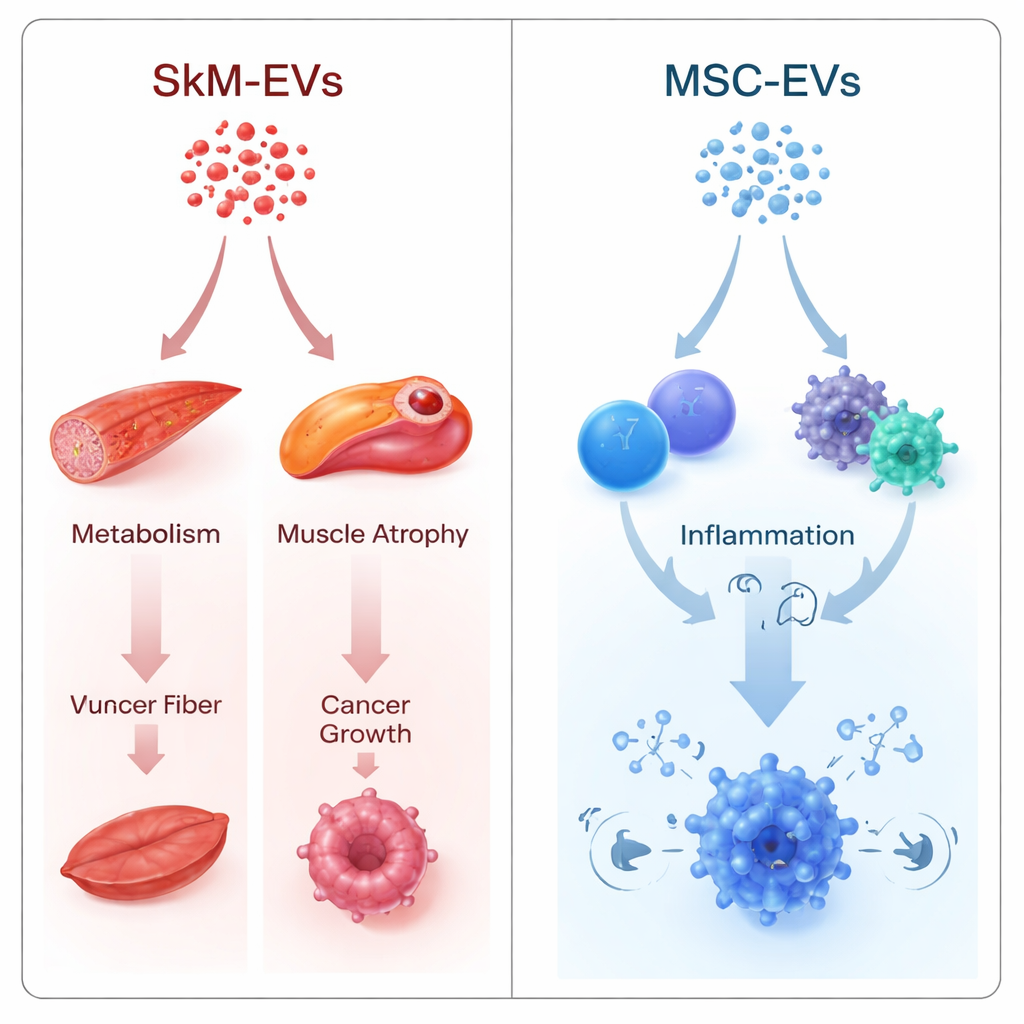
מסלולים המקושרים לשריר, מטבוליזם וסרטן
המחברים השתמשו בשתי אסטרטגיות משלימות. אחת השוותה ישירות בין EVs של שריר ושל תאי גזע, וביקשה היכן ה-microRNA שלהן שונים. השנייה טיפלה בכל סוג EV בנפרד, והפכה את פרופיל ה-microRNA שלו לציון "השפעה" ברמת הגן שמעריך עד כמה המטען עשוי לדכא מסלולים מסוימים. למרות המתמטיקה השונה, שתי הגישות הצביעו באותו כיוון. EVs שמקורם בשריר הראו נטייה חזויה לעכב מסלולים הקשורים לבילד השריר (אותות FoxO ו‑TGF-β), בקרה על סוכר בדם ואיזון אנרגיה (FoxO, mTOR, AMPK), ומסלולי גדילה סרטנית (אותות ErbB וקבוצה שסומנה כ"microRNAs בסרטן"). רבים מהמטרות המשפיעות ביותר היו רגולטורים מרכזיים של גלווקונאוגנזה בכבד, מניעים מרכזיים של ניוון שריר, וגנים מרכזיים המעודדים סרטן.
וניקולות תאי גזע ומערכת החיסון
ל-EVs של תאי הגזע הייתה תמונה שונה. המטען של ה-microRNA שלהם צפוי להשפיע חזק יותר על מסלולים קשורים למערכת החיסון: איתות NF-κB, אינטראקציות ציטוקין־קולטן, איתות בקולטני תאי B ו‑T, ודיפרנציאציה של תאי Th17. אלה מרכזיים לאופן שבו הגוף חוֹשֵׁב זיהום, מפעיל וכבה דלקת ולעצב את זהות תאי המערכת החיסונית. הנטייה הזאת תואמת עדויות ניסיוניות הולכות וגדלות שתומכות בכך ש-EVs של תאי גזע יכולים לווסת תגובות חיסוניות באופן רחב ונבדקים במצבים שבהם צמצום דלקת הוא קריטי, כגון מחלות אוטואימוניות ודלקתיות.
מתחזיות מחשב לטיפולים עתידיים
בסך הכל, העבודה מצביעה על כך ש‑EVs שמקורם בשריר עשויים להיות מיועדים מטבעם למצבים שמעורבים בבליה של שריר, מטבוליזם מוטה או גדילה בלתי מבוקרת של תאים, בעוד ש‑EVs של תאי גזע עשויים להתאים יותר למחלות המונחות על ידי ליקויים בתפקוד המערכת החיסונית. הממצאים מבוססים כולו על ניתוח חישובי של נתונים קיימים ואינם מוכיחים עדיין תועלת בחולים, וכן אינם לוקחים בחשבון מטענים אחרים של EVs כגון חלבונים או ליפידים. עם זאת, על ידי הפיכת פרופילי microRNA מורכבים ל"טביעות אצבע" ברמת מסלולים, המחקר מציע מפת דרכים להתאמת מקורות EV לסוגי מחלה ועוזר לתת עדיפות לשילובים שהכי מבטיחים לבדיקה במעבדה ולבסוף, בקליניקה.
ציטוט: Kawamoto, Y., Yamaguchi, A., Ma, X. et al. Functional properties of skeletal myotube-derived extracellular vesicles based on microRNA profiles: a comparative analysis with mesenchymal stem cell-derived extracellular vesicles. Sci Rep 16, 7436 (2026). https://doi.org/10.1038/s41598-026-38076-8
מילות מפתח: וניקולות חוץ־תאיות, שריר שלד, microRNA, תאי גזע מזנכימליים, מסלולי איתות תאית