Clear Sky Science · he
ייצור תאי T מסוג TCRγδ מהתאים העובריים האנושיים
דרכים חדשות לצייד את המערכת החיסונית
טיפולי סרטן נעזרים יותר ויותר במערכת החיסון של הגוף כדי לאתר ולהשמיד גידולים. סוג תאי חיסון מבטיח במיוחד, המכונה תאי גמא‑דלתא (gamma‑delta), מסוגל להרוג תאי סרטן מבלי להצריך זיהוי מדויק של סוג הרקמה של המטופל—מה שהופך אותו למועמד חזק לטיפולים "מוכנים לשימוש". עם זאת, תאים אלה נדירים בדם של מבוגרים, והתרבותם בכמויות גדולות קשה. המחקר הזה מתאר שיטה לגדל תאי גמא‑דלתא במעבדה, החל מתאים עובריים אנושיים, ופותח אפיק לתרופות אימונו‑תרפויטיות נגישות יותר.
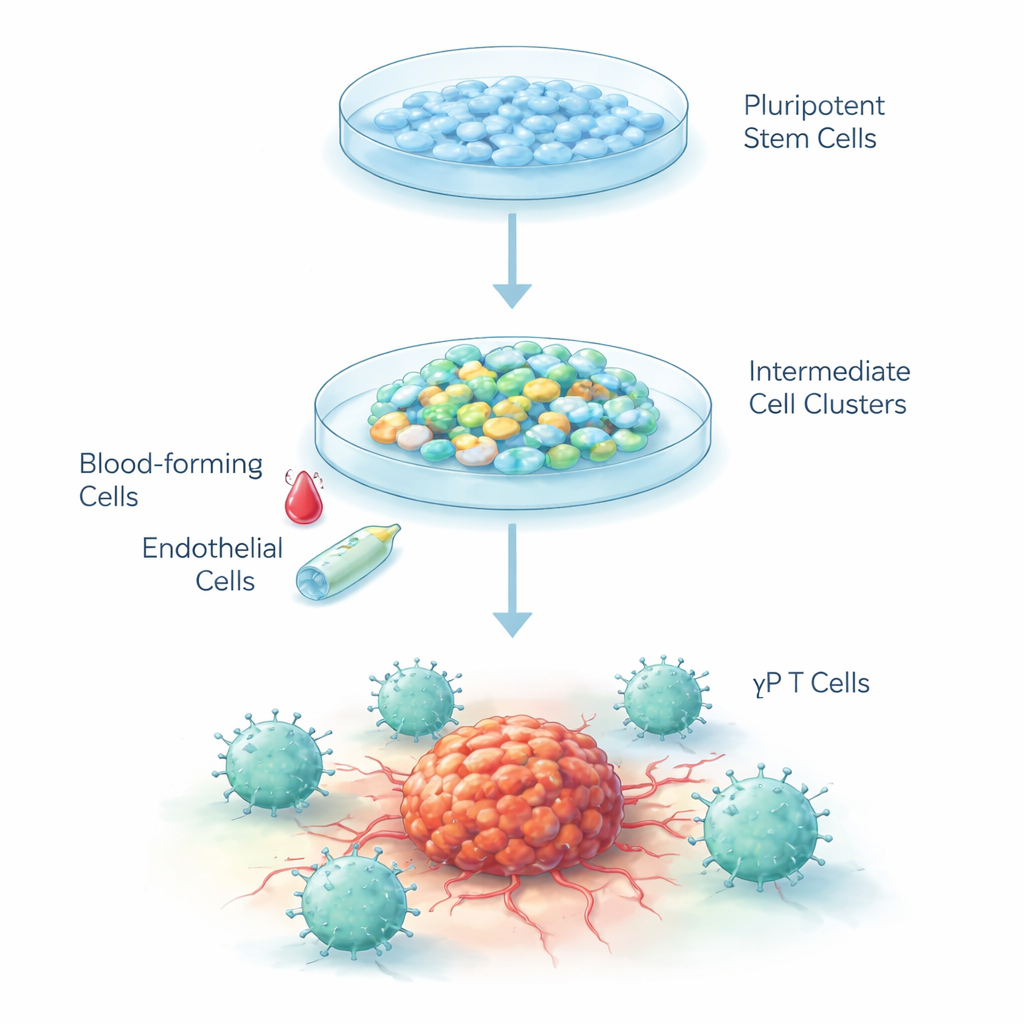
לשנות תאים 'לוח חלק' ללוחמים נגד סרטן
תאים עובריים אנושיים הם תאים "לוח חלק" שיכולים, בעקרון, להפוך כמעט לכל רקמה בגוף. החוקרים תכננו מתכון שלב‑אחר‑שלב כדי להנחות את התאים להתפתח לאורך אותו מסלול שהם עוברים בעובר כאשר מערכת הדם והחיסון נוצרת לראשונה. השתמשו בתהליך בעל שלושה שלבים: ראשית הובלת התאים לעבר תאים דמויי‑כלי דם מוקדמים, לאחר מכן להמפסקים לא-בשלים של יצירת דם, ולבסוף לתאי T מסוג גמא‑דלתא. התאים גודלו במבנים תלת‑ממדיים בתמיסה מיוחדת בתנאי חמצן נמוכים המדמים את העובר המתפתח, ולאחר מכן הוחזרו לרמות חמצן רגילות כשהם התבגרו.
בניית קו ההרכבה של תאי החיסון
בשלב הראשון אותות כימיים דחפו את התאים העובריים להפוך למזודרם, השכבה המוקדמת שממנה מתפתחים הדם וכלי הדם. בתוך שישה ימים, כמעט 40% מהתאים בכל אשכול הראו סימני "תאי אנדותל המטופואטיים" — סוג של תא מעבר שיכול לתת מקור לתאי דם. בשלב השני, שינוי גורמי הגדילה עורר תאים אלה לבצע מעבר לתאי אבות דם צפים חופשית. למעלה מ‑99% מתאים צפים אלה נשאו סימן מוקדם מרכזי של דם, וכ‑כ‑90% הביעו סימן נוסף של תאי דם, מה שמעיד על אוכלוסייה טהורה מאוד עם פוטנציאל חזק להמשיך בדרך התפתחות לתאי חיסון.
הגעה לתאי גמא‑דלתא
לשלב הסופי סיפקה הקבוצה אותות הידועים כמעודדים התפתחות תאי T, כולל חלבון מפעיל Notch המדמה רמזים הנמצאים בדרך כלל בית השד (התימוס). לאחר 25 יום, יותר מ‑40% מהתאים התבגרו לתאי גמא‑דלתא, שנזהו על ידי קולטני השטח המאפיינים שלהם ופרופיל "כפול‑שלילי" (חסרי התוויות CD4 ו‑CD8 הרגילות שנמצאות ברוב תאי T אחרים). באופן חשוב, יוצרו מעט מאוד תאי T קונבנציונליים מסוג אלפא‑בטא, מה שמראה שהפרוטוקול מעדיף באופן משמעותי את הענף של גמא‑דלתא. ניתוח גנטי לאורך זמן הראה שהתאים הפעילו וכיבו קבוצות גנים בסדר מאורגן שמשקף במדויק את הדרך שבה הדם ותאי ה‑T נוצרים בתוך הגוף.
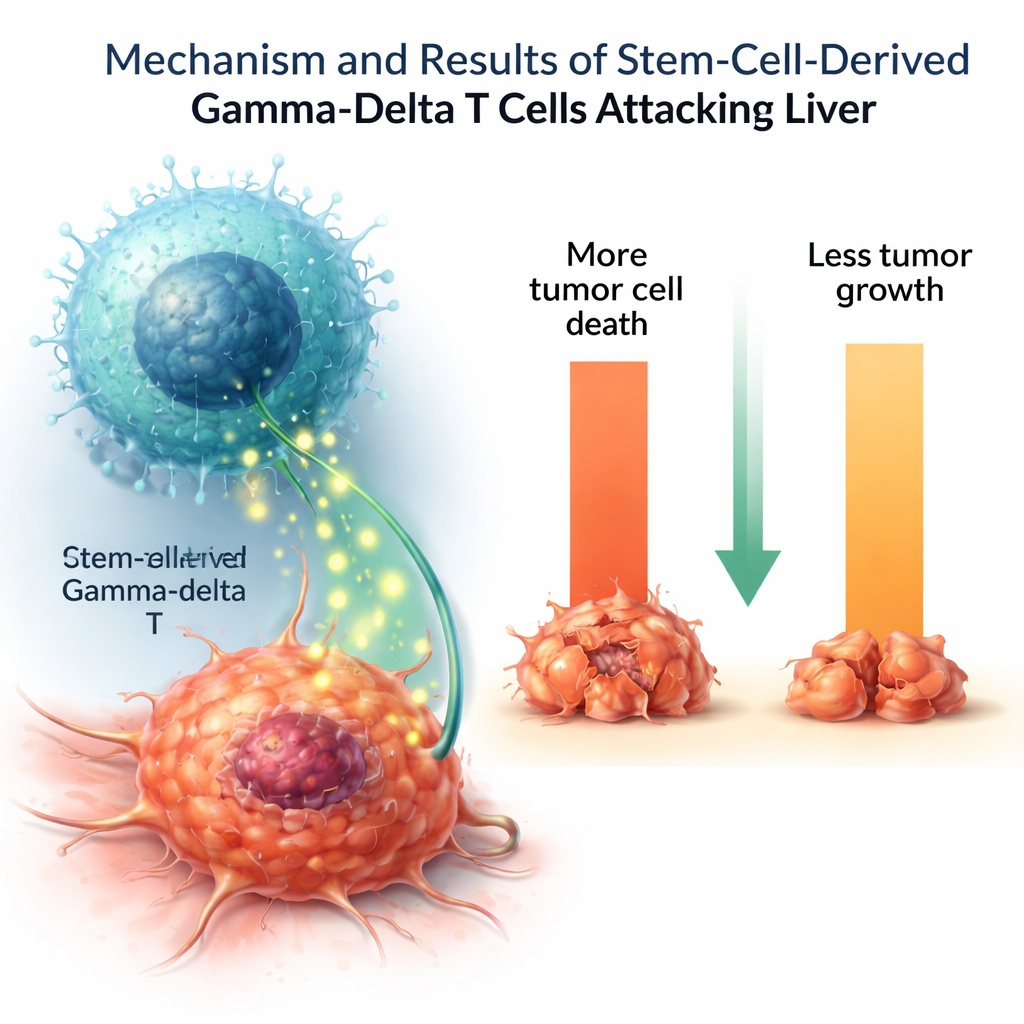
בחינת התאים שגודלו במעבדה
כדי לבדוק האם התאים המיוצרים במעבדה מתפקדים כלוחמי סרטן אמיתיים, החוקרים חשפו אותם למספר שורות תאי גידול אנושיות. תאי הגמא‑דלתא הרגו חלק ניכר מתאים של תאי סרטן כבד והאטו את גדילתם, בעוד שהשפעתם על תאים בריאים ביקורתיים הייתה מועטה. כאשר גודרו, הם הפרישו מולקולות שליח חשובות במערכת החיסון כגון פקטור נמק גידולים (TNF) ואינטרלוקין‑2, המסייעות לתאם ולהעצים מתקפות חיסוניות. חלק ממולקולות ההרג היו ברמות נמוכות יותר מאשר בתאי גמא‑דלתא טבעיים, מה שמרמז שהתאים שגודלו במעבדה עשויים לא להיות בשלים לחלוטין או לייצג תת‑סוג תפקודי מסוים.
מה זה יכול להביא לטיפול בסרטן בעתיד
על‑ידי שימור גרסה מוקטנת של התפתחות דם מוקדמת בצלחת—בלי שימוש בתאים מזינים מן החי—המדענים ייצרו כמויות גדולות של תאי גמא‑דלתא פחות מחודש, מהר ופשוט יותר משיטות קודמות. אמנם דרוש עוד עבודה לטיהור תערובת התאים הסופית, להגדלת הייצור ולהתאמת המתכון לתנאים מאושרים קלינית וללא סרום, הגישה הזו מצביעה על מקור מתחדש של תאי גמא‑דלתא סטנדרטיים. אם תאים אלה יוכחו כבטוחים ויעילים בבדיקות נוספות, הם עשויים להפוך לחלק זמין ונפוץ בארסנל של אימונותרפיות "מוכנות לשימוש" בדור הבא נגד סרטן, כולל גידולי כבד.
ציטוט: Zhang, X., Chen, C., Fu, Y. et al. Generation of TCRγδ + T cells from human embryonic stem cells. Sci Rep 16, 6762 (2026). https://doi.org/10.1038/s41598-026-37941-w
מילות מפתח: תאי גמא-דלתא, אימונותרפיה נגד סרטן, תאים עובריים אנושיים, הבחנה תאית, סרטן כבד