Clear Sky Science · he
אינטרלוקין‑7 מעורר EMT לקידום גדילת גידול ומטסטזות בסרטן ריאה שאינו תאי קטן דרך מסלול Notch1/TGF‑β
מדוע חלבון איתות חשוב בסרטן הריאה
סרטן הריאה נשאר אחד מסוגי הסרטן הקטלניים ביותר בעולם, בעיקר משום שהוא לעתים קרובות מתגלה לאחר שכבר התפשט. המחקר הזה מתמקד בשליח חיסוני טבעי, אינטרלוקין‑7 (IL‑7), ושואל שאלה חשובה: בסרטן ריאה שאינו תאי קטן (NSCLC), האם IL‑7 מסייע לגוף להילחם בגידול, או שמא הוא מסייע לגידול לגדול ולהתפשט? על‑ידי מעקב אחרי האופן שבו IL‑7 משפיע על תאי סרטן ריאה במטופלים, בתרביות תאים ובחיות מעבדה, החוקרים חושפים מסלול שנראה שדוחף את הגידולים לכיוון גדילה מוגברת, התפשטות ועמידות לטיפול.
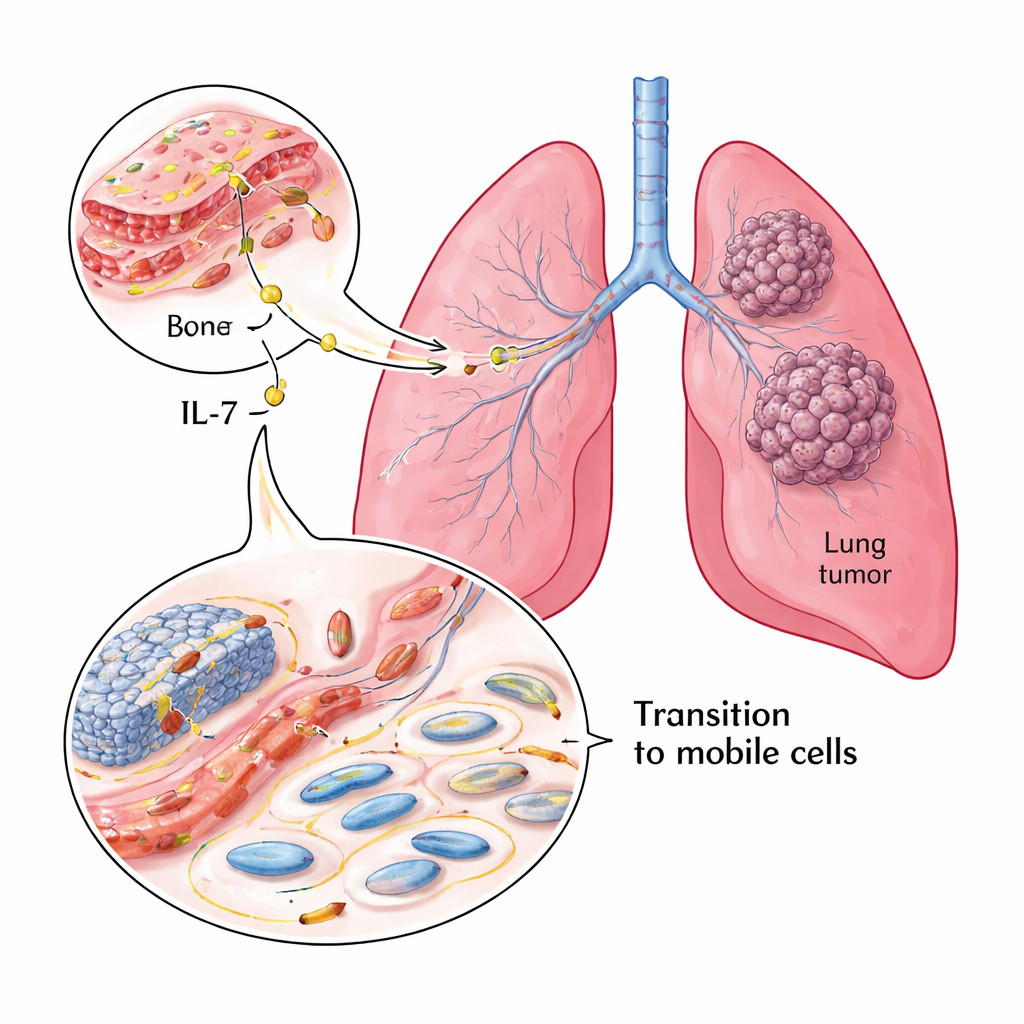
מבט מקרוב על גידולי ריאה ותוצאי מטופלים
הצוות החל בבחינת דגימות גידול מ‑119 מטופלים עם NSCLC. באמצעות שיטות צביעה על רקמות משומרות, הם מדדו את רמות IL‑7, קולטן ה‑IL‑7 (IL‑7R) ושני סמנים מרכזיים המתארים עד כמה תאי הסרטן "עוגנים" או ניידים. E‑cadherin מקושר לתאים מחוברים הדוק פחות ניידים, בעוד Vimentin מקושר לתאים גמישים ובולטים פולשניים יותר. ברוב הגידולים נצפו רמות גבוהות של IL‑7 ו‑IL‑7R. כאשר IL‑7 ו‑IL‑7R היו בשפע, E‑cadherin נטה להיות נמוכה ו‑Vimentin גבוהה — דפוס לא רצוי. מטופלים שלגידוליהם היה יותר E‑cadherin חיו זמן רב יותר, בעוד אלה עם IL‑7R גבוה הפגינו הישרדות גרועה יותר, מה שעושה את IL‑7R למנבא חזק של התוצאה.
כיצד תאי סרטן עוברים מלהישאר במקום לפרידה
כדי לצאת מהקהלת הקורלציה, החוקרים בדקו כיצד IL‑7 משפיע ישירות על תאי סרטן ריאה בגידול במעבדה. כאשר שתי שורות תאי NSCLC נחשפו ל‑IL‑7, התאים השתנו ממראה קומפקטי ודמוי פסיפס לצורה מוארכת ובעלת יכולת תנועה חופשית יותר. בתוך התאים חלו שינויים ברמות החלבונים בהתאמה: E‑cadherin ירד, בעוד סמני "תאים ניידים" כמו N‑cadherin, Vimentin ו‑Snail1 עלו. שלד האקטין של התאים, המסייע להם לזחול, גם הוא הפך בולט יותר ויצר שלוחות. חסימת קולטן ה‑IL‑7 הפכה את ההשפעות האלה, מה שמעיד ש‑IL‑7 מוביל את תהליך שינוי הצורה הזה — הנקרא מעבר אפיתל‑למזנכימלי (EMT) — דרך הקולטן שלו על תאי סרטן הריאה.
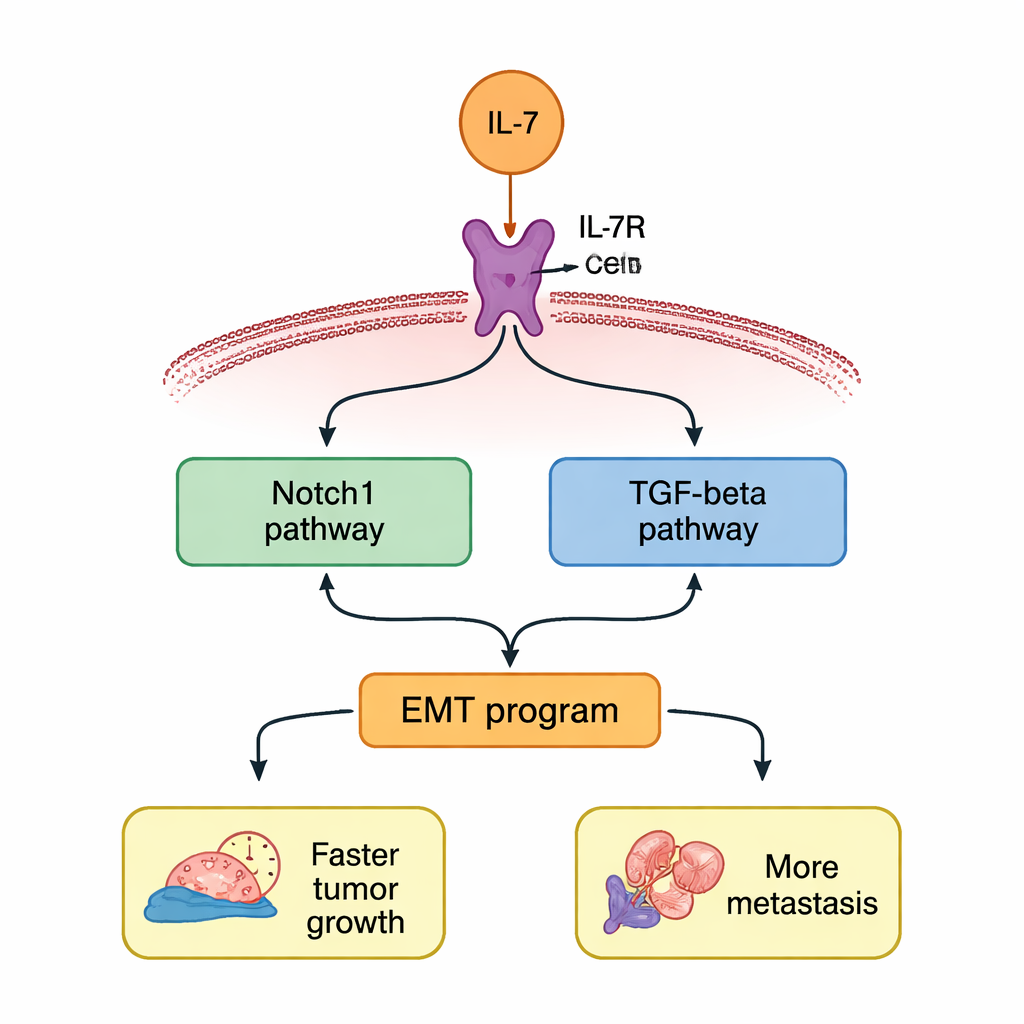
שני מסלולים מקושרים שמעצימים את הסכנה
לאחר מכן המחקר שאל כיצד IL‑7 מעביר את ההוראות הללו בתוך התא. המחברים התמקדו בשני מסלולי איתות ידועים, הפעילים לעתים קרובות בסרטנים אגרסיביים: Notch1 ו‑TGF‑β. לאחר טיפול ב‑IL‑7, גם Notch1 וגם TGF‑β עלו ברמות הגן והחלבון בתאי סרטן הריאה. אם החוקרים חסמו את IL‑7R, עליות אלה נעלמו. כאשר השתמשו בתרופות ספציפיות לעיכוב Notch1 או TGF‑β, שני המסלולים שקטו יחד, מה שמרמז על לולאת משוב חיובית שבה כל מסלול תומך בשימור השני. חיתוך של כל אחד מהמסלולים השתק חלקית את תכנית ה‑EMT והפחית את ההגברה ש‑IL‑7 יצר בצמיחה, הנדידה והחדירה של התאים.
מצלחת פטרי אל ריאות חיות
כדי לבדוק האם הממצאים במעבדה מתקיימים גם ביונקים חיים, הצוות פנה למודלים של עכברים. בקבוצת ניסויים אחת, תאי סרטן ריאה הושתלו מתחת לעור. עכברים שקיבלו IL‑7 פיתחו גידולים גדולים וכבדים יותר מאשר קבוצת הביקורת. רקמת הגידול של בעלי החיים הללו הראתה E‑cadherin נמוכה יותר, Vimentin ו‑Snail1 גבוהים יותר, ופעילות מוגברת של Notch1 ו‑TGF‑β. כאשר העכברים קיבלו גם מעכבים של Notch1 או TGF‑β, גדילת הגידול וסמנים אגרסיביים אלה הופחתו באופן משמעותי. במודל שני, תאי סרטן הוזרקו לדם דרך וריד הזנב. כאן, בעכברים שטופלו ב‑IL‑7 נצפו יותר מטסטזות ריאה ומשקל ריאות גבוה יותר, בעוד שתרופות החוסמות את המסלולים שוב צמצמו את ההתפשטות.
מה משמעות זאת לטיפול העתידי בסרטן ריאה
בסיכום, המחקר מצייר את IL‑7 לא כסייע חיסוני חד־משמעי, אלא ככלי דו‑להבי ב‑NSCLC. בסביבה זו נראה כי IL‑7 דוחף תאי גידול לשחרר את הקשרים שלהם, לאמץ זהות ניידת יותר ולנדוד לאתרים חדשים, וכולו דרך רשת מחזקת שממוקדת סביב מסלולי Notch1 ו‑TGF‑β. עבור מטופלים, ממצאים אלה מרמזים כי IL‑7R גבוה בגידולים עלול להעיד על פרוגנוזה גרועה וכי טיפולים שעוצבו בקפידה המיועדים ל‑IL‑7/IL‑7R או לנתיבים המושרשים ממנו עשויים לעזור להאט את גדילת הגידול והמטסטזות. אף שעדיין נדרש מחקר נוסף למיפוי הקישורים המולקולריים המדויקים ולבדיקת הבטיחות בבני‑אדם, המחקר מדגיש סט חדש ומבטיח של מנופים לשינוי המאזן נגד סרטן הריאה.
ציטוט: Shao, Y., Cheng, H., Ni, W. et al. Interleukin-7 induces EMT to promote tumor growth and metastasis in NSCLC via Notch1/TGF-β pathway. Sci Rep 16, 7326 (2026). https://doi.org/10.1038/s41598-026-37876-2
מילות מפתח: סרטן ריאה שאינו תאי קטן, אינטרלוקין‑7, מעבר אפיתל־מזנכימלי, מסלול Notch1, אותות TGF‑beta