Clear Sky Science · he
אסטרטגיות חישוביות לחשיפת תובנות ממעכבים ידועים להמשך אופטימיזציית עופרת: מחקר מקרה על אנלוגים של סלקוקסיב
מדוע שינויים זעירים בכדורי כאב חשובים
משככי הכאבים המודרניים לא רק מטשטשים כאבים; הם מחדירים שינויים מדויקים בכימיה של הגוף. סלקוקסיב, תרופה אנטי‑דלקתית נפוצה, מתמקדת באנזים המעורב בכאב ונפיחות תוך שמירה יחסית על אנזים קרוב המגן על הקיבה. יחד עם זאת, עשרות קרובים כימיים של סלקוקסיב מפגינים התנהגות שונה מאוד בגוף. המחקר הזה משתמש במודלינג ממוחשב כדי לשאול שאלה שמסתתרת מאחוריה פשטות מטעה בעלת השלכות גדולות על תרופות בטוחות יותר: עד כמה משנה אטום אחד קטן במולקולה?
האנזים שמפעיל את תחושת הכאב
כאשר רקמה ניזוקה או מדוללת, הגוף משחרר מולקולה שומנית בשם חומצה ארכידונית. אנזים בשם COX‑2 ממיר את המולקולה הזו לפרוסטגלנדינים, שמפעילים כאב, חום ונפיחות. אנזים קשור, COX‑1, עוזר להגן על רירית הקיבה ועל טסיות הדם. משככי כאבים ישנים כמו איבופרופן משפיעים על שני האנזימים, מקלים על הכאב אך לעתים קרובות מגרדים את הקיבה. סלקוקסיב עוצב להיכנס לכיס מעט גדול יותר שנמצא בעיקר ב‑COX‑2, לחסום אותות כאב ולהשאיר במידה רבה את פעילות ההגנה של COX‑1. הבנת הצורה המדויקת של הכיס הזה, וכיצד מולקולות התרופה מתמקמות בתוכו, היא מהותית לתכנון תרופות חדשות שיהיו גם יעילות וגם בטוחות.
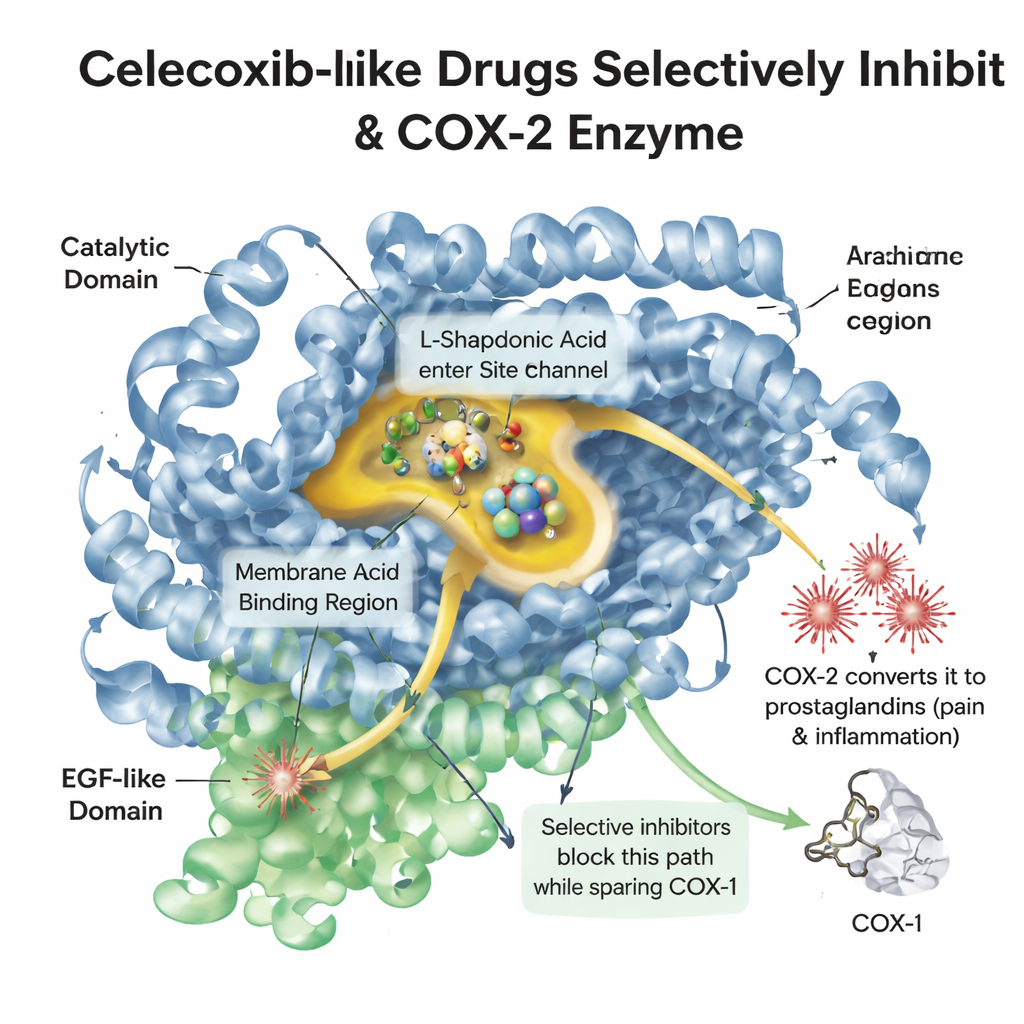
ספריה דיגיטלית של תרופות דומות במראה
החוקרים הרכיבו אוסף של 375 מולקולות שמשתפות את המסגרת התלת‑טבעתית הבסיסית של סלקוקסיב אך שונות בדרכים קטנות, כגון החלפה של אטום יחיד או קבוצת צד. הם שלפו את המבנים האלה ואת יעילות החסימה של COX‑2 שנמדדה מתוך מסד נתונים ציבורי לתרופות. באמצעות תוכנות כימיה ייצרו מודלים תלת‑ממדיים של כל מולקולה, חישבו כמעט 2,000 תיאורים מספריים של צורתן ותכונותיהן, ולאחר מכן דוקקו אותן למבנה ברזולוציה גבוהה של אנזים COX‑2. בדוקינג, מחשב מדרבן את המולקולה לתוך כיס האנזים בדרכים רבות ומעניק ניקוד עד כמה כל תנוחה מתאימה בצפיפות.
מה באמת שולט בחוזק ובבחירה
הצוות התרכז בשלוש אזורים מרכזיים בסלקוקסיב. "אתר‑1" הוא טבעת שיושבת באזור שומני בכיס; "אתר‑2" הוא טבעת הנושאת זנב עשיר בפלואור; ו"אתר‑3" הוא טבעת הנושאת קבוצת סולפונאמיד שיוצרת קשרי מימן חזקים. הניתוח שלהם הראה שאתר‑1 מעדיף קבוצות קטנות ולא‑קוטביות ששומרות על מגעים הידרופוביים; הפיכת האזור לידידותי יותר למים, למשל על ידי הוספת קבוצת –OH או חומצה, בדרך כלל החלישה את התרופה. באתר‑2, קבוצות אלקטרונגרטיביות קטנות כמו פלואור שיפרו לעתים קרובות את החוזק על ידי שיפור אינטראקציות בכיס הדחוס, בעוד זנבות גדולים או קוטביים יותר נטו לפגוע בפעילות. באתר‑3, החנקן בסולפונאמיד, היכולת לתרום קשר מימן, היה קריטי; החלפתו בגרסה שאינה יוצרת קשרים הורידה במובהק את הקשירה.
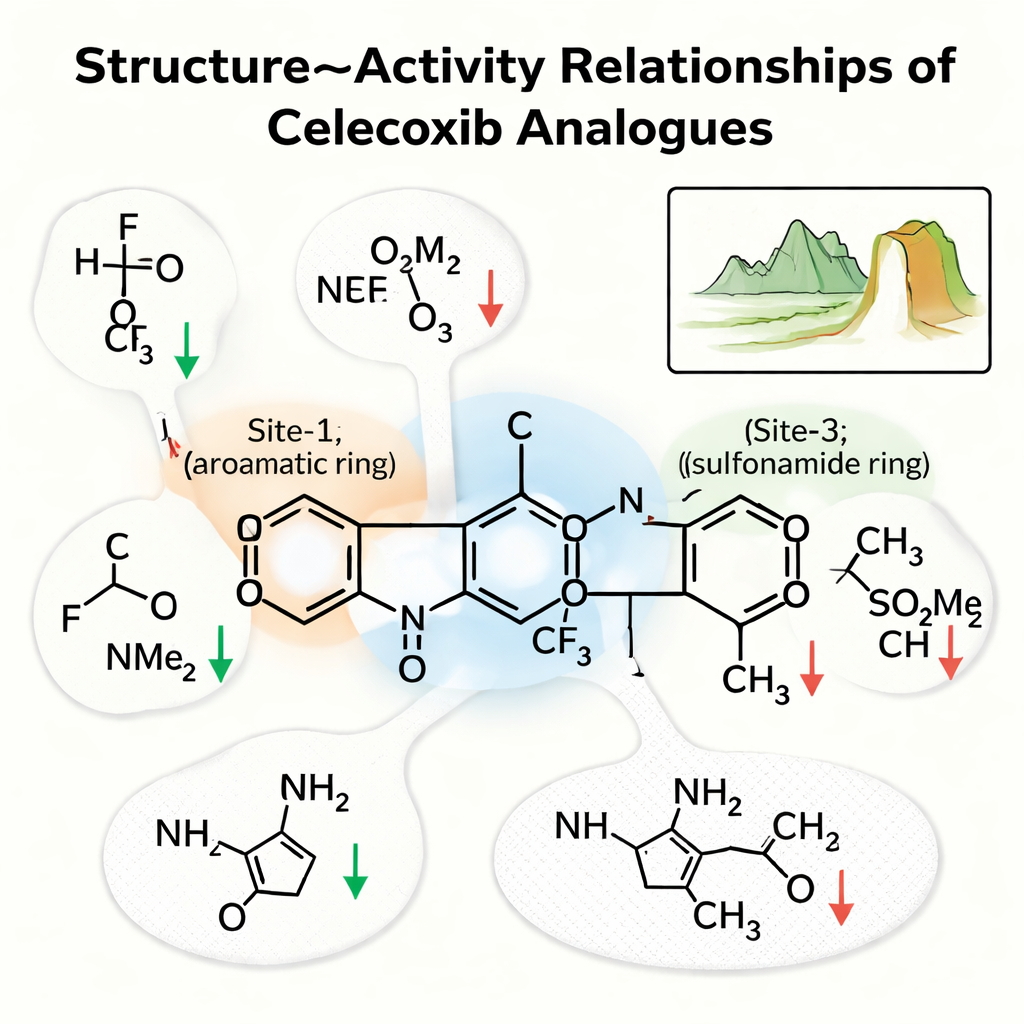
צוקים בנוף הכימי
כדי להתקדם מעבר למגמות פשוטות, המחברים בנו "נוף מבנה‑פעילות", ששואל עד כמה קפיצת החוזק של התרופה מתרחשת כאשר המבנה משתנה מעט בלבד. במבט זה, רוב תרכובות הדומה לסלקוקסיב נמצאות על גבעות מתונות: זעזוען — למשל, הזזת הלוגן או הוספת קבוצה קטנטנה גמישה — מייצר שינויים צפויים בעוצמה. אבל כמה זוגות יוצרים "צוקי פעילות" חדים, שבהם שינוי זעום, כגון החלפת מתיל בקבוצת טריפלואורומטיל או הוספת אטום פלואור יחיד, גורם לרווח או לאובדן דרמטי של פעילות. המחקר גם הריץ סימולציות דינמיקות מולקולריות מלאות — סרטונים וירטואליים של קומפלקסים תרופה‑אנזים בתנועה — שאישרו שהאנלוגים הטובים ביותר יושבים בצורה יציבה בכיס במשך מאות ננו‑שניות.
מניעת דור הבא של משככי כאב בטוחים יותר
עבור מי שאינו מומחה, המסקנה היא שבעיצוב תרופתי, הפרטים הקטנים חשובים עד מאוד. שתי תרכובות שנראות כמעט זהות על הנייר יכולות להשתנות במאות עד אלפי מונים בעוצמת החסימה של COX‑2, פשוט משום שאטום נוסף אחת משפר את ההתאמה בכיס מיקרוסקופי או מפריע למגע מרכזי. על ידי מיפוי שיטתי של אילו שינויים עוזרים או מזיקים בכל אחד משלושת האתרים המרכזיים של סלקוקסיב, ובהדגשת "הצוקים" המסוכנים שבהם שינויים זעירים משפיעים יתר על המידה, עבודה חישובית זו מציעה מפת דרכים לכימאים. היא מצביעה לכיון של תרופות אנטי‑דלקתיות חדשות שישמרו את עוצמת ההקלה של סלקוקסיב תוך קידום הבטיחות והסלקטיביות אף יותר.
ציטוט: Grewal, S., Ghosh, B., Narayan, U. et al. Computational strategies for unraveling insights from known inhibitors for further lead optimization: A case study on Celecoxib analogues. Sci Rep 16, 6720 (2026). https://doi.org/10.1038/s41598-026-37798-z
מילות מפתח: מעכבי COX-2, אנלוגים של סלקוקסיב, תרופות אנטי‑דלקתיות, עיצוב תרופתי חישובי, מבנה‑פעילות