Clear Sky Science · he
SIRT3 מדכאת התקדמות סרטן הכליה על ידי ויסות אצטילציה של IDH2
מדוע מחקר הסרטן של הכליה הזה חשוב
סרטן הכליה, ובפרט סוג הנקרא קרצינומה של תאי הכליה, הופך נפוץ יותר ולעתים קשה לטפל בו לאחר שהוא מתפשט. המחקר בוחן את מה שמתרחש בתוך תאי הסרטן כדי להבין כיצד שינויים זעירים במפעלי האנרגיה שלהם — המיטוכונדריות — מסייעים לגידולים לגדול, וכיצד תרכובת טבעית מן הצמחים, הונוקיול, עשויה לסייע להאט אותם. עבור הקוראים זה מציע הצצה לאופן שבו הבנת ה"תחזוקה" התאית יכולה לפתוח אופציות חדשות מעבר לתרופות הקיימות.
בלם חבוי בתוך תאי הכליה
תאים שלנו מנהלים באופן רציף את ייצור האנרגיה ואת התוצרים המזיקים שנוצרים בתהליך. בתאי כליה בריאים, חלבון בשם SIRT3 פועל כמפקח תחזוקה בתוך המיטוכונדריות, ושומר על חלבונים אחרים במצב תפקודי. המחברים בחנו מאגרי נתונים ציבוריים רחבים של סרטן ודגימות רקמת חולים ומצאו שרמות SIRT3 היו באופן עקבי נמוכות בגידולי הכליה לעומת הרקמה הסמוכה התקינה. גידולים בעלי הרמות הנמוכות ביותר של SIRT3 הציגו דפוסי ביטוי גנים הקשורים לגידול מהיר יותר ויכולת תנועה מוגברת, מה שמרמז שכאשר ה"בלם" התאי הזה אובד, תאי הסרטן נעשים אגרסיביים יותר.
כיצד תאי הסרטן מעוותים את מאזן האנרגיה שלהם
כדי לבדוק האם אובדן SIRT3 אכן מניע את ההתנהגות הסרטנית, החוקרים הפחיתו SIRT3 בקווי תאי סרטן כליה שגודלו במעבדה. תאים עם פחות SIRT3 השתכפלו מהר יותר ויצרו הרבה יותר מושבות, סימן לשרידות וגדילה מוגברת. כאשר תאים אלה הושתלו בעכברים, הגידולים שהתפתחו היו גדולים וכבדים יותר מאשר גידולים שמקורם בתאים ביקורתיים. יחד, הניסויים האלה מראים ש-SIRT3 לא רק חסר בסרטן הכליה — הוא למעשה מעכב את גדילת הגידול כאשר הוא נוכח.
אנזים מרכזי ובעיית ה"חלודה" בתא
הצוות התמקד אז בחלבון מיטוכונדריאלי נוסף, IDH2, שעוזר לייצר NADPH, מולקולה שתומכת במערכות שמנטרלות סוגי חמצן תגובתיים (ROS) — כימיקלים מזיקים הדומים ל"חלודה" תאית. ניתן לשנות את התנהגותו של IDH2 על ידי הוספה של תג כימי קטן הנקרא אצטיל. ידוע ש-SIRT3 מסיר תגיות כאלה. בתאי סרטן כליה, SIRT3 נקשר פיזית ל-IDH2 והסיר קבוצות אצטיל במיקום ספציפי (K413). כאשר SIRT3 הופחת, סימן האצטיל הצטבר, פעילות IDH2 ירדה, רמות ה-NADPH פחתו ורמות ה-ROS עלו. המיטוכונדריות איבדו חלק מהממברנה הפוטנציאלית שלהן, סימן לתפקוד לקוי. באמצעות וריאנטים מהונדסים של IDH2 שחיקו את המצב האצטילטי או את המצב הלא-אצטילטי, המחברים הראו שהצורה האצטילטית יכולה להתגבר על השפעת האטת הגדילה של SIRT3, וקשרה את הבלם הסרטני למתג הכימי היחיד הזה.
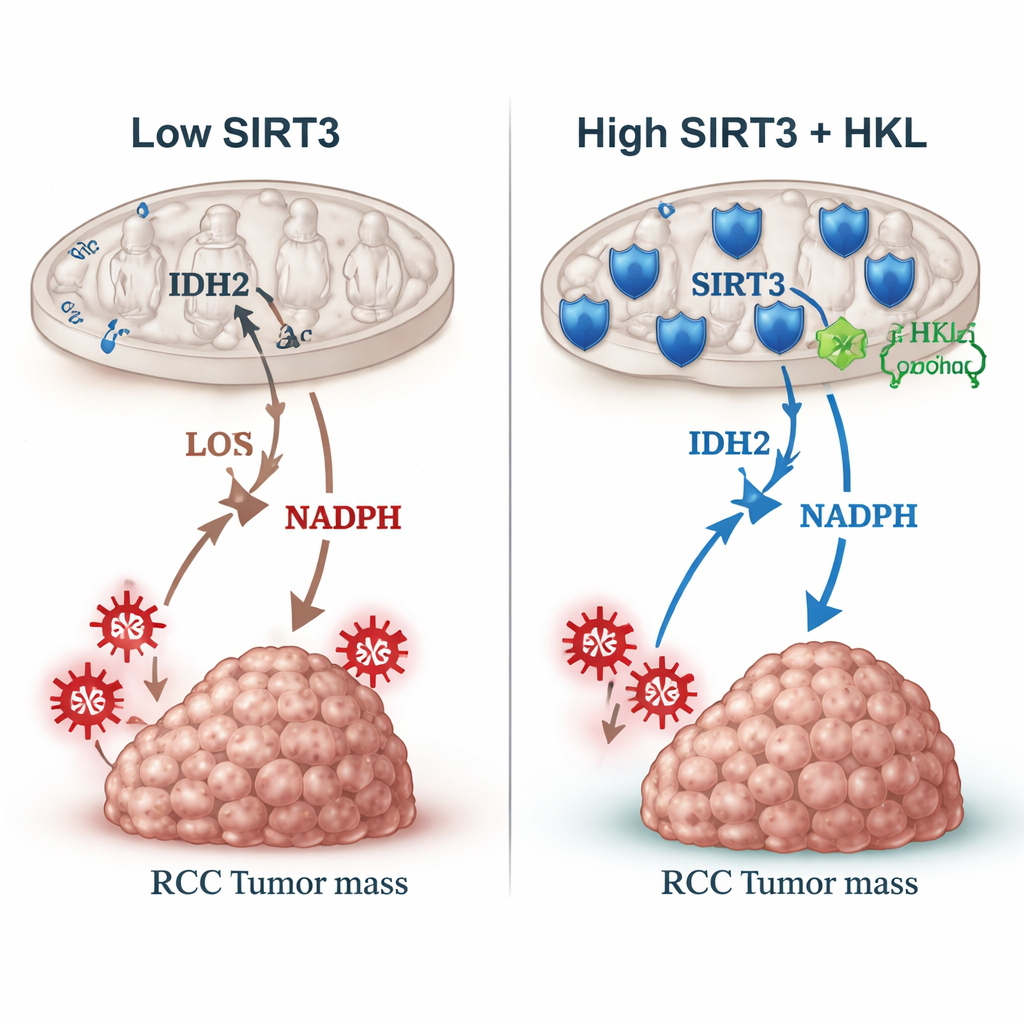
להפעיל מחדש את הבלם עם תרכובת צמחית
מכיוון ש-SIRT3 נראה כמגן, המחברים שאלו האם ניתן להגבירו בעזרת תרופה. הם בחנו את הונוקיול, מולקולה טבעית מקליפת המגנוליה הידועה כבר כמקיימת השפעות על מסלולי סרטן שונים. במינון שנבחר בקפידה שלא ימית את התאים ישירות, הונוקיול הגדיל עם הזמן את רמות SIRT3 בתאי סרטן כליה, לצד רגולטורים קשורים (p-AMPK ו-PGC-1α). עם עליית SIRT3, IDH2 איבד את תג האצטיל, רמות ה-ROS ירדו והתאים גדלו ויצרו מושבות לאט יותר. כאשר הונוקיול שُילב עם סונטיניב, תרופה סטנדרטית לסרטן הכליה, השילוב דיכא את הגדילה יותר מאשר סונטיניב לבד, בחלקו על ידי הרחקת עודף ה-ROS שסונטיניב עצמו עלול לגרום. השפעות דומות נצפו כאשר החוקרים השתמשו בנוגד חמצון קלאסי, מה שתומך ברעיון ששימת שליטה על הלחץ החמצוני יכולה להפוך טיפולים קיימים ליעילים יותר.
מה זה עשוי להשפיע על טיפולים עתידיים
לעיני הלא-מומחים, המסר המרכזי הוא שהמחקר מזהה את SIRT3 כבלם טבעי של גידול בסרטן הכליה, שפועל דרך ויסות עדין של IDH2 ומאזן בין מולקולות מגנות למזיקות בתוך המיטוכונדריה. כאשר SIRT3 נמוך, תאים צוברים ROS שמקדם נזק ומשיגים יתרון גדילה. שיקום פעילות SIRT3 — אולי באמצעות הונוקיול או תרופות עתידיות מדויקות יותר — עשוי להאט את גידול הגידול ולעזור לטיפולים הקיימים לפעול טוב יותר. אף שהונוקיול עצמו עדיין ניצב בפני אתגרים, כולל קליטה ויעדיות מרובות, העבודה מצביעה על מסלול ברור — ציר SIRT3–IDH2–רדוקס — שאנשי פיתוח תרופות יכולים כעת למקד אליו כדי לעצב טיפולים חכמים יותר, מבוססי מטבוליזם, לקרצינומה של תאי הכליה.
ציטוט: Li, L., Tian, Y., Chen, S. et al. SIRT3 suppresses renal cancer progression by regulating IDH2 acetylation. Sci Rep 16, 7619 (2026). https://doi.org/10.1038/s41598-026-37783-6
מילות מפתח: סרטן הכליה, SIRT3, מיטוכונדריה, לחץ חמצוני, הונוקיול