Clear Sky Science · he
שינויים במודיפיקציות היסטונים במעיים של Aedes aegypti לאחר חשיפה לווירוס חום העמקים של ריפט ואלי
למה הגנים של היתושים חשובים לבריאות האדם
וירוס חום העמקים של ריפט ואלי מחלה בהמה ובני אדם בחלקים מאפריקה ומועברת על‑ידי יתושים. כדי למנוע התפרצויות, מדענים צריכים להבין לא רק את הווירוס עצמו אלא גם כיצד היתושים מגיבים כשהם בולעים דם נגוע. המחקר הזה בוחן את מעי היתוש ברזולוציה יוצאת דופן, ושואל כיצד הווירוס משנה את אריזת ה‑DNA של היתוש כדי להפעיל או לכבות גנים קריטיים — שינויים שיכולים להשפיע האם החרק יהפוך למעביר יעיל או חלש של המחלה.
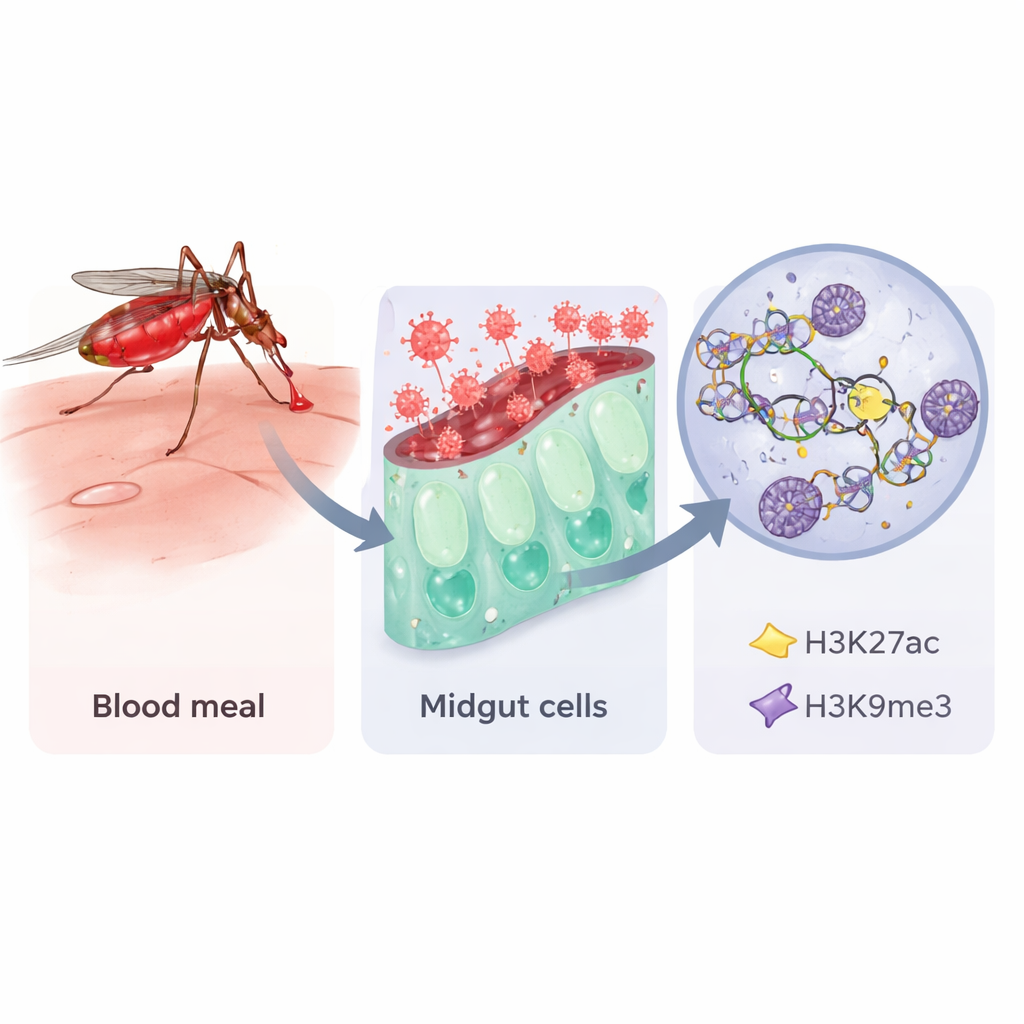
לפתוח את ספר ה‑DNA של היתוש
כמו בבני אדם, יתושים לא משנים את אותיות ה‑DNA שלהם כשהם נחשפים לזיהום, אך הם יכולים לשנות עד כמה ה‑DNA דחוס. המחברים התמקדו בשתי תגיות כימיות על חלבוני היסטון, שמשמשים כגלגלות ל‑DNA. תגית אחת, שנקראת H3K27ac, בדרך כלל מסמנת מקטעים פתוחים ופעילים של ה‑DNA; השנייה, H3K9me3, מקושרת לאזורים מושתקים ושקטים. באמצעות שיטה רגישה הנקראת CUT&RUN, בשילוב רצף RNA, הצוות בחן את התגיות הללו ואת פעילות הגנים במעיים של Aedes aegypti לאחר שלושה סוגי ארוחות: סוכר בלבד, ארוחת דם רגילה, או דם המכיל זן חיסון של וירוס חום העמקים של ריפט ואלי. הם אספו דגימות מהמעיים יום, שלושה ו‑שבעה ימים לאחר ההאכלה כדי לתפוס שלבי זיהום מוקדמים, אמצעיים ומאוחרים.
כיצד ארוחת דם פשוטה מחדש לחצת את המעי
ארוחת דם לבדה, גם ללא וירוס, גרמה לשינויים נרחבים בפעילות הגנים במעי. אלפי גנים שינו את פעילותם יום אחד לאחר ההאכלה, בייחוד אלה המעורבים בעיכול חלבונים, בניהול אנרגיה ובבניית רכיבים תאיים חדשים. רבים מהגנים הללו שכנו ליד אזורים המסומנים ב‑H3K27ac, תואם לרעיון שדם מעורר את המעי לפתוח שכונות DNA ספציפיות הנדרשות לעיכול ולהפקת ביציות. בימים הבאים, ככל שהדם עוכל, התבנית התפתחה: מכונות ייצור האנרגיה נותרו פעילות, ולמעשה בהמשך הושפעו גנים המעורבים בארגון כרומוזומים ומחזור התא. היתושים שבקבוצת הביקורת של הסוכר הראו לעומת זאת דפוסים יציבים יותר, מה שמרמז כי שלא קיום ארוחת דם עשוי להוביל לנוף DNA שונה, שאולי קשור להזדקנות.
כשווירוס פוגש את הגנות המעי
הוספת וירוס חום העמקים של ריפט ואלי לדם שינתה את התמונה. בתחילה, יום אחד ושלושה לאחר ההאכלה, מעי היתושים שנחשפו לווירוס הגבירו פעילות גנים הקשורים להגנה חיסונית ולהעברת אותות בתא, מעבר לשינויים שנגרמו על ידי הדם בלבד. בו‑זמנית, הקשרים הרגילים בין תגיות ההיסטון והגנים הסמוכים הפכו למורכבים יותר. במיוחד ביום השלישי, אזורים רבים שסומנו בדרך כלל בתגית המושבתת H3K9me3 איבדו את הסימון ההוא, ומאות גנים סמוכים הפכו ליותר פעילים, כולל אלה המעורבים בשליטה על גנים אחרים, בהעברת אותות בתוך התא ובניהול צורת התא וקוטביותו. ביום השביעי, כאשר כ‑חצי מהיתושים נשאו וירוס מדבק, הפעילות הגנית הכוללת במעיים החשופים ירדה, גנים הקשורים למערכת החיסון דוכאו, וסימונים מעוררי פעילות מסוג H3K27ac נדחקו באופן נרחב בהשוואה לביקורת הדם בלבד.
רמזים לתכסיסי וירוס והגנות היתוש
על‑ידי התאמת פעילות גנים לשינויים בקרבת ההיסטונים, החוקרים זיהו קבוצה קטנה של גנים שההתנהגות שלהם מעוררת חשד. כמה גנים המסייעים לארגן מבני ממברנה או להזיז חומרים בתוך התאים הגבירו את הפעילות בעוד שהתוויות המעוררות המקומיות שלהם נחלשו, מה שהופך אותם למועמדים לסיוע בהרכבה או בהעברה של הווירוס בתוך התא. אחרים, כגון גנים הקשורים לנטרול מולקולות ריאקטיביות או לזיהוי פתוגנים, הציגו דפוסים התואמים לתפקודים אנטי‑ויראליים. גן אחד בולט, הנושא תחום חלבוני שמוכר מגורמי אנטי‑ויראליות בבני אדם, ראה עלייה ב‑RNA תוך כדי אובדן גם של סימני היסטונים מעוררים וגם מכבידים, דבר המרמז על לחץ רגולטורי חזק במהלך הזיהום. המחקר גם הדגיש מסלול פולריות תאית, הקרוי smoothened/hedgehog, שאמצעיו דוכאו בשלב מאוחר של הזיהום, תואם לראיות שרבות מהווירוסים מעדיפים תאים בעלי פולריות גבוהה.
מה המשמעות הזו לשליטה במחלות מועברות על‑ידי יתושים
ללא‑מומחה, המסר המרכזי הוא שתאי המעי של היתוש אינם מקבלים פלישת וירוס באופן פסיבי. הם מעצבים במהירות מחדש את אריזת ה‑DNA שלהם, ראשית כדי להניע עיכול ורבייה לאחר ארוחת דם, ולאחר מכן להפעיל — או לפעמים להחליש — הגנות נגד וירוס חום העמקים של ריפט ואלי. שתי תגיות היסטון, H3K27ac ו‑H3K9me3, משתנות בצורה מורכבת במהלך המאבק הזה, ומשפיעות על אילו גנים יכולים להגיב. אף שרק חלק מהשינויים הגנטיים ניתן לקשור ישירות לתגיות אלה, העבודה מראה שסימנים אפיגנטיים מהווים שכבה חשובה בתשובת היתוש לזיהום. בטווח הארוך, הבנת המתגים הללו עשויה לסייע למדענים לעצב אסטרטגיות חדשות שהופכות יתושים לפחות מסוגלים לשאת וירוסים, ולהוסיף כלי נוסף למאבק במחלות חדשות המועברות על‑ידי יתושים.
ציטוט: Ogg, H.A., Mikol, Z.M., King, D.C. et al. Altered histone modifications in Aedes aegypti midguts following Rift Valley fever virus exposure. Sci Rep 16, 6605 (2026). https://doi.org/10.1038/s41598-026-37729-y
מילות מפתח: וירוס חום העמקים של ריפט ואלי, Aedes aegypti, אפיגנטיקה ביתושים, מודיפיקציות היסטונים, יכולת וקטורית