Clear Sky Science · he
אפיונן בחומרה של תחום הקטליטי של דה-אצטילאז היסטון 5 אנושי
למה מתגים זעירים באריזת ה‑DNA שלנו חשובים
בתוך כל תא, ה‑DNA שלנו מסולל סביב חלבונים שמשמשים כמוטות ומסייעים להכניס מטרים של חומר גנטי אל תוך מרחב מיקרוסקופי. האם גן נדלק או כבוי תלוי לעיתים קרובות בסימני כימיה קטנים על חלבונים אלה. המחקר הזה מתמקד במתג חלבוני מסוים בשם HDAC5, שמקושר למחלת לב, הפרעות מוחיות, סרטן ועוד. בהבנה של אופן הפעולה של HDAC5 ברמה מולקולרית, מקווים החוקרים לסלול דרך לתרופות מדויקות יותר עם פחות תופעות לוואי.
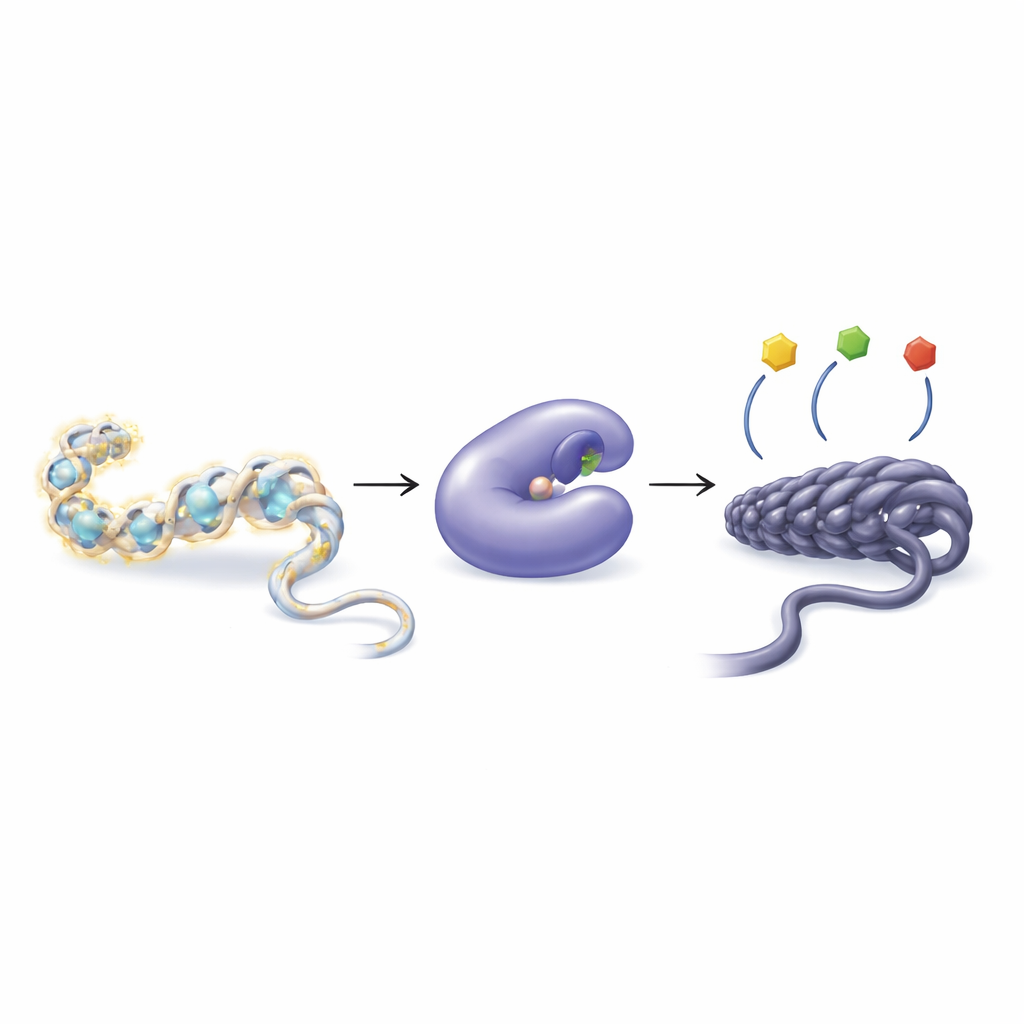
איך תאים מכוונים גנים עם תגיות כימיות זעירות
ה‑DNA שלנו לא צף חופשי אלא מלופף סביב חלבונים שנקראים היסטונים, ויוצר מבנה המכונה כרומטין. תאים יכולים להצמיד או להסיר קבוצות כימיות קטנות, כמו קבוצות אצטיל, מקצוות ההיסטונים כדי להרחיב או לכווץ את הכרומטין. אריזה רופפת בדרך כלל מקלה על קריאת גנים; אריזה הדוקה נוטה להשתיקם. שתי קבוצות אנזימים מנהלות את האיזון הזה: היסטון אצטילטרנספראזות מוסיפות קבוצות אצטיל, בעוד דה‑אצטילאזי היסטון (HDAC) מסירים אותן. כאשר האיזון הזה משתבש, הוא עלול לתרום למגוון מחלות כולל סרטן, בעיות לב, אובדן שריר והפרעות חיסון.
למה HDAC5 הוא יעד מבטיח אך מסובך לתרופות
HDAC הם משפחה רחבה של אנזימים קשורים המחולקים למספר מחלקות. תרופות רבות שבשימוש קליני חוסמות כמה סוגי HDAC בבת אחת, מה שעלול לשתק תפקודים נורמליים חשובים ולגרום לתופעות לוואי חריפות. דה‑אצטילאזי המחלקה IIa, כולל HDAC5, בולטים כי הם נפוצים ברקמות ספציפיות כמו מוח, לב ושרירשלד והם משתפים פעולה עם חלבונים אחרים לוויסות רשתות גנים מפתח. HDAC5 לעיתים משמש כגשר, מביא אנזים שותף בעל פעילות גבוהה (HDAC3) לגנים מסוימים כדי להדק את הכרומטין ולשתוק אותם. בשל התפקידים הממוקדים האלה, HDAC5 נחשב ליעד אטרקטיבי לתרופות סלקטיביות יותר, אך היה מחסור בנתונים ביוכימיים מפורטים ולא הייתה מבנה רזולוציה גבוהה של הליבה הפעילה שלו, מה שהקשה על תכנון רציונלי של תרופות.
שיקום HDAC5 בצינור מבחנה
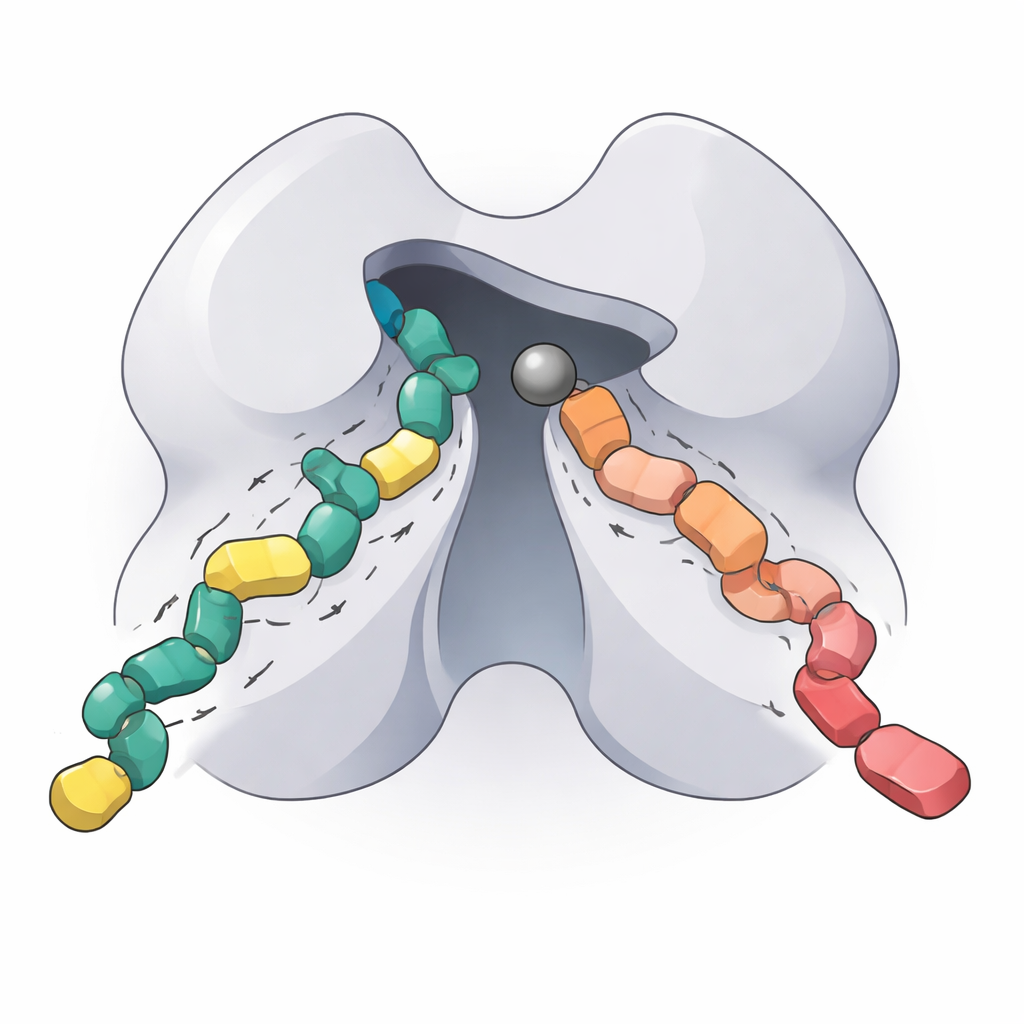
כדי לטפל בפער הזה, החוקרים ייצרו רק את הליבה הקטליטית של HDAC5 האנושי — החלק שמבצע את התגובה הכימית — בחיידקים, טיהרו אותו ואישרו שהוא יוצר בחלופה יציבה של יחידה בודדת בחסרון. לאחר מכן בדקו עד כמה הוא פעיל בתנאי מלחים וחומציות שונים. הפעילות של HDAC5 נותרה חזקה בטווח רחב של ריכוזי מלח ושיאתה היתה בתנאים מעט בסיסיים, בדומה לסביבה בתוך תאים רבים. באמצעות מולקולות בדיקה פלואורסצנטיות מיוחדות, הם מצאו שהצורה הטבעית של HDAC5 מזהה רק סוג אחד מסוים של סובסטרט המשמש לבחינת אנזימי המחלקה IIa. בהובלת מחקרים קודמים על HDAC קשורים, החליפו חומצת אמינו אחת (היסטידין) לטירוזין במיקום קריטי. באופן מרשים, שינוי קטן זה איפשר לגרסה המוטנטית של HDAC5 לעבד ביעילות שני סוגי סובסטרטים, מה שמאיר כיצד שייר יחיד באתר הפעיל מכוון את העדפתו הכימית של האנזים.
בדיקה והשוואה של שני מועמדי תרופות חדשים
הצוות בדק לאחר מכן שתי מולקולות ניסיוניות החוסמות HDAC5, הידועות כ‑NT160 ו‑FFK24. תרכובות אלה משתמשות בקבוצת קישור חדשה לאבץ שממזערת חלק מההרעלות והחוסר בסלקטיביות שנצפו בתרופות ישנות המבוססות על הידרוקסאמאט. על ידי מדידת האופן שבו כל מעכב האט את HDAC5 בתגובות מבוקרות בקפידה, המחברים קבעו קבועי מעכבות נמוכים מאוד בטווח הננומולרי, כלומר שתי התרכובות נקשרות חזק לאנזים. NT160 קישר בעקביות בערך בעוצמה פי עשרה יותר מאשר FFK24. כדי להבין מדוע, החוקרים השתמשו בעיגון ממוחשב (דוקינג) עם מבנה לחזות AlphaFold של הליבה של HDAC5. לשני המעכבים היה אזור ראש משותף שנכנס עמוק לכיס הפעיל ונגע ביון המתכת, אך הזנב של NT160 יצר קשרים מייצבים נוספים עם חומצות אמינו ספציפיות בכיס. אינטראקציות נוספות אלה ככל הנראה מסבירות את החוזק הגדול יותר שלו.
מה זה אומר לטיפולים ממוקדים בעתיד
על ידי שיקומו של ליבה עובדת של HDAC5, מיפוי תנאי הפעולה האופטימליים שלו, ניתוח כיצד החלפת חומצת אמינו בודדת משנה את התנהגותו וכימות האופן שבו שני מעכבים מהדור הבא נקשרים, המחקר הזה מספק "טביעת אצבע" ביוכימית מפורטת של אנזים חשוב אך קודם לכן לא מתואר. לקהל שאינו מומחה, המסקנה המרכזית היא ש‑HDAC5 עוזר לשלוט האם גנים מסוימים פעילים או מושתקים, וכי כוונון מדויק של המתג הזה עשוי להיות שימושי בטיפול במחלות לב, נוירודגנרציה, סרטן והפרעות חיסוניות. התובנות והכלים החדשים שמוצגים כאן אמורים לסייע לחוקרים לעצב תרופות סלקטיביות נגד HDAC5 ומחלקה IIa — שפועלות במקום הנדרש ובו בזמן ממזערות השפעות לא רצויות בשאר הגוף.
ציטוט: Mammen, C., Hornung, F.M., Anzenhofer, C. et al. In vitro characterization of the catalytic domain of human histone deacetylase 5. Sci Rep 16, 7935 (2026). https://doi.org/10.1038/s41598-026-37633-5
מילות מפתח: דה-אצטילאז היסטון 5, ויסות אפיגנטי, מעכבי HDAC, טיפול ממוקד בסרטן, מבנה הכרומטין