Clear Sky Science · he
שינויים בפעילות EGFR לאחר עריכת CRISPR/Cas9 של אתר קשירת EGF
למה חשוב לשנות מחדש מסלול איתות סרטני
סרטן צוואר הרחם תכופות תלוי במתג צמיחה רב־עוצמה המכונה קולטנית גורם הצמיחה האפידרמלי (EGFR). בגידולים רבים יש כמות עצומה של קולטן זה, ובכל זאת תרופות שמטרתן לחסום אותו עזרו רק לחלק מהמטופלים. המחקר הזה בדק שאלה יסודית עם השלכות טיפוליות משמעותיות: מה קורה אם מסירים את יכולת EGFR לתפוס את אות הצמיחה המועדף עליו, גורם הצמיחה האפידרמלי (EGF), מבלי להסיר את הקולטן עצמו?
כיבוי "מפתח ההפעלה" מולקולרי
החוקרים התמקדות בקו תאי של סרטן צוואר הרחם שנושא כמויות גדולות של EGFR תקין במרביתו. במקום להרוס את הגן, השתמשו בעריכת הגנום CRISPR/Cas9 כמספר נפוץ כדי לשנות רק כמה חומצות אמינו בכיס הקשירה של EGF ב‑EGFR. שני מיקומים מסוימים, הקרויים L14 ו‑Y45, מסייעים לעגן את EGF על הקולטן. על‑ידי החלפת אבני הבניין הללו באחרות, ניסתה הצוות לשמור על נוכחות EGFR אך לעקור ממנו את היכולת לזהות EGF, וכך לבודד את תפקיד האינטראקציה הבודדת הזו בהתנהגות תאי הסרטן.
בנייה של קווי תאים סכמטיים
בשלב ראשון בדקו את המוטציות הללו בתאים באמצעות פלסמידים שמייצרים באופן חולף EGFR רגיל או משונן. EGF שסומן בפלואורסצנציה הראה שכל הצורות המוטנטיות קשורות להרבה פחות ליגנד מאשר הקולטן הרגיל, במיוחד כאשר L14 ו‑Y45 שונו יחד. לאחר מכן החוקרם הוצגו את השינויים האלה ישירות לגנום התאי באמצעות CRISPR/Cas9, ויצרו כמה שיבוטים תאים חדשים. חלק נשאו מוטציה בודדת, אחרים נשאו את המוטציה הכפולה בעותק אחד של EGFR ושינויים מנטרלים בעותק השני. דגמי מחשב של צורות החלבון שהתקבלו הראו שהשינויים האלה עיוותו את אתר הקשירה מספיק כדי להחליש או לבטל את עיגון EGF, בהתאם לניסויי הקשירה.
כאשר הקולטן זז אך התאים שורדים
דימות מפורט גילה כי הקולטנים הערוכים התנהגו באופן שונה מאוד בתוך התא. בתאי הסרטן שלא נערכו, EGFR יושב על ממברנת התא, לקולט EGF ולאחר מכן נע פנימה תוך הפעלה כימית דרך זרחון. בשיבוטים הנושאים את המוטציה הכפולה, קשירת EGF כמעט נעלמה ו‑EGFR כבר לא נראה על הממברנה; במקום זאת כמות קטנה של הקולטן שנותרה הצטברה בפנים התא. גם שינוי יחיד ב‑Y45 צמצם משמעותית את הקשירה והקטין את רמות EGFR הכוללות. עם זאת, למרות ההפרעה למסלול האיתות המוכר EGF–EGFR, תאי הסרטן נותרו חיים והמשיכו לגדול בתרבית עם שינויים מתונים בלבד בדפוסי מחזור התא שלהם.
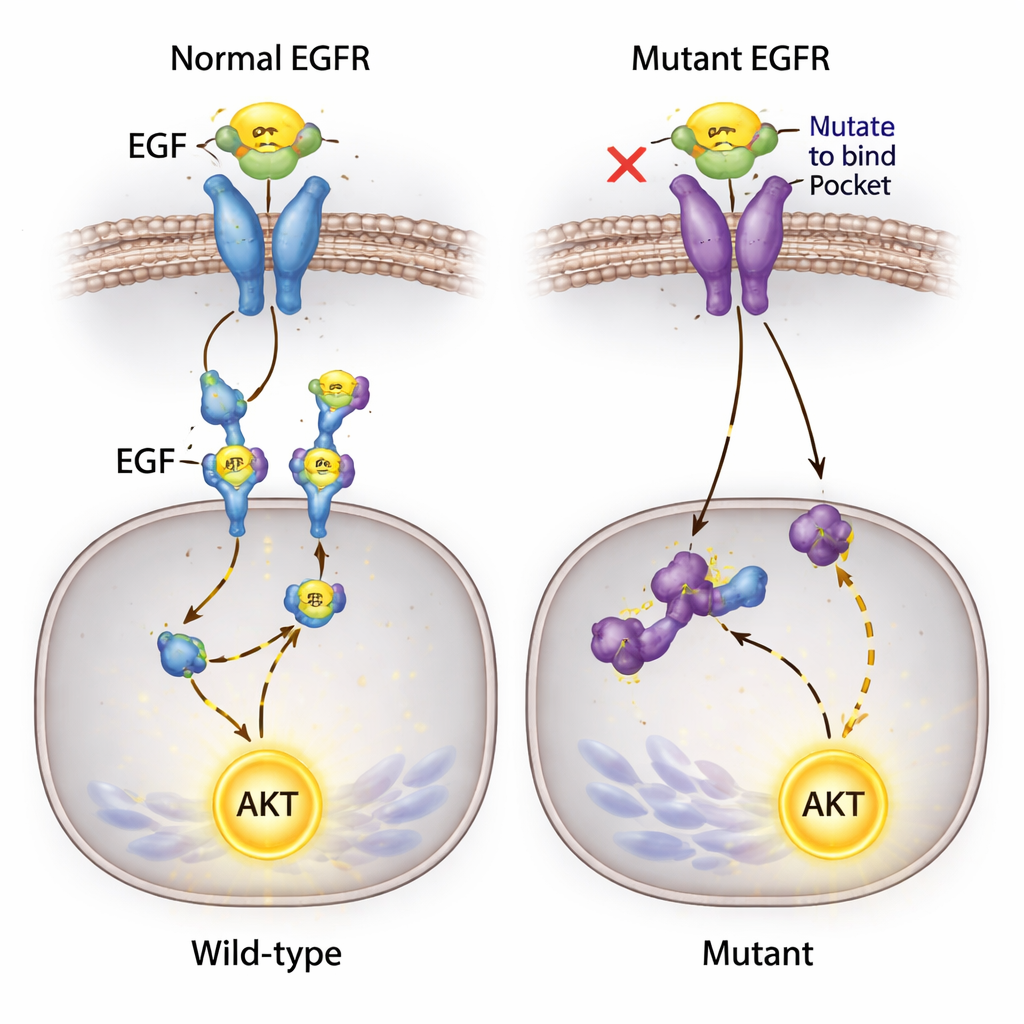
אות בלתי צפוי שלא מפסיק
אחד הממצאים המפתיעים ביותר הסתבך סביב AKT, חלבון מפתח שמעודד שרידות תאים ובדרך כלל מופעל מטה ל‑EGFR. החוקרים ציפו שחסימת קשירת EGF–EGFR תשקיט את המסלול הזה. במקום זאת, כאשר הוסיפו EGF למדיום, AKT הופעל בעוצמה בכל קווי התאים — כולל באלה שבהם EGF כבר לא הצליח לקשור את EGFR ושבהם זרחון הקולטן לא היה נראה. מאחר שהתאים אלה נושאים מוטציה ידועה בגן איתות אחר, PIK3CA, הצוות חושד שדרכים חלופיות עשויות לאפשר ל‑EGF לתרום להפעלת AKT, אולי דרך חלבונים ממברנליים אחרים או מוטציות רקע, ומעקפות את EGFR שעבר עריכה.
שינויים גנטיים חבויים וטיפולים עתידיים
כדי לוודא ש‑CRISPR אינו גורם לעריכות לא מכוונות נרחבות, המדענים רצפו את הגנומים המלאים של קווי התאים החדשים. הם אימתו שהמוטציות הרצויות ב‑EGFR אכן נמצאות ולא מצאו ראיות לחתכים באתרי יעד משוערים של מדריכי CRISPR. עם זאת, זיהו שפע של מוטציות ספונטניות שפזורות ברחבי הגנום, שחלקן עלולות להשפיע על התנהגות התאים. ממצא זה מדגיש שאפילו כאשר CRISPR פוגע ביעד המתוכנן, ה‑DNA הבלתי יציב של תאי סרטן יכול לסבך את פרשנות התוצאות הניסיוניות ואת תכנון טיפולים גנטיים מדויקים.
מה משמעות הדבר עבור מטופלים
לקריאה ציבורית, המסר המרכזי הוא כי חסימת הלחיצה הידידותית בין EGF ל‑EGFR — אפילו בדיוק אטומי מאוד — אינה בהכרח עוצרת את קבלת פקודות "לגדול ולהישאר בחיים" על‑ידי תאי הסרטן. המחקר מראה שתאי סרטן יכולים לנתב מחדש אותות מרכזיים כמו הפעלת AKT סביב קולטן חסום, וכי יש להעריך בקפידה גם את עריכת ה‑CRISPR בכאלו גנומים בלתי יציבים. קווי התאים המהונדסים הללו מספקים כעת דגם מעבדה חזק לחיפוש אחר נתיבי גיבוי שמחזיקים גידולים התלויים ב‑EGFR, מידע שלבסוף עשוי להוביל לטיפולים משולבים המכוונים הן ל‑EGFR והן לשותפיו הנסתרים.
ציטוט: Popović, J., Hahut, A., Torres, G.E. et al. Changes in EGFR activity following CRISPR/Cas9-editing of the EGF binding domain. Sci Rep 16, 6797 (2026). https://doi.org/10.1038/s41598-026-37579-8
מילות מפתח: EGFR, סרטן צוואר הרחם, CRISPR, אותות EGF, מסלול AKT