Clear Sky Science · he
שיטה עם ליגאז ביוטין מפוצל חושפת חלבונים המקושרים לאלפא‑סינוקלאין באוליגומריזציה
למה הצטברות חלבונים במוח חשובה
במחלת פרקינסון ומצבים קרובים, חלבון מוחי השגרתי והמסייע בשם אלפא‑סינוקלאין עלול להצטבר לגושים דביקים הידועים כשממני לווי (Lewy bodies). הצטברויות אלה מופיעות עשורים לפני הופעת התסמינים ומהוות סימן מאפיין שבא לאחר המוות, אך אנחנו עדיין לא יודעים אילו חלבונים אחרים מסייעים לדחוף את אלפא‑סינוקלאין ממצב חסר‑נזק לצורת אגגרגטים מסוכנים. המחקר הנוכחי משתמש ב"תג‑קרבה" מולקולרי מעודן כדי למפות אילו חלבונים יושבים קרוב לאלפא‑סינוקלאין בזמן שהוא עובר ממולקולות בודדות לגושים קטנים, ומציע רמזים חדשים לאופן התחלת המחלה ולאיזה מסלולים ייתכן שניתן לכוון כדי להאט או למנוע אותה.
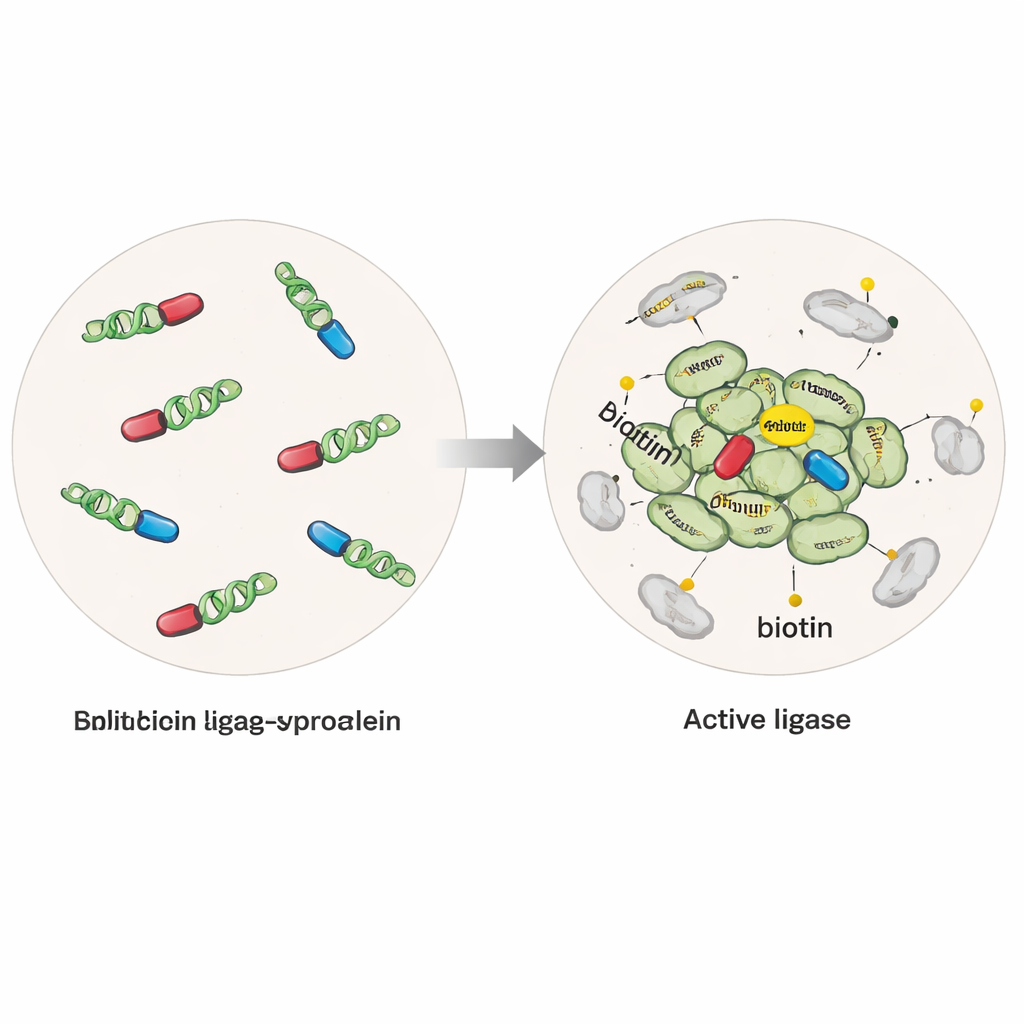
"תג" מולקולרי שמאיר את השכנים
החוקרים הנדסו תאים אנושיים כך שייצרו אלפא‑סינוקלאין מחובר לאנזים מותאם שיכול להצמיד תג ביוטין קטן לכל חלבון בטווח של מספר מיליארדי מטרים. בגרסה אחת האנזים היה שלם ופעל כל אימת שאלפא‑סינוקלאין היה נוכח, ותמך בלכידת חלבונים הקרובים הן למולקולות בודדות והן לגושים. בגרסה שנייה וסלקטיבית יותר, ה"מפוצלת", האנזים נותק לשני חצאים בתרדמם, כל חצי מצורף למולקולת אלפא‑סינוקלאין נפרדת. רק כאשר מולקולות אלפא‑סינוקלאין התקבצו למולטימרים או אוליגומרים החצאים התאחדו מחדש ולהפכו לאנזים פעיל, והתג הופעל באופן ספציפי סביב האגגרגטים הראשוניים האלה. על‑ידי הוספת פיברילות אלפא‑סינוקלאין מזוקקות לתאים, הצוות יכל גם להניע הצטברות דמוית‑מחלה ולהשוות בין מצבים נורמליים לפתולוגיים.
בניית מפת חלבונים קרובים
לאחר זמן התאמה עבור התיוג, הצוות שלף את כל החלבונים המסומנים בביו‑טין וזיהה אותם באמצעות ספקטרומטריה של מסה, טכניקה שמשקלת וסופרת חלבונים בדיוק גבוה. בכל התנאים נמצאו 1,277 חלבונים מובחנים, ולאחר סינון קפדני צמצמו זאת ל‑581 שנראו סבירים כהיו קרובים באמת לאלפא‑סינוקלאין. בהשוואה בין מערכות האנזים השלם והמפוצל, הם יכלו להבחין בין חלבונים שמקושרים בעיקר למולקולות בודדות לבין כאלה המעדיפים מולטימרים. הם גם השוו תאים עם ובלי פיברילות מוספות כדי לראות כיצד סביבת החלבונים המקומית של אלפא‑סינוקלאין משתנה ברגע שההצטברות מונעת.
מסלולים תאיים מרכזיים נמשכים לתוך הגושים
הסכימה של האינטראקטום מצביעה על מספר נושאים ביולוגיים מרכזיים. בתנאים נורמליים, אלפא‑סינוקלאין מולטימרי ישב קרוב להרבה חלבונים הקשורים לתנועה ממברנלית ולאנזימים המשנים חלבונים — דבר שמתיישב עם התפקיד המוצע שלו בסיוע לתאי עצב בניהול וזיקולות סינפטיות ושמירה על איכות החלבון. כמה אנזימים המוסיפים קבוצות זרחן, כולל קינאזות PAK4, RIPK2 ו‑MAP4K4, הועשרו בקרבת מולטימרים בריאים אך נראה שאיבדו מגע לאחר היווצרות האגגרגטים, מה שמרמז כי שיבוש קשרים אלה עשוי להעדיף צורות חלבון הקשורות למחלה. הצוות גם זיהה חלבונים הקשורים לאיתות דמוי‑אינסולין, התומכים בקישורים קליניים בין עמידות לאינסולין למחלת פרקינסון, ומצא שההצטברות מגייסת חלבונים המעורבים בסילוק חלבונים פגומים, כגון משפחת השופרונים 14‑3‑3 ורכיבים ספציפיים של מסלולי דגרדציה תאית.
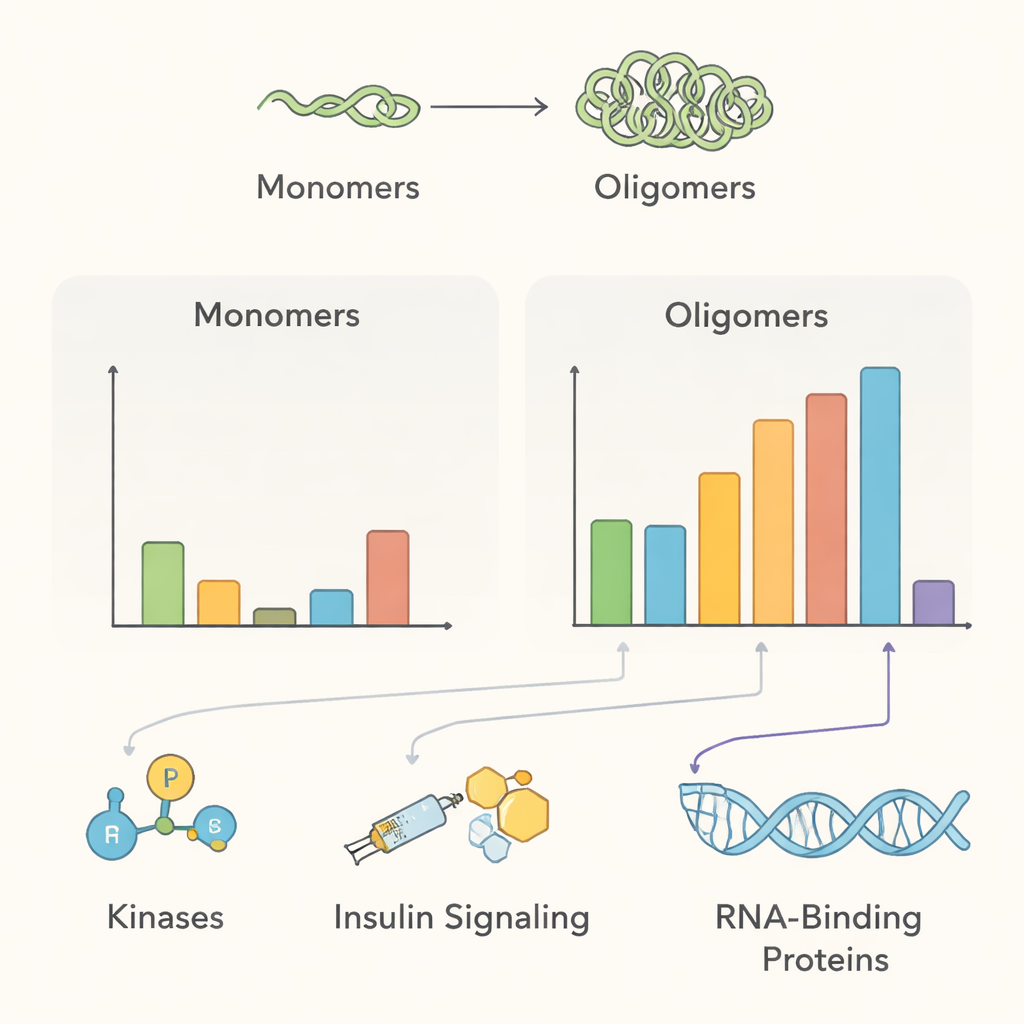
קשרים מפתיעים להפרעות מוחיות אחרות
מעבר למחלת פרקינסון, הנתונים מדגישים קישור מפתיע לאמיאוטרופית לטרלית סקולרוזיס (ALS) ודמנציה פרונטו‑טמפורלית (FTD). חלבון קושר‑RNA בשם FUS, שמזיז מיקום ומצטבר במצבים אלה, הופיע קרוב לאלפא‑סינוקלאין מולטימרי הן בתנאים נורמליים והן בתנאי הצטברות. חלבונים נוספים הקשורים ל‑RNA גם שינו את קירבתם כאשר אלפא‑סינוקלאין הצטבר. ממצאים אלה מעלים אפשרות כי צבירי אלפא‑סינוקלאין קטנים עלולים ללכוד חלבוני‑טיפול ב‑RNA במקום הלא נכון בתוך התאים, וקושרים ביולוגיה של מחלות גוף‑לווי עם זו של ALS ו‑FTD, אם כי אינטראקציות פיזיות ישירות עדיין צריכות להיות מאומתות.
מה משמעות הדבר להבנת המחלה
לקהל הלא‑מומחה, המסקנה העיקרית היא שעבודה זו מספקת "רשימת מגע" שלב‑ראש של חלבונים הנעים עם אלפא‑סינוקלאין כשהוא עובר מסיוע נורמלי להיווצרות גושים מזיקים. המחקר מרמז שאיבוד מערכות יחסים מגנות מסוימות — כמו עם קינאזות ספציפיות או אנזימי בקרת איכות — עשוי להיות חשוב לא פחות מהרכשת שותפים רעילים חדשים. אמנם הניסויים נערכו במודל תאי מפושט ועדיין אינם מוכיחים סיבה ותוצאה, הם מדגישים מועמדים ומסלולים ממשיים לבדיקה עתידית בניורונים וברקמות מוח. בטווח הארוך, מיפוי שכונות החלבון המשתנות האלה עשוי להנחות אסטרטגיות לשיקום אינטראקציות מגנות, תמיכה באיתותים קשורים לאינסולין, או מניעת לכידת חלבוני‑RNA, ובכך להאט את ההתקדמות משינויים מולקולריים תת‑סופריים למחלת גוף‑לווי מתקדמת.
ציטוט: Fernandes, A.R., Owen, A.P., Faroqi, A.H. et al. A split biotin ligase approach reveals proteins associated with oligomeric alpha-synuclein during aggregation. Sci Rep 16, 7270 (2026). https://doi.org/10.1038/s41598-026-37551-6
מילות מפתח: אלפא‑סינוקלאין, מחלת לווי, הצטברות חלבונים, פרוקסימיטי פרוטאומיקה, מחלת פרקינסון