Clear Sky Science · he
מודל למידת עומק שניתן ליישום קליני וכללי לגידולים במדיאסטינום האנטריורי בתמונות CT ממספר מוסדות
מדוע חשוב לזהות גידולים חזה נדירים
רובנו כמעט שלא נשמע את הביטוי «גידול במדיאסטינום האנטריורי» בביקור קליני, בדיוק מפני שממצאים אלה — שלעיתים קשורים לבלוטת התימוס בחזית הלב — נדירים. עם זאת, כשהם מופיעים הם קשים לזיהוי ואף קשים למדידה מדויקת בסריקות CT; משימות אלה בדרך כלל דורשות מומחים במרכזי סרטן גדולים. המחקר בוחן האם מערכת בינה מלאכותית (AI) שאומנה בקפידה יכולה לסייע לרופאים בבתי חולים רבים לזהות ולשרטט באופן אמין את הגידולים העמומים האלה בתמונות CT שגרתיות, וכך לשפר אבחון ותכנון טיפול עבור מטופלים שעלולים להיות מנותקים מהטיפול המתאים.
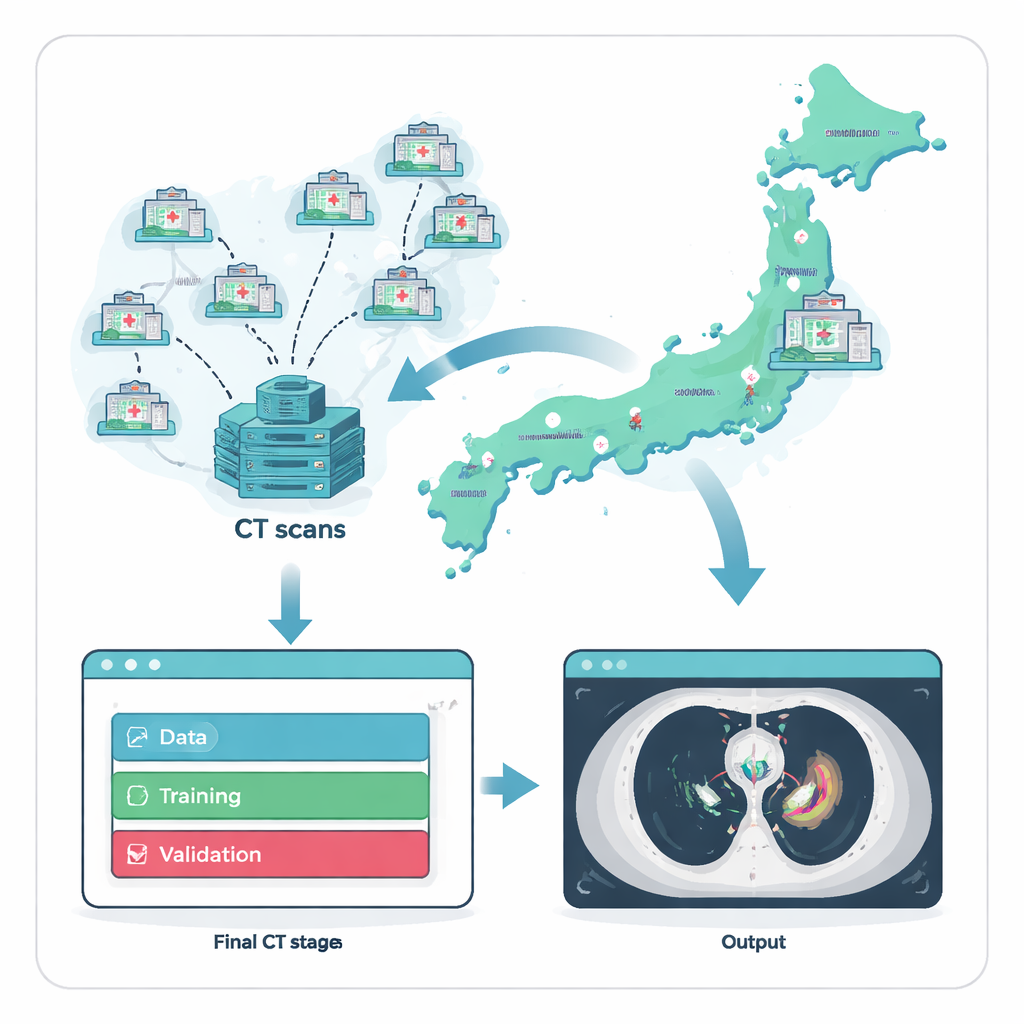
איסוף מקרים נדירים ברחבי המדינה
מכיוון שגידולים במדיאסטינום האנטריורי אינם שכיחים, המכשול הראשון הוא פשוט למצוא מספיק דוגמאות כדי לאמן מערכת AI. החוקרים התמודדו עם זה בשיתוף בית החולים הלאומי לסרטן של יפן ו-135 בתי חולים מפנים ברחבי המדינה. במשך שני עשורים רכשו 711 סריקות חזה ב-CT, כל אחת של מבוגר שאובחן הגידול שלו תחת המיקרוסקופ. כדי להבטיח מבחן הוגן וריאלי, חילקו את הנתונים לשלוש קבוצות: סט אימון גדול, סט כיוונון עדין קטן יותר, וסט מבחן חיצוני נפרד לחלוטין של 164 סריקות שנלקחו מ-121 בתי חולים שלא תרמו תמונות לאימון. ההפרדה המחמירה הזאת מדמה את הביצועים של המערכת כאשר תושם בבתי חולים חדשים שהיא לא ‘‘ראתה’’ בעבר.
הפיכת הסריקות לחומר לימוד מהימן
מודל AI טוב רק כמו הדוגמאות שהוא לומד מהן, ולכן הצוות השקיע רבות בתיוג מומחים. עבור כל סריקת CT, המומחים שרטטו בדיוק את גבולות הגידול בחלק הקדמי של החזה. מנתח חזה או טכנאי רדיולוגיה ציירו את הקווים הראשוניים, ולאחר מכן שני רדיולוגים אבחון מנוסים בדקו אותם. חילוקי דעות הוכרעו בדיון משותף, מה שייצר רפרנס איכותי המשקף כיצד מומחים מפרשים את התמונות במעשה. באמצעות פלטפורמת AI מסחרית ללא קוד, קלינאים — ללא כתיבת קוד מחשב — בנו ולאימנו מודל תלת־ממדי להדמות שרטוטים מומחים אלה, מה שאפשר לצוות הרפואי לכוון ישירות את תהליך הפיתוח.
איך ה-AI רואה גידולים בתלת־ממד
לב המערכת הוא גרסה תלת־ממדית של ארכיטקטורת רשת עצבית ידועה בשם U-Net, שנועדה לנתח נפחי CT שלמים במקום חתכי בודדים. היא מקבלת ערמת תמונות חזה וצופה, עבור כל יחידת נפח זעירה, האם היא שייכת לגידול או לרקמה התקינה, ובאופן אפקטיבי צובעת מסכת תלת־ממד מעל הגידול. במהלך האימון הוצג המודל לסיבובים אקראיים, שינויי קנה מידה וגזירות של התמונות כדי שיהיה חסין לשינויים קלים במיקום המטופל ובהגדרות הסורק. החוקרים לאחר מכן מדדו עד כמה אזורי הגידול החזויים על ידי המודל תואמים את שרטוטי המומחים, באמצעות מדדי חפיפה סטנדרטיים שמעניקים ניקוד גם למיקום גבול מדויק וגם לכיסוי מלא של נפח הגידול.
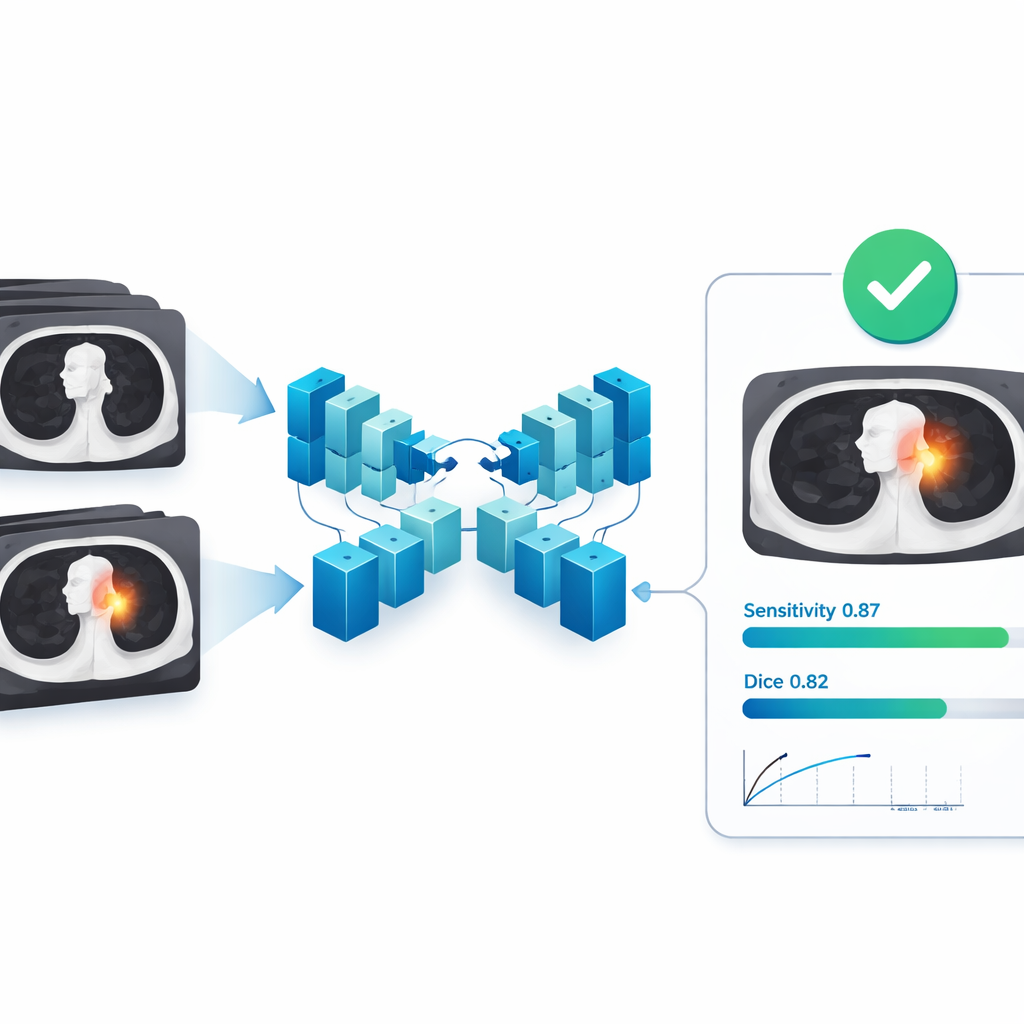
ביצועים במספר בתי חולים וסוגי גידולים
בסט המבחן החיצוני מ-121 בתי חולים עצמאיים, מודל ה-AI הראה התאמה חזקה לסגמנטציות המומחים. בממוצע, מדד החפיפה שלו (Dice) היה 0.82, עם מדד קשור של Intersection over Union בערך 0.72; הדיוק והזיכרון (precision ו-recall) עמדו שניהם סביב 0.82–0.85, כלומר המודל נדיר לסווג רקמה תקינה כגידול ותפס את רוב רקמת הגידול. חשוב מכך, תוצאות אלה החזיקו מעמד מול יצרני סורקי שונים, גדלים וסוגי גידולים שונים, מה שמרמז שהמערכת יכולה להתמודד עם המגוון שנמצא בשלבי הקליניקה הריאלית. כאשר הוערכה כגלאי — בשאלה הפשוטה האם היא מוצאת כל נגע בכלל — המודל הגיע לרגישות של כ-0.87 גם תחת כלל התאמה נוקשה, עם פחות מהתראה שגויה אחת בממוצע לכל סריקה, פרופיל שמושך במיוחד עבור תמיכה בסקרינג לסרטן.
איפה המערכת מסייעת והיכן האדם נשאר קריטי
מבט קרוב על הצלחות וכשלונות חשף דפוס ברור: ה-AI התפקד היטב עם גידולים גדולים ונוטה להתקשות בנגעים קטנים או חלשים מאוד, כשהוא חלקית מפספס אותם או מבלבל מבנים תקינים סמוכים כמו כלי דם או אוספי נוזלים. זה תואם את הניסיון היומיומי ברדיולוגיה, שבו ממצאים זעירים או בעלי ניגוד נמוך הם הקלים ביותר להתעלם מהם. המחברים טוענים שהכלי לכן יש להשתמש בו בסביבה של "אדם-בלולאה". הוא יכול לשמש כקורא ראשון יעיל שמסמן גידולים סבירים ומשרטט את גבולותיהם, מספק נפחים מוכנים למשימות כמו תכנון טיפול וניתוח, בעוד שרדיולוגים ממקדים את תשומת לבם בבדיקת אזורים קטנים, עדינים או מעורפלים.
מה זה אומר למטופלים ולכלים עתידיים
לאדם מן השורה, המסר המרכזי הוא שמערכת AI שאומנה על קבוצת גידולים חזה נדירה אך חמורה יכולה לסייע באופן מהימן לרופאים למצוא ולשרטט את סוגי הסרטן האלה בסריקות CT, אפילו בבתי חולים שלא תרמו נתונים לאימונה. על ידי אספקת מפות גידול תלת־ממדיות מדויקות ושמירה על שיעור התרעות שגויות נמוך, המודל יכול להאיץ אבחון, לתמוך בתכנון קרינתי וכירורגי מדויק יותר, ולספק רשת ביטחון נוספת נגד נגעים שהוחמצו. יחד עם זאת, העבודה מדגישה כי בינה מלאכותית אינה תחליף לשיפוט מומחה — במיוחד עבור הגידולים הקטנים והחלשים ביותר — אלא עוזר מבטיח שהולך ומתחזק ככל שמביאים יחד קלינאים, נתוני דימות ופלטפורמות AI נוחות לשימוש.
ציטוט: Takemura, C., Miyake, M., Kobayashi, K. et al. A clinically applicable and generalizable deep learning model for anterior mediastinal tumors in CT images across multiple institutions. Sci Rep 16, 6774 (2026). https://doi.org/10.1038/s41598-026-37504-z
מילות מפתח: גידולים במדיאסטינום האנטריורי, למידת עומק בהדמיית CT, סגמנטציה של תמונות רפואיות, תמיכה באבחון סרטן, בינה מלאכותית ברדיולוגיה