Clear Sky Science · he
עיצוב ואימונוגניות של Saccharomyces boulardii משוחזרת המפרישה חיסון תת‑יחידה נגד רוטה‑וירוס P2‑VP8
מדוע שמר ידידותי למעי יכול להיות חשוב לבריאות ילדים
רוטה‑וירוס הוא גורם מרכזי לשלשול קשה בילדים קטנים, במיוחד במדינות בעלות הכנסה נמוכה שבהן הגישה לטיפול רפואי מוגבלת. החיסונים הקיימים מצילים חיים רבים אך יעילותם נמוכה יותר בהגדרות אלו, והם דורשים שרשרת קירור מהמפעל עד למרפאה. מחקר זה בוחן סוג שונה מאוד של חיסון: הפיכת שמר פרוביוטי נפוץ למפעל זעיר המפריש חלבון של רוטה‑וירוס במעי, מתוך תקווה לעורר הגנה בצורה יציבה וקלה למתן.
להפוך מיקרואורגניזם מועיל לכלי משלוח חיסון
החוקרים התרכזו ב‑Saccharomyces boulardii, שמר פרוביוטי שכבר משמש למניעה או טיפול בשלשולים. הרעיון שלהם היה להנדס את השמר כך שיפריש קטע מחלבון ממברנה של רוטה‑וירוס, שנקרא VP8, שבו הווירוס משתמש כדי להיצמד לתאי אדם. הם חיברו את VP8 לחלק עוזר קצר של חלבון הידוע כ‑P2, אשר הוכח בעבר כמגביר תגובות חיסוניות, ויצרו חלבון משולב בשם P2‑VP8. מאחר שמדובר רק בקטע קטן ובלתי מדבק של הווירוס, גישה זו משתלבת במסגרת חיסוני ה"תת‑יחידה" שמטרתם להיות בטוחים וקלים יותר לטיפול מאשר חיסוני וירוס מלאים.
תכנון המועמד לחיסון תחילה במחשב
לפני ביצוע ניסויים בחיות, הצוות השתמש במערך כלים ממוחשבים כדי לחזות כיצד חלבון P2‑VP8 יתנהג. הם מיפו אזורים של VP8 שסביר שתאי החיסון יזהו ובדקו אם אזורים אלה צפויים להיות יעילים בקבוצות גנטיות אנושיות שונות. לאחר מכן בנו מודל תלת‑ממדי של P2‑VP8 וסימולציות של אינטראקציה שלו עם TLR3, חיישן על תאי חיסון שמסייע לזהות זיהומים וירליים. הסימולציות הצביעו על כך ש‑P2‑VP8 יציב, מסיס, לא רעיל ובעל יכולת ליצור קשר חזק ומתמשך עם הקולטן החיסוני — כל אלה סימנים מעודדים למועמד חיסון.
הנדסת השמר להפרשת חלבון הרוטה־וירוס
כדי להבטיח שהשמר הפרוביוטי יפיק את החלבון ביעילות, החוקרים כתבו מחדש בקפידה את הגן של P2‑VP8 באמצעות קודונים — "מילים" תלת‑אותיות של DNA — אשר Saccharomyces boulardii קורא בקלות יותר. האופטימיזציה היא כמו לתרגם מתכון לדיאלקט מקומי של השמר כדי שמכונת התרגום שלו תוכל לבצע אותו במהירות ובדיוק. לאחר מכן הכניסו את הגן המותאם לווקטור ביטוי לשמר והפעילו אותו ב‑S. boulardii. בתרבית מעבדתית איששו שהםנדס השמר הפריש חלבון בגודל הצפוי באמצעות שיטות סטנדרטיות של הפרדה חלבונית (SDS‑PAGE) ו‑western blot עם נוגדנים מותאמים אישית, מה שמראה שהפרוביוטיקה יכולה לשמש כיצרן חי של קטע החיסון.
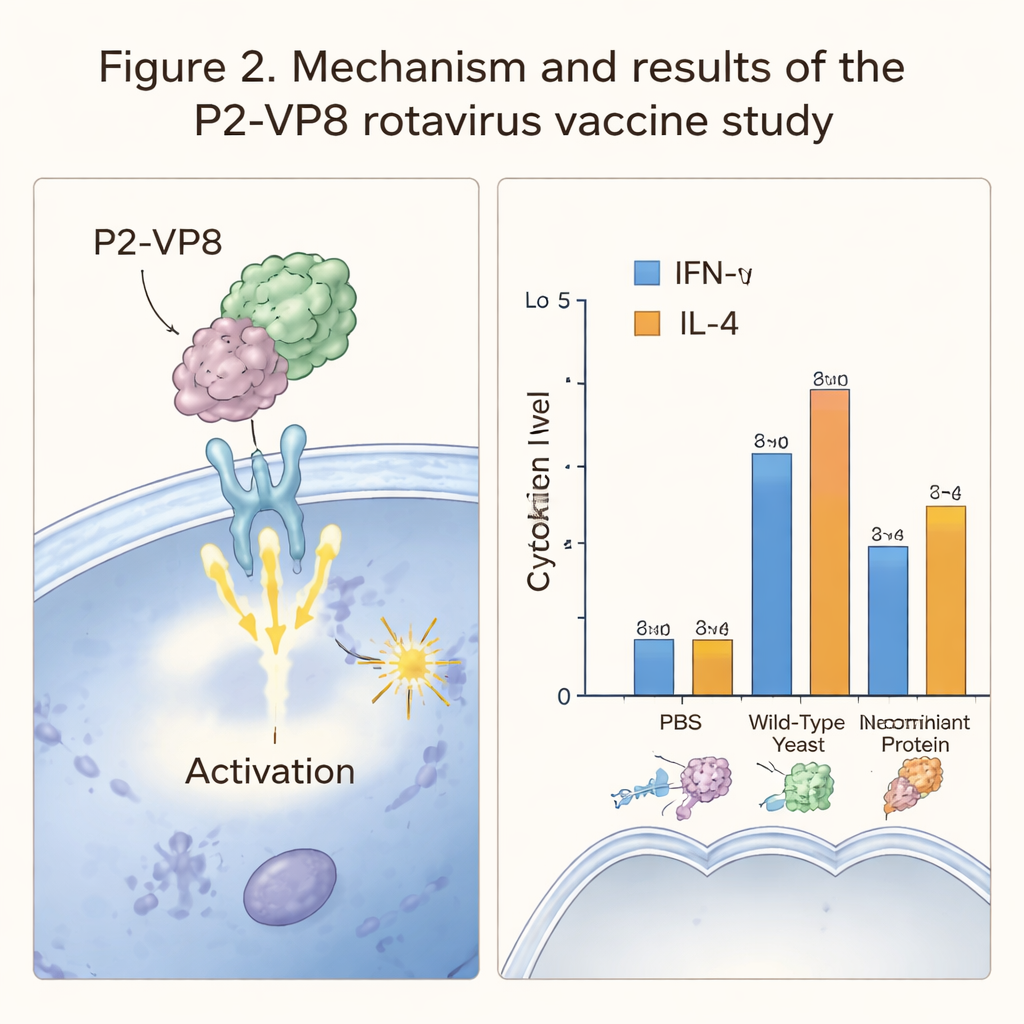
בדיקת תגובות חיסוניות בעכברים
לאחר מכן הצוות בחן כיצד חיסון מבוסס‑שמר מתנהג בחיות חיות. עכברים קיבלו جرعات פיה של השמר המשוחזר במקפסלות לאורך מספר שבועות, בעוד קבוצות השוואה קיבלו שמר רגיל, תמיסת מלח בלבד או חלבון P2‑VP8 מזוכך בהזרקה. לאחר החיסון מדדו החוקרים מולקולות איתות חיסוניות מרכזיות, IFN‑γ ו‑IL‑4, המשקפות סוגים שונים של הפעלה חיסונית. בעכברים שקיבלו את השמר המהונדס או את החלבון המוזרק נצפו רמות גבוהות יותר של ציטוקינים אלו בהשוואה לבעלי החיים בקבוצות הביקורת, מה שמצביע על כך שמערכת החיסון שלהם זיהתה והגיבה לקטע הרוטה‑וירוס. עם זאת, לא נצפו פרוליפרציה חזקה של תאי‑T או רמות נוגדנים עמידות בקבוצת ההאכלה בשמר, מה שמעיד שהתגובה החיסונית למתן פומי הייתה יחסית חלשה.
מה משמעות עבודה זו ומה עוד צריך לתקן
בסך הכל, המחקר מראה שניתן להפוך שמר פרוביוטי למפעל המפריש קטע מוביל של חיסון רוטה‑וירוס ושהמבנה מתנהג כמצופה במבחני מחשב מפורטים. בעכברים, השמר מהונדס עורר פעילות חיסונית מסוימת אך לא ייצר תגובות חזקות ובעלות אופיין מגן הנדרשות לחיסון מצליח. עבור קורא שאינו מומחה, המסקנה היא שהקונספט — שימוש מיקרואורגניזם ידידותי כחיסון אכיל — נראה ישים טכנית, אך העיצוב הנוכחי עדיין אינו חזק דיו. עבודות עתידיות יצטרכו לשפר את עיצוב החלבון, המינון ואסטרטגית המשלוח, ולכלול ניסויים ישירים לבחינת ההגנה מפני זיהום רוטה‑וירוס לפני שניתן יהיה לקדם גישה כזו לשימוש במציאות.
ציטוט: Farhani, I., Yamchi, A., Nikoo, H.R. et al. Design and immunogenicity of a recombinant Saccharomyces boulardii secreting the P2-VP8 subunit rotavirus vaccine. Sci Rep 16, 6932 (2026). https://doi.org/10.1038/s41598-026-37374-5
מילות מפתח: חיסון נגד רוטה‑וירוס, שמר פרוביוטי, חיסוני תת‑יחידה, חיסון ושאי פה, עיצוב חיסון