Clear Sky Science · he
אפופטוזה יעילה דרך שברים דו-גדיליים ב‑DNA בתאי אפיתל אנושיים המוענקים על‑ידי השפעה לא‑תרמית של גלי טרהרץ רחבי פס בעוצמה גבוהה
אור חדש על הריגת תאי סרטן
טיפולים בסרטן לעתים קרובות מאזנים על חבל דק: הם חייבים להשמיד את התאים הממאירים מבלי להזיק במידה רבה לרקמות בריאות או למערכת החיסון. המחקר הזה בוחן כלי יוצא דופן למשימה זו — פולסים חזקים של גלי טרהרץ (THz), סוג של אור בלתי נראה שנמצא בין מיקרוגל לאינפרא‑אדום. החוקרים מראים שפולסים ברוחב פס גבוה ובעוצמה שדה מותאמת יכולים להפעיל בתאים ממאירים מנגנון של "התאבדות" מבוקרת (אפופטוזה), בלי לבשל את הרקמה או לעורר מוות תאיים אלים שגורם לדלקת.
מדוע מוות תאי עדין חשוב
טיפולים אנטי‑סרטניים רבים דוחפים תאים לכיוון מוות, אך לעתים קרובות זה קורה במחיר של נזקים נלווים. תרופות וסוכנים ביולוגיים עלולים לאבד את יעילותם כשהגידול מפתח עמידות, והם עלולים גם לדכדך את המערכת החיסונית. שיטות פיזיקליות כמו קרינה X, רדיואקטיביות או השמדה בחום עלולות לפגוע ברקמה הבריאה הסמוכה, ולעתים קרובות לגרום לנקרוזה — צורה אלימה של מוות תאי שמעוררת דלקת וכאב. שיטה שמובילה במקום זאת לאפופטוזה, תהליך מסודר שבו התאים מפרקים את עצמם בשקט, יכולה להציע דרך פחות טראומטית להקטין גידולים, במיוחד כאלה קרובים לעור.
גלי טרהרץ פוגשים תאי סרטן השד
הצוות התרכז בתאי סרטן השד האנושיים (MCF‑7), סוג של תאי אפיתל הנפוץ במחקרים מעבדתיים. הם חשפו תאים אלה לפולסים רחבי פס של THz בעוצמה שדה גבוהה למשך עד ארבע שעות, תוך שמירה על טמפרטורת גוף תקינה. עוצמות השדה הגיעו למיליוני וולטים לסנטימטר — גבוהות בהרבה מהשימוש היומיומי. בתנאים אלה, החלק של התאים שעברו אפופטוזה עלה בעקביות עם משך החשיפה. בעוצמת ה‑THz הגבוהה ביותר שנבדקה נכנסו כמעט 99% מהתאים למצב אפופטוטי, בעוד שפחות מ‑1% מתו מנקרוזה. גל רחב, נקי כזה של מוות מתוכנת מרמז שהפולסים של THz עושים יותר מאשר חימום התאים.
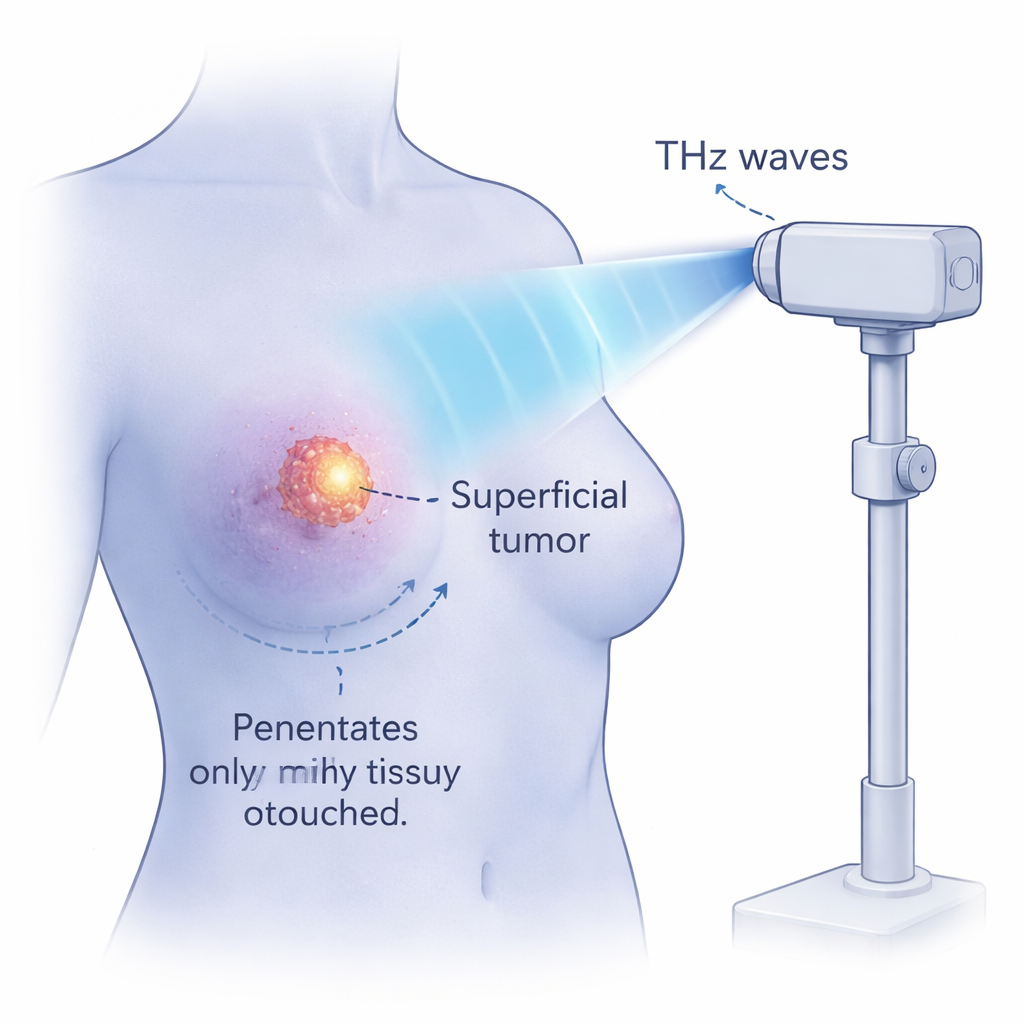
השפעות לא‑חימומיות ומגבלות טמפרטורה בטוחות
מכיוון שמים סופגים קרינה בתחום ה‑THz בעוצמה, החשש הברור הוא חימום לא מכוון. המדענים השתמשו בהדמיה תרמית כדי לעקוב אחרי שינויים בטמפרטורה במהלך ההארה. גם אחרי ארבע שעות בעוצמה מתונה, התאים התחממו רק בכ‑3 °C, והנקרוזה נותרה מתחת ל‑4%. ניסויי בקרה נפרדים שבהם תאים הוחממו למשך ארבע שעות הראו שטמפרטורות מתחת ל‑41 °C יצרו כמעט אפס מוות, בעוד שקפיצה חדה בנקרוזה התרחשה מעל 43 °C. אפילו בהגדרות ה‑THz החזקות ביותר, החוקרים שמרו על טמפרטורות התאים באזור של עד 43 °C וראו כמעט אפופטוזה מלאה עם נקרוזה מינימלית. בהורדת שיעור החזרה של הפולסים הראו שהם יכולים לשלוט בטמפרטורה תוך שמירה על השפעה אנטי‑גידולית חזקה, מה שמדגיש שמנגנון לא‑תרמי פועל כאן.
רעידות שמפרקות את ה‑DNA והפעלת גנים של מוות
כדי למצוא את המנגנון, הקבוצה בחנה את פנים התאים. במיקרוסקופ אלקטרוני, תאים שטופלו ב‑THz הראו סימנים מוקדמים קלאסיים של אפופטוזה: דחיסות בחומר הגנטי, שינויים בגרעינים וממברנות חיצוניות שלמות. באמצעות סמן פלורוסנטי בשם γ‑H2AX גילו שברי דו‑גדיל נרחבים ב‑DNA — נזק בשכיחות גבוהה הרבה יותר בתאים מוארים לעומת בקרים לא מטופלים או מחוממים בעדינות. דפוס הנזק עקב אחר פרופיל העוצמה של קרן ה‑THz והתחזק כלפי המרכז שלה. ניתוחי גנים וחלבונים חשפו כי אוסף מולקולות מגיבות למתח ונזק, כגון GADD45B ו‑c‑Jun, הופעלו בחוזקה, בעוד ששחקנים מוכרים במסלולי מוות תאיים מסורתיים, כולל p53 והרבה קזפאזות, לא שינויו משמעותית. המחברים מציעים שעוצמות ה‑THz הגבוהות עלולות להניע תהודות רטט חזקות ב‑DNA, להעמיס פיזית ולשבור את הסליל הכפול ואז להפעיל מסלול אפופטוטי מובהק שתלוי פחות ב‑p53 ובקזפאזות.
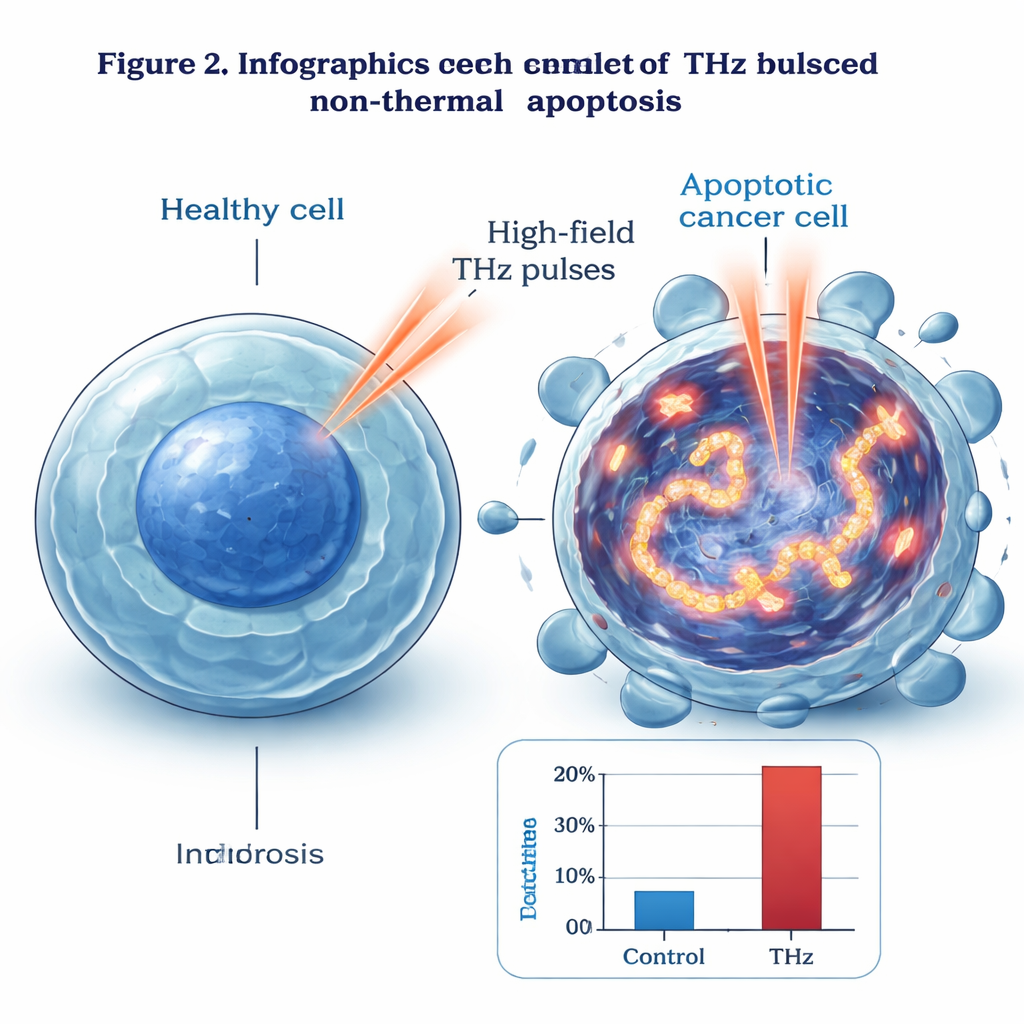
מצלחת מעבדה לטיפולים עתידיים
בעוד שהניסויים בוצעו בתרביות תאים, הם מרמזים על סגנון חדש של טיפול פיזיקלי בסרטן. גלי THz בעוצמה גבוהה נראים כיכול לחדור כמה מילימטרים לרקמה לחה — מספיק כדי להגיע לגידולים שטחיים — אך מאבדים מעוצמתם במהירות, מה שעשוי להחיות איברים עמוקים. מאחר שההשפעה היא בעיקר לא‑תרמית, היא עשויה, בהיגיון, להרוג תאים סרטניים שכבה אחר שכבה ללא קילוף רקמה סביבתית או עוררות דלקת חזקה. יש עוד עבודה רבה: מנגנון "התהודה" המוצע עבור ה‑DNA צריך אישור, יש לבדוק בקפידה את הבטיחות לתאים נורמליים, ונדרשים ניסויים בחיות ובקליניקה. עם זאת, המחקר הזה פותח דלת לרעיון שפולסים של אור מהונדסים בקפידה, המותאמים לתנועות הטבעיות של מולקולות ביולוגיות, עשויים בעתיד להציע דרך מדויקת ויחסית עדינה להשמדת סוגים מסוימים של סרטן.
ציטוט: Zhou, H., Wei, X., Peng, XY. et al. Efficient apoptosis via double-strand breaks of DNA in human epithelial cells induced by non-thermal effect of high-field broadband terahertz waves. Sci Rep 16, 6163 (2026). https://doi.org/10.1038/s41598-026-37373-6
מילות מפתח: טיפול בסרטן בעזרת טרהרץ, אפופטוזה לא‑תרמית, שברים דו‑גדיליים ב‑DNA, תאי סרטן השד, השמדת גידול פיזיקלית