Clear Sky Science · he
מיקוד בציר Akt–EphA2 ובדבקות תא–תא מעלה את הרגישות לאנואקיס בתאי סרטן
מדוע תאים סרטניים חופשיים חשובים
כשתאים סרטניים נפרדים מגידול ונעים דרך זרם הדם, הם בדרך‑כלל אמורים למות כי הם מאבדים את האחיזה לרקמה הסובבת. מנגנון הבטיחות הזה, הנקרא מוות תאי עקב ניתוק, מגן על רקמות בריאות מפיתוח במקום שאינו מתאים. תאים סרטניים גרורתיים, עם זאת, לעתים קרובות מפתחים יכולת להתעלם מהמנגנון הזה ולהישאר בחיים בזמן ציפה, מה שמקל עליהם לזרוע גידולים חדשים. במחקר זה נשאלת שאלה שנראית פשוטה אך חשובה: אם נשיב תחושת מגע מכנית מרכזית בתאי סרטן של השד האגרסיביים, האם נוכל להכריח את התאים הנודדים האלה למות, ואם לא — אילו טריקים חלופיים הם משתמשים כדי לשרוד?
החייאת תחושת המגע האבודה
תאים בודקים באופן קבוע עד כמה הסביבה שלהם קשה, וגוררים את המבנים שמעגנים אותם. ברקמה בריאה, אובדן מגע או הנחיתה על משטח רך מאוד נוטים לעורר השמדה עצמית. החלבון Tropomyosin 2.1 (Tpm2.1) הוא חלק חשוב במכונת המתח הפנימית הזו ולעתים קרובות חסר או מופחת בתאים סרטניים. החוקרים השתמשו בקו תאים של סרטן השד הגרורתי שנחקר רבות ומהונדסו כך שיביע יותר Tpm2.1, ובכך שיקמו חלק ניכר מחישת הקשיות. כאשר תאים המותאמים הללו הוכפו לגדול בכלים מיוחדים שאינם מאפשרים אחיזה, הם עברו יותר מוות תאי, גדלו לאט יותר ונעו פחות מאשר תאי סרטן לא מותאמים. עם זאת, אפילו לאחר כמה ימים בציפה, כ‑70% מהתאים שמביעים Tpm2.1 עדיין היו בחיים, מה שמרמז שהחייאת תחושת המגע לבדה אינה פותרת את הבעיה במלואה.
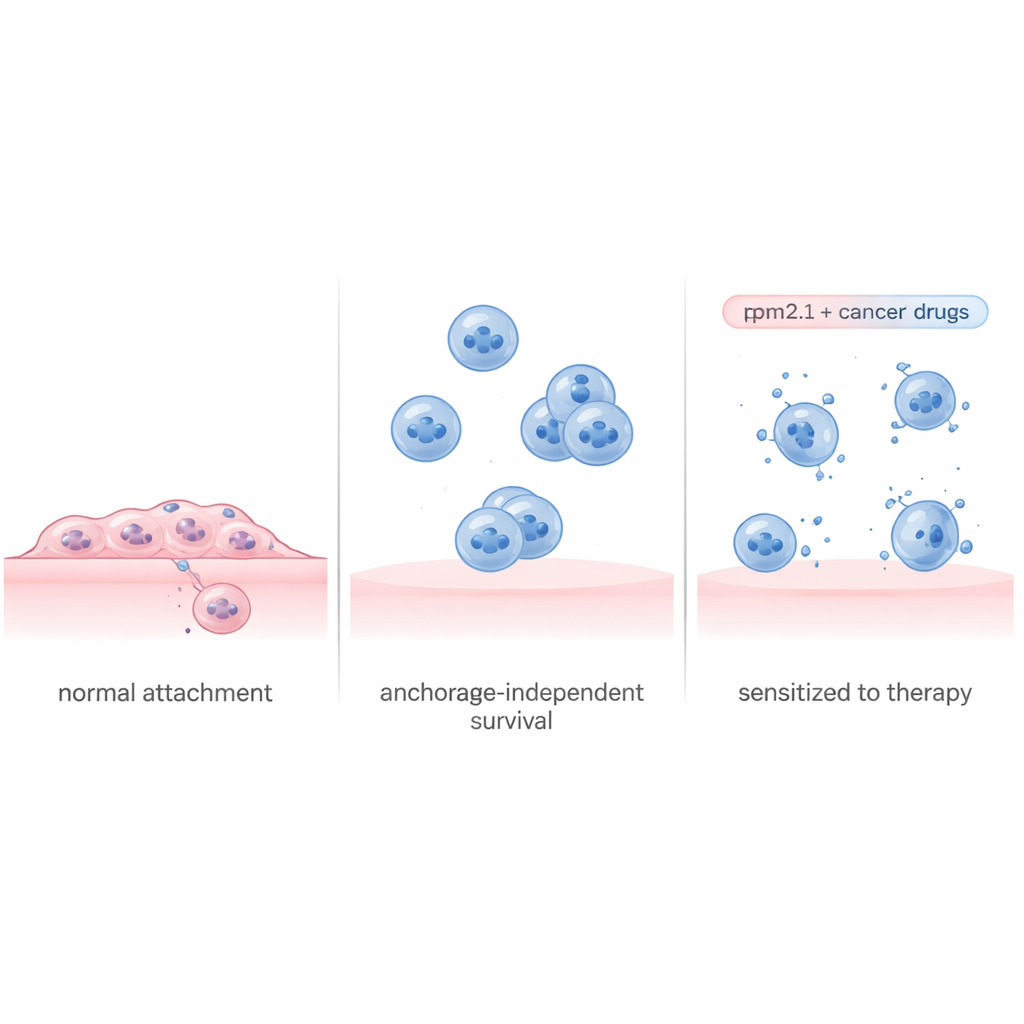
קריאת ספר השורדות של תאי הסרטן
כדי להבין מדוע חלק מהתאים מתו בעוד אחרים שרדו, הקבוצה הפרידה את התאים הצפים שמביעים Tpm2.1 לשתי קבוצות: אלה שהראו סימנים מוקדמים של מוות תאי ואלה שנראו בריאים. הם מדדו אילו גנים הופעלו או כובו בכל קבוצה על פני ארבעה ימים. התאים המתים הציגו כיבוי רחב של תכניות מעורבות בחלוקה תאית, תיקון DNA ודבקות, לצד אותות שיחרוּר שנראו כמו דרך ללא מוצא להשמדה עצמית. לעומת זאת, התאים ששרדו הפעילו תכנית הישרדות מתואמת. זמן קצר אחרי הניתוק הם הפעילו מסלולים דלקתיים ובקשורים למערכת החיסון ובהמשך הגבירו מסלולים מרכזיים לצמיחה ולהישרדות, כולל מסלול ידוע סביב החלבון Akt. במקביל חיזקו במידה רבה גנים המסייעים לתאים להיצמד זה לזה, מה שאיפשר להם ליצור אשכולות מגן גם ללא אחיזה למטריצת הרקמה הסובבת.
חוזק במספרים: כיצד אשכולות תאים מתנגדים למוות
מכיוון שנתוני הגנים הצביעו על עלייה בדבקות תא–תא, החוקרים בדקו האם צפיפות פשוטה יכולה לסייע לתאים לשרוד בציפה. כאשר תאי Tpm2.1 גדלו בצפיפות גבוהה, שבה היו קלות להיווצרות אשכולות, מתים פחות תאים מאשר כאשר שמרו על צפיפות נמוכה. מולקולת דבקות אחת, ICAM1, בלטה כבעלת רמות גבוהות במיוחד בתאים ששרדו והיא כבר ידועה בסיוע להיווצרות אשכולות של תאי גידול נודדים ולהיקבע ברקמות מרוחקות. חסימת ICAM1 בעזרת מעכב מולקולרי קטן גרמה ליותר מוות של תאי Tpm2.1 בציפה, בעוד שהייתה לה השפעה מועטה בתרביות רגילות מחוברות. ממצאים אלה תומכים ברעיון שבעוד שמערכות המכניקה הפנימיות שלהם שוקמו חלקית, תאים סרטניים עדיין יכולים להימנע מהמוות על‑ידי אחיזה זה בזה במקום באורגניזציה הסובבת.
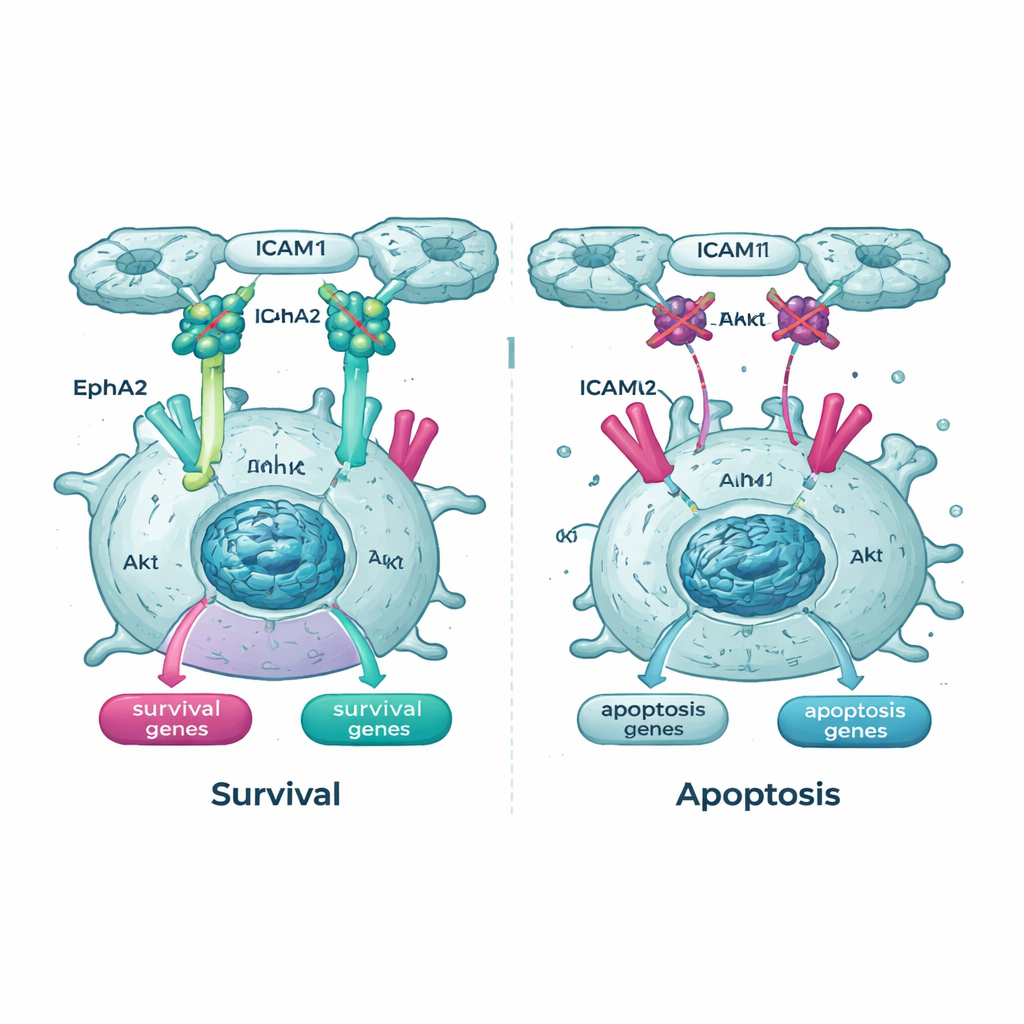
כיבוי קווי חיים מרכזיים בתוך התא
סקרי הגנום גם הדגישו את מסלול Akt ואחד משותפיו, קולטן בשם EphA2, כקווי חיים חשובים לתאים סרטניים צפים. בתאי Tpm2.1, הצורה הפעילה ומופשרת‑הפוספט של Akt הייתה נמוכה יותר בציפה בהשוואה לתאים ביקורתיים, ורמות ופעילות EphA2 פחתו אף הן. כאשר הצוות טיפל בתאים בתרכובות החוסמות את Akt או את EphA2, גם התאים הרגילים וגם תאי Tpm2.1 הפכו לנטויים יותר למות בציפה. ראוי לציון שהתאים ששקמו את חישת הקשיות היו רגישים במיוחד לתרופות אלה לאורך זמן, מה שמרמז שברגע שבדיקות הבטיחות המכניות שלהם משוחזרות חלקית, הם נסמכים יותר על אותות ההישרדות שנותרו.
הפיכת מצב מוכוון לחולשה קטלנית
ללא‑מומחה, המסר המרכזי הוא שתיקון ממסר בטיחות אחד שבור בתאים סרטניים — היכולת שלהם להרגיש ולהגיב לאובדן מגע — הכרחי אך לא מספיק כדי לגרום להם להשמדה עצמית. התאים ששרדו עשו זאת על‑ידי התאגדות מחדש והפניית התקשורת הפנימית שלהם דרך מסלולי צמיחה והישרדות חלופיים. עבודה זו מראה ששיקום חישת הקשיות בעזרת Tpm2.1 מכניס תאי סרטן שד גרורתיים למצב "מוכוון" שבו הם קרובים יותר למות אך עדיין לא מחויבים לו. על‑ידי חסימת ציר Akt–EphA2 והפרעה לדבקות תא–תא דרך ICAM1, חוקרים יכולים לדחוף את התאים המוכוונים הללו מעבר לקצה ולהגביר במידה רבה את המוות התאי המושרה על‑ידי ניתוק. במונחים מעשיים, המחקר משרטט אסטרטגיה לטיפולים משולבים עתידיים שמטרתם להשמיד תאים גידוליים צפים לפני שיכולים לזרוע גרורות חדשות.
ציטוט: Vivante, A.G., Dwivedi, N., Sheetz, M.P. et al. Targeting the Akt–EphA2 axis and cell–cell adhesion enhances anoikis sensitivity in cancer cells. Sci Rep 16, 6197 (2026). https://doi.org/10.1038/s41598-026-37327-y
מילות מפתח: גרורת סרטן השד, דבקות תאית, אנואקיס, אותות Akt, חישה של קשיות