Clear Sky Science · he
הדמיית מולקולות ביולוגיות בין-תאיות באמצעות חיישני חלבון פלואורסצנטי עם עוגנים ליפיד-PEG
צפייה בתקשורת התאית בזמן אמת
המוח והגוף שלנו נשענים על שיחה כימית מתמדת בין תאים. יונים ונוירו-מוליכים מעבירים מסרים דרך רווחים זעירים, אבל אותות מהירים וחולפים אלה קשים לצפייה בלי להפריע להם. מחקר זה מציג שיטה פשוטה ל"צביעת" תאים חיים בחיישנים זוהרים הנצמדים לפני השטח החיצוני שלהם, ומאפשרת למדענים לצפות במסרים אלה — במיוחד יוני אשלגן והנוירו-מוליך גלוטמט — בשידור חי ובפרטיות. 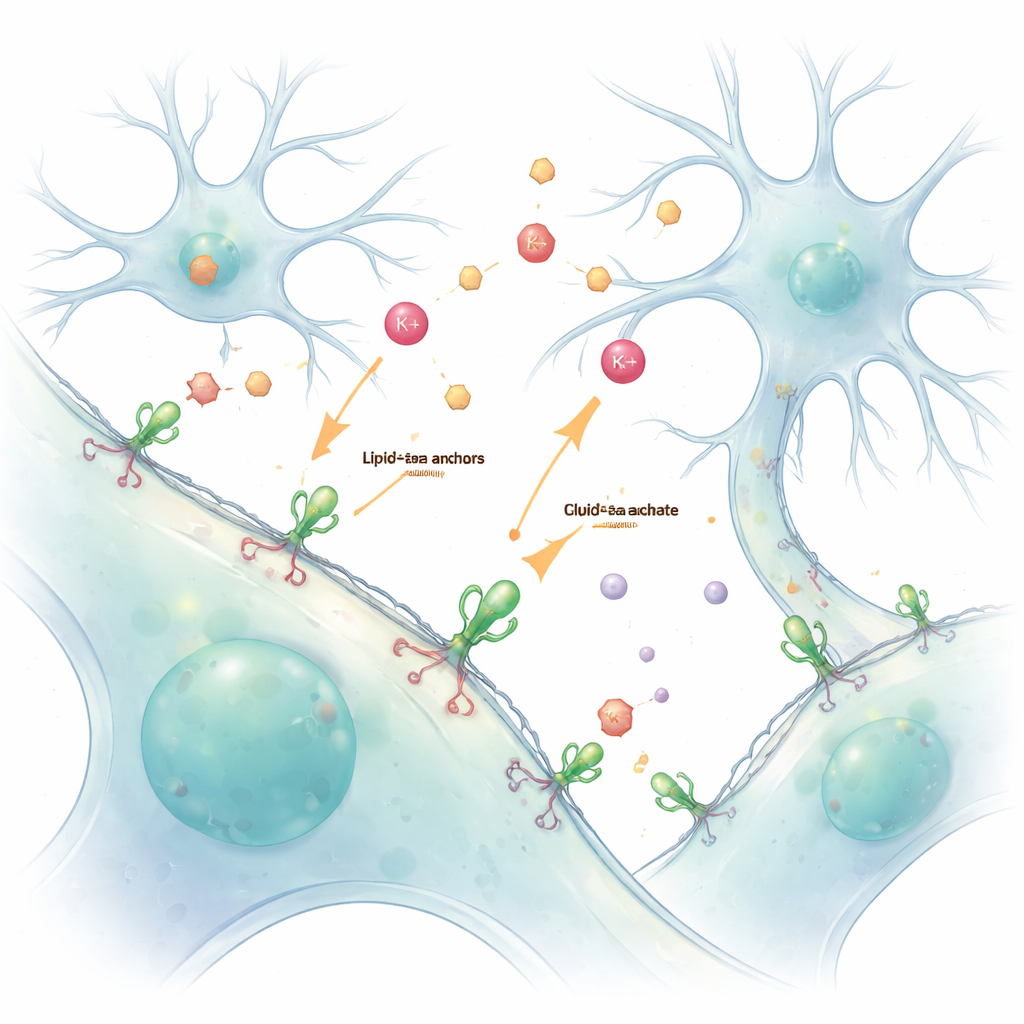
דרך חדשה לתייג את פני התא
באופן מסורתי חוקרים מהנדסים תאים לייצור חיישני חלבון פלואורסצנטי באמצעות ה-DNA שלהם. גישה זו, למרות שהיא עוצמתית, לעתים יוצרת מיקום לא נכון של החיישנים בתוך התא, ומקשה להפריד בין מה שקורה בפנים לבין מה שקורה מבחוץ. המחברים פתרו זאת באמצעות יד כימית שנקראת עוגן ליפיד–PEG. קצה אחד של המולקולה נשזר בממברנה החיצונית, ואילו הקצה השני מקושר כימית לחיישן חלבוני פלואורסצנטי. כשחיישנים מוכנים אלה מתווספים פשוט לתאים חיים, הם מצפים באופן ספונטני את המשטח החיצוני ויוצרים שכבה זוהרת ויציבה שמדווחת על מה שמתרחש בנוזל שמסביב.
הפיכת אשלגן וגלוטמט לאור
הצוות התאים שני חיישנים פלואורסצנטיים קיימים: GINKO2, המשיב ליוני אשלגן, ו-R-iGluSnFR1, המשיב לגלוטמט. הם זיכו חלבונים אלה מבקטריה ואז צרפו אליהם את עוגני הליפיד–PEG. בתאים אנושיים בתרבית, חיישן האשלגן המעוגן יצר קו מתאר חלק לאורך פני התא ובהירה שלו גדלה בכל פעם שאשלגן חוץ-תאי עלה, ואז דמתה כשהרמות ירדו. חשיבות הדבר היא שהתכונות הפלואורסצנטיות והרגישות שלו תואמו במידה רבה לחיישן המקורי ללא שינוי בניסויי מבחנה, מה שמראה שעיגון לא הפחית את הביצועים. אותו המצב התקיים עבור חיישן הגלוטמט, שנשאר רגיש לאחר העיגון והדגיש באופן ברור את הגלוטמט במרחב שמיד מחוץ לתאים.
האזנה לנוירונים בתרביות ובחתכים
לאחר מכן החוקרים עברו לתאי עצב מההיפוקמפוס של עכבר, אזור מוח חשוב ללמידה ולזיכרון. הם ציפו נוירונים אלו בחיישן גלוטמט מעוגן בליפיד–PEG וטעינו את פנים אותם תאים בצביעה קלציום נפרדת המדווחת על פעילות חשמלית. באמצעות מיקרוסקופיה של החזרה טוטאלית פנימית הם יכלו לצפות במבזקי אדום של גלוטמט על פני התא בעוד שהאותות הירוקים בתוך התאים דיווחו על ירי. תצוגת צבע כפול זו הראתה שהחיישנים המעוגנים יכולים לעקוב אחרי שחרור ספונטני של נוירו-מוליך ללא כל שינויים גנטיים בתאים עצמם.
מיפוי גלים כימיים ברקמת המוח
בהמשך הצוות בדק את השיטה בחתכי מוח חדים, אשר שומרים על החיבורים הטבעיים של ההיפוקמפוס. הם יישמו את חיישן האשלגן המעוגן על חתכים וגרו סיבים עצביים חשמלית. החיישן המעוגן הפיק עליות פלואורסצנטיות ברורות וחוזרות לאחר כל גירוי, בעוד שחיישנים שאינם מעוגנים התפזרו במהירות ונתנו אותות חלשים וחסרי יציבות. באמצעות אמבטיית חתכים בתמיסות עם רמות אשלגן ידועות, ותיקון לנצנוץ החלש של הרקמה עצמה, המחברים בנו עקומת כיול ואמדו ריכוזי אשלגן חוץ-תאיים בפועל. רמות בסיס היו כ-2.5 מילימול ועלו לכ-3.4 מילימול בגירוי מתון, בהתאמה למדידות אלקטרודות קלאסיות. חיישנים מעוגנים גם לאשלגן וגם לגלוטמט חשפו כיצד האותות הללו מתפשטים באופן שונה: שינויים בגלוטמט נשארו קרובים לסינפסות פעילות, בעוד עליות באשלגן התפרשו למרחקים של מאות מיקרומטרים, מרמזות על השפעות רחבות יותר על סיכון רשת הפעילות.
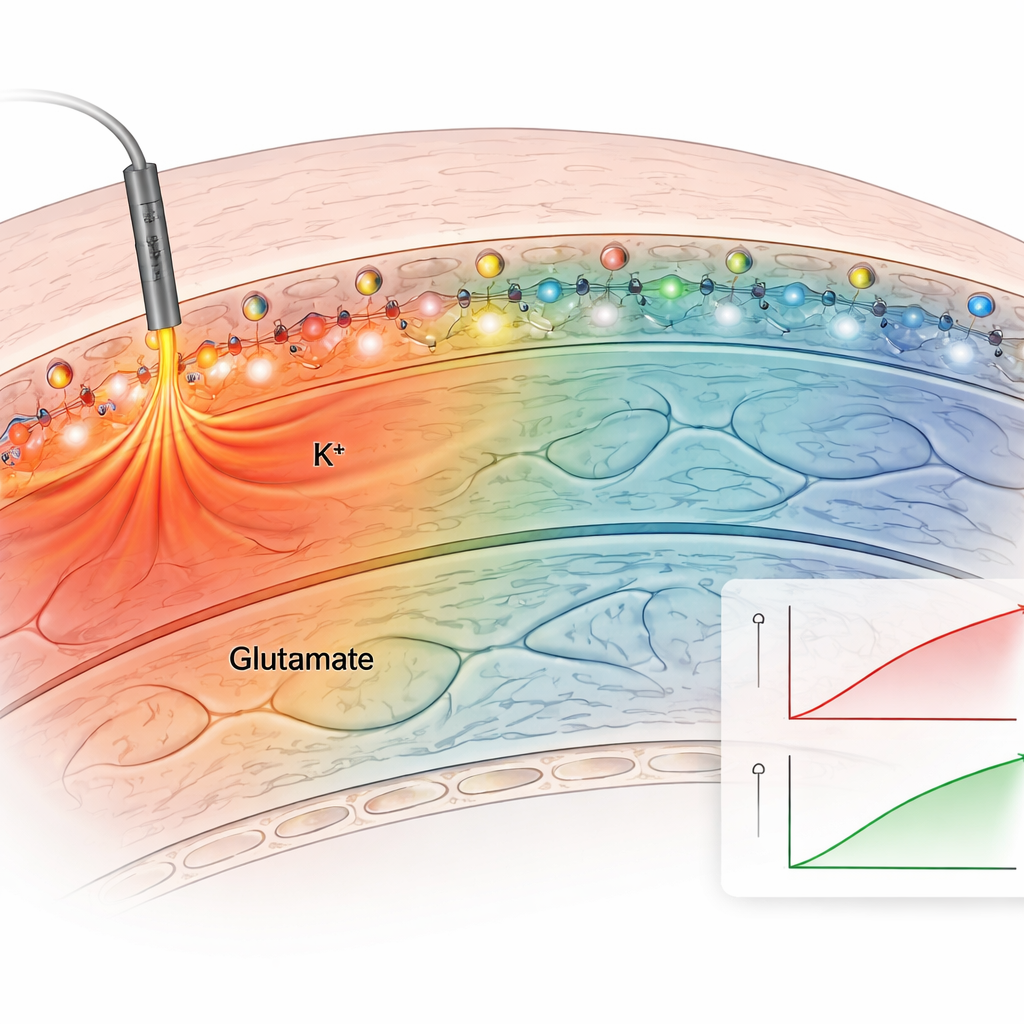
חקר אופן ניקוי ויצירת האותות במוח
מכיוון שהחיישנים קבועים על פני התא, המחברים יכלו לפרק אילו תהליכים מעצבים גלים חוץ-תאיים אלה. חסימת משאבות גלוטמט, שברגיל אוספות גלוטמט, גרמה לחיישן הגלוטמט המעוגן להראות אותות גדולים וארוכי-שנות, ואישרה שלוקל uptake מקומי מגביל את התפשטות הגלוטמט. חסימת קולטני גלוטמט מסוג AMPA הקטינה הן תגובות חשמליות והן אותות אשלגן, מה שמעיד שרוב עליית האשלגן נובעת מנוירונים פוסט-סינפטיים המופעלים על ידי קלט סינפטי. חסימת תעלות נתרן בעזרת טטרודוטוקסין כמעט ביטלה את שינויי האשלגן, וקשרה אותם ישירות לפוטנציאלי פעולה. יחד, ניסויים אלה ממחישים כיצד חיישנים מעוגנים יכולים להפוך כימיה מורכבת ומופצת לסרטים ומפות אינטואיטיביים.
מדוע הדבר חשוב למחקר המוח העתידי
עבור לא-מומחים, המסר המרכזי הוא שעבודה זו מציעה דרך מהירה ולא-גנטית לצפות תאים ורקמות חיים עם מדווחים מולקולריים רגישים מאוד. במקום לשנות גנטית כל סוג תא, מדענים יכולים להוסיף חלבוני חיישן מוכנים מבחוץ ולדמות מיידית כיצד יונים ונוירו-מוליכים משתנים בזמן אמת על פני התא. גישה זו משפרת שליטה, חזרתיות ודיוק מרחבי תוך הימנעות מאתגרי העברת גנים, במיוחד בהכנות עדינות כגון חתכי מוח חדים. ככל שיפותחו חיישנים פלואורסצנטיים נוספים לחומרים שונים, אסטרטגיית העיגון בליפיד–PEG עשויה להפוך לכלי נפוץ לצפייה בשפה הכימית של תאים ברחבי הגוף.
ציטוט: Mita, M., Kiyosue, K. & Tani, T. Imaging intercellular biomolecules by using fluorescent protein indicators with lipid-PEG anchors. Sci Rep 16, 6964 (2026). https://doi.org/10.1038/s41598-026-37240-4
מילות מפתח: סיגנלינג חוץ-תאי, ביו-חיישנים פלואורסצנטיים, הדמיית גלוטמט, דינמיקת אשלגן, נוירונים של ההיפוקמפוס