Clear Sky Science · he
אפיוניה מבנית של קשירת מתכות בטרנספראזית הסולפטור הטירוזינית האנושית TPST2
למה יוני מתכת זעירים חשובים לתקשורת תאית
בתוך תאי הגוף שלנו, מכונות מולקולריות רבות ומצומצמות מותחות ומתאמות באופן שקט כיצד רקמות מתפתחות, הורמונים פועלים ותאי חיסון מתקשרים. אחת מהן, אנזים בשם TPST2, מוסיפה תג סולפט קטן לחלבונים מסוימים כשהם עוברים דרך מרכז המשלוחים של התא — הגולג'י. מחקר זה מגלה כיצד יוני מתכת פשוטים כמו נתרן ומנגן מסייעים ל-TPST2 לתפקד באופן יעיל יותר על ידי הקשחת אזורים מסוימים במבנה שלו — תובנה שעשויה לקשר בין מאזן המינרלים בתא לסרטן ומחלות הקשורות להורמונים. 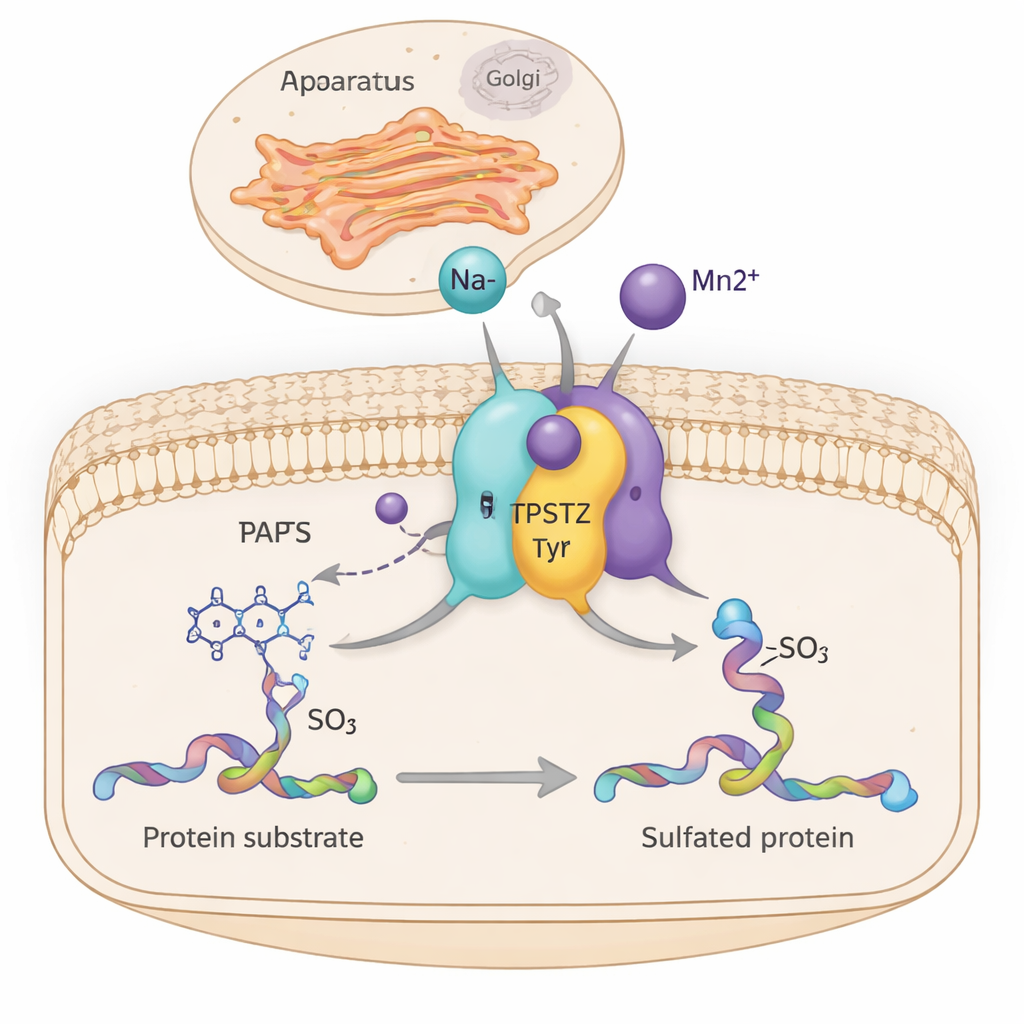
חלבון שמקשט חלבונים אחרים
TPST2 שייך למשפחה של אנזימים המבצעים "סולפטציה של טירוזין", שינוי כימי שמתווסף לשיירי טירוזין מסוימים בחלבונים. חלבונים מסולפטים אלה ממלאים תפקידים מרכזיים מחוץ לתא, ומשפיעים על קרישת הדם, תנועת תאי דם לבנים, קשירה של הורמונים לקולטן ואפילו על דרכי כניסת וירוסים לתאים. בבני אדם יש שני אנזימים עיקריים המבצעים סולפטציה, TPST1 ו-TPST2, שהם ממוקמים בממברנת הגולג'י ומייצרים את השינוי כאשר החלבונים מוכנים לייצוא. ניסויים בעכברים מראים שאובדן TPST2 מופרע בייצור הורמון בלוטת התריס, מעכב גדילה וגורם לעקרות זכרית, מה שמדגיש את חשיבותו לפיזיולוגיה תקינה.
קישורים לסרטן ולבריחה מהחיסון
מחקרים עדכניים קישרו ישירות את TPST2 למחלה. במלנומה, TPST2 מסלף רכיב של קולטן האינטרפרון באופן שמחליש איתות חיסוני, וחסימת TPST2 מחזקת את ההשפעה של טיפולי חיסון שמטרתם PD-1. בסרטן הלבלב, מסלול תלוי-TPST2 מסייע לייצוב חלבון (integrin β4) המקדם גדילת גידול והתפשטות. עיכוב TPST2 במודלים אלה מאט חלוקה וחדירה של תאי סרטן. מאחר ש-TPST2 פועל על חלבונים במעטפת התא, הוא משנה ביעילות את האופן שבו תאים חשים ומגיבים לסביבתם, מה שהופך אותו למטרה מבטיחה לפיתוח תרופות חדשות.
מציאת "מתגי ההפעלה" המטאליים
ביוכימאים ידעו זמן רב ש-TPST2 הופך פעיל בהרבה בנוכחות מתכות דו-ערכיות כגון מנגן (Mn²⁺), אך הסיבה המבנית לכך הייתה לא ברורה. במחקר זה ייצרו החוקרים את הליבה הקטליטית של TPST2 האנושי וגבישו אותה יחד עם תוצרי תגובה ובאחד משני יונים: נתרן (Na⁺) או מנגן. באמצעות קריסטלוגרפיית קרני X ברזולוציה גבוהה הם מצאו שתי כיסי קשירת מתכת קטנים בתוך האנזים, כל אחד עם סידור מסודר של האטומים בסידור ששי-צדדי (אוקטהדרלי). על ידי כוונון אורך הגל של קרני ה-X לחתימות הייחודיות של מתכות שונות, אישרו החוקרים ש-Mn²⁺ תופס באופן סלקטיבי את האתרים הללו, בעוד מתכות כמו אבץ ונחושת נקשרות חלש במקומות אחרים או לא נקשרות כלל.
הקשחת חלקים נעים מרכזיים במקום שינוי כללי של המבנה
בהפתעה, TPST2 בנוכחות נתרן ובנוכחות מנגן נראו כמעט זהים באופן כללי; לא נצפה פתיחה או סגירה דרמטית של החלבון. במקום זאת, המתכות השפיעו בעיקר על שני אזורים גמישים ליד פתח האתר הפעיל: הליקס בשם α3 ולולאה סמוכה הידועה כלולאת α12–α13. במצבים ללא מתכת או עם קשירה רופפת, מקטעים אלה נעים ומציגים אי-סדירות חלקית. כש-Na⁺ נקשר, הם הופכים מסודרים יותר; Mn²⁺ מהדק אותם אף יותר, כפי שניכר בירידה בתנועתיות התרמית בנתוני קרני ה-X ובניתוחים ממוחשבים של גמישות. קשיחות נוספת זו מעלה במידה מתונה את טמפרטורת ההתמוססות של האנזים ונחשבת כמפחיתה את העלות "האנטרופית" של ארגון אתר הפעיל — מה שמקל ומהר יותר עבור TPST2 להנחות תת-מוצרים למיקום הנכון לסולפטציה. 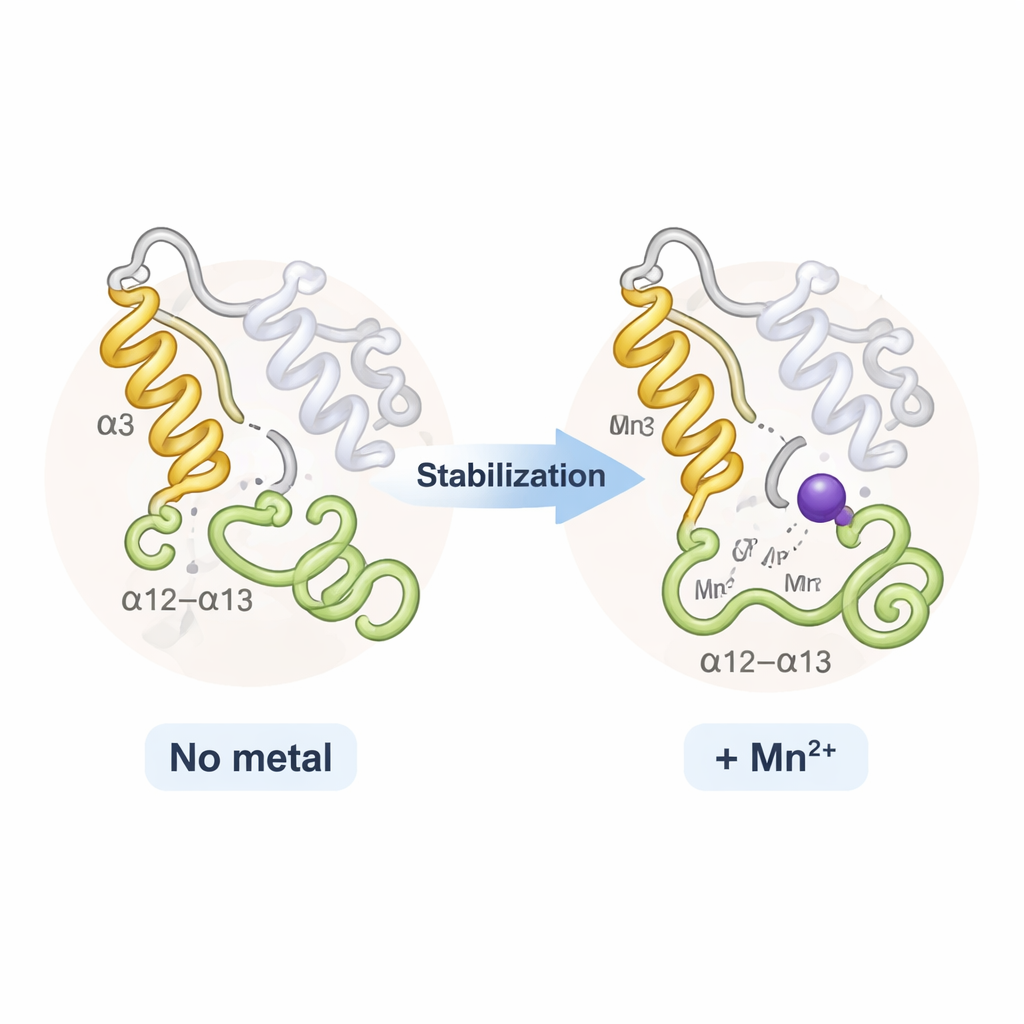
ממינרלים תאי לשליטה באיתות
המחברים מציעים מודל של "הפעלה באמצעות הזמנה". בהיעדר מתכת קשורה, TPST2 רופף סביב כניסת האתר הפעיל ופועל ביעילות נמוכה. נתרן, המצוי בשפע בתאים, יכול להיקשר לאותם אתרים וליצור מצב חלקית מסודר ופעיל במידה מועטה. מנגן, המצוי ברמות מיקרומולריות מבוקרות בתוך הגולג'י, נקשר בעוצמה רבה יותר ונועל את האזורים המרכזיים במצב מסודר באופן מיטבי, וכך ממקסם את היעילות הקטליטית. מסקנה זו מציעה ששינויים עדינים ברמות המנגן בגולג'י יכולים לכוונן עד כמה חזק TPST2 משנים את יעדיהם. מאחר ש-TPST2 משפיע על ייצור הורמונים ואיתות בסרטן, העבודה מדגישה קישור פוטנציאלי בין מאזן יוני מתכת, "קישוטים" חלבוניים ומחלה — ומספקת מסגרת מבנית לתכנון תרופות שמווסתות את פעילות TPST2 על ידי חיקוי או הפרעה של קשירת המתכת.
ציטוט: Jin, M., Noh, C., Yang, J. et al. Structural characterization of metal binding in human tyrosylprotein sulfotransferase 2, TPST2. Sci Rep 16, 6066 (2026). https://doi.org/10.1038/s41598-026-37189-4
מילות מפתח: סולפטציה של טירוזין, TPST2, מנצניום, מנגנון גולג'י, שינוי חלבוני