Clear Sky Science · he
למידת מכונה אינטגרטיבית ודוקינג מולקולרי חושפים ש־Narirutin פוגע ב‑ABCC1/ABCG2 לעיצוב מחדש של המיקרו‑סביבה החיסונית בסרטן המעי הגס
תרכובת פרי עם תקוות גדולות בסרטן
סרטן המעי הגס הוא אחד מהסוגים הקטלניים ביותר בעולם, ורבים מהמטופלים עדיין נאלצים להתמודד עם טיפולים קשים ועם עמידות לתרופות. במחקר זה בוחנים את הנארירוטין, חומר טבעי המצוי בפירות ההדר, כדי לבדוק האם הוא עשוי לסייע לגוף להילחם בגידולים במעי הגס בצורה עדינה יותר — על‑ידי שינוי האופן שבו תאי הסרטן מנהלים תרופות וכיצד תאי מערכת החיסון מתנהגים סביב הגידול.
מההדרים אל יעדי הסרטן
החוקרים התחילו בשאלה פשוטה: אם נארירוטין היה תרופה, לאילו חלקים בתא הוא היה נקשר? באמצעות מאגרי נתונים רבי‑ממדים פתוחים וכלי חיזוי ממוחשבים, סרקו הם אלפי גנים מתוך גידולי המעי והרקמה התקינה. לאחר מכן חפפו את הגנים המקושרים לסרטן עם אלה שנארירוטין סביר שישפיע עליהם. מתוך יותר מ‑3,000 גנים ששונו בסרטן המעי הגס, חזו כי נארירוטין יתקשר באופן משמעותי עם תשעה בלבד, ובפרט עם חמישה גנים "צמתיים" היושבים בנקודות בקרה מרכזיות בתוך תאי הגידול.
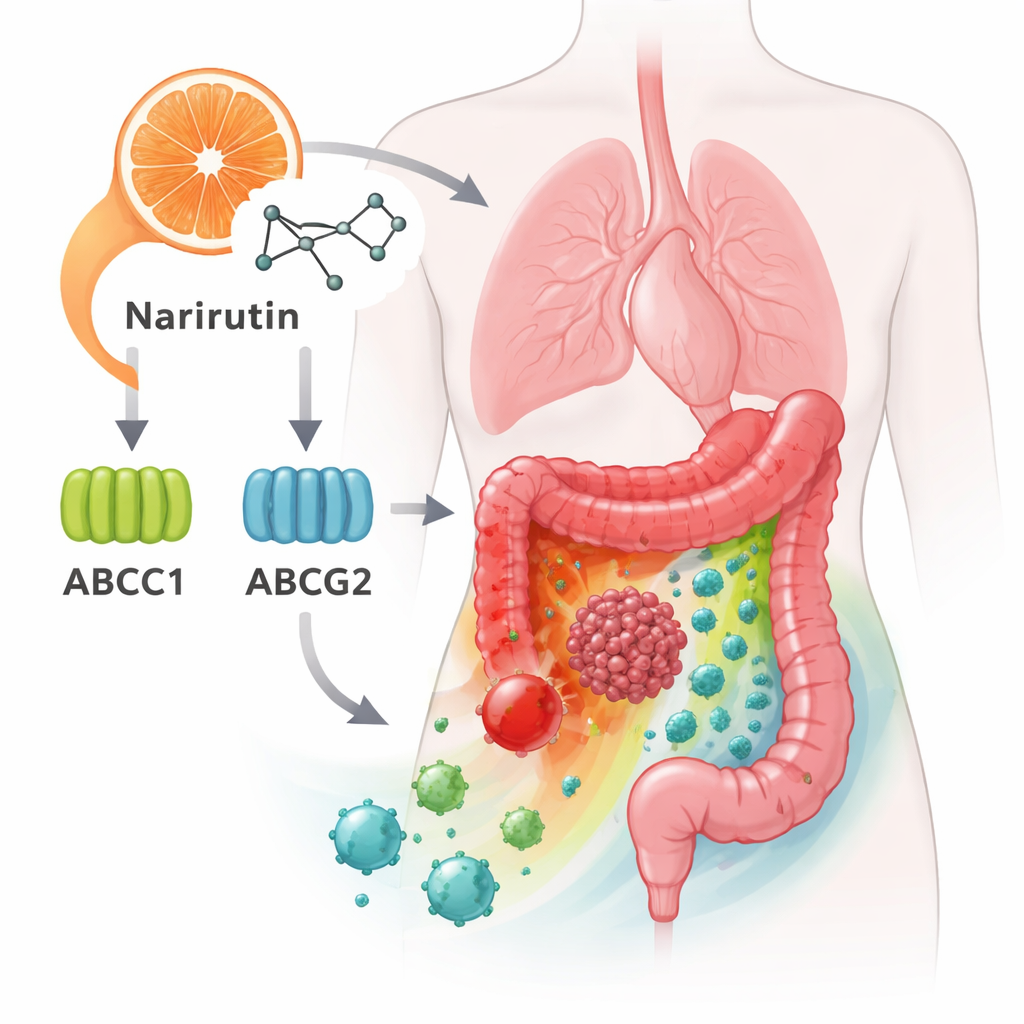
שומרי סף מרכזיים על פני תא הסרטן
בין הגנים הצמתיים הללו, בלטו שניים: ABCC1 ו‑ABCG2. הם מקודדים לחלבוני משאבה שיושבים בממברנת התא ומדחפים תרופות החוצה — אחת הסיבות לעמידות של חלק מהסרטן בכימותרפיה. הניתוח החדש מציע שנארירוטין יכול להיקשר למשאבות אלה ואולי להשפיע על פעילותן. גנים צמתיים נוספים, כולל CA12, EPHX2 ו‑PTGS1, מעורבים בניהול חומציות, מטבוליזם של שומנים ואותות דלקתיים. יחד הם מסייעים לקבוע האם גידול יתפתח ללא פיקוח, כיצד הוא יגיב לתרופות וכיצד יתנהל במגע עם רקמה סמוכה תקינה.
קשירה מדומיינת ותוצאות במציאות
כדי לבדוק האם נארירוטין יכול באמת להידבק לחלבונים המטרה האלה, השתמשו החוקרים בדוקינג מולקולרי — דגמים ממוחשבים ברזולוציה גבוהה שמנבאים כיצד מולקולה קטנה מתיישבת בתוך חלבון גדול. הדימויים הראו שנארירוטין מתאים בנוחות לכיסים בחלבוני היעד ויוצר אינטראקציות יציבות, כלומר הקשירה סבירה פיזיקלית. כאשר בחנו את נתוני החולים, מצאו כי הגנים הצמתיים מבחינים היטב בין רקמת סרטן לרקמה תקינה וקשורים לאורך החיים. לדוגמה, רמות גבוהות יותר של ABCC1 ו‑PTGS1 נטו להיות מקושרות לתוצאות גרועות יותר, מה שמרמז כי דיכוי גנים אלה — יתכן בעזרת תרכובות כמו נארירוטין — עשוי להיות מועיל.
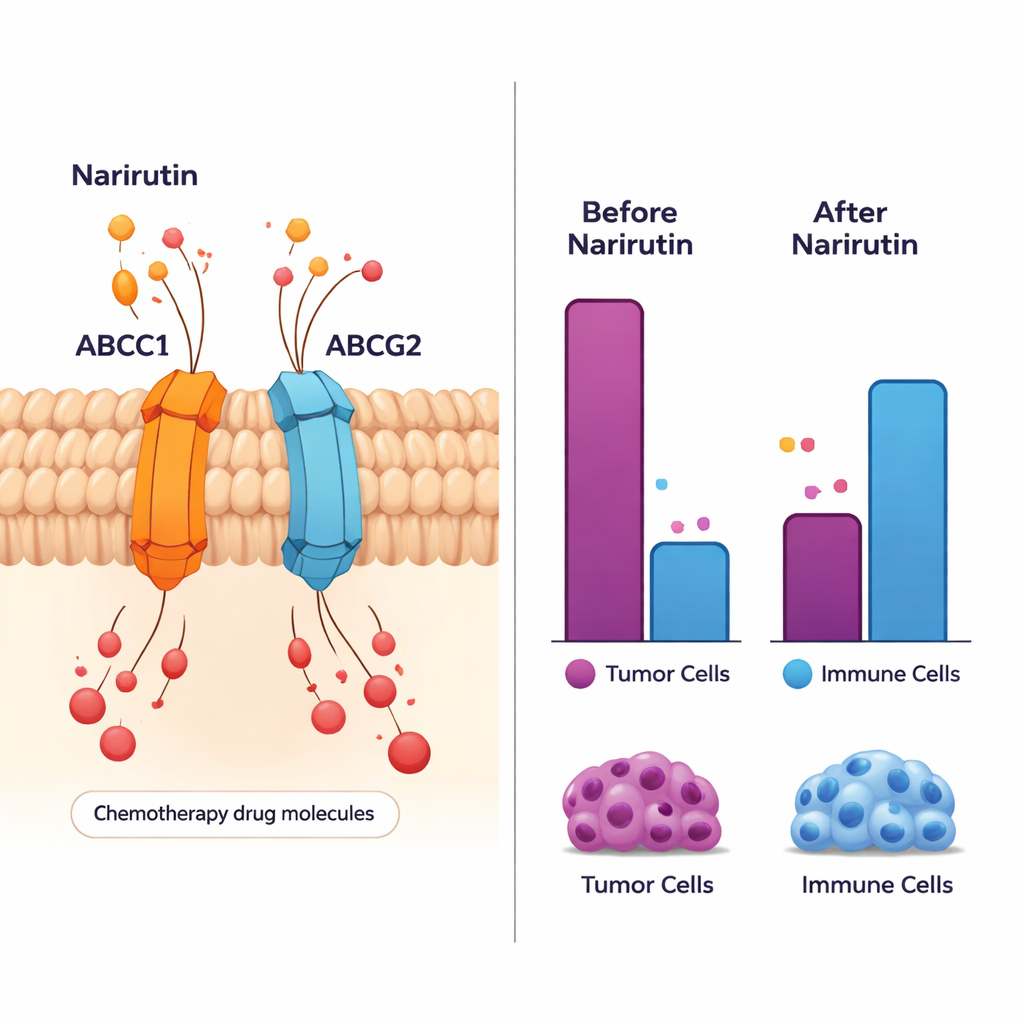
עיצוב מחדש של השכונה החיסונית של הגידול
הסרטן לא גדל בבדידות; הוא חי בתוך "שכונה" פעילה של תאי חיסון, כלי דם ורקמות תומכות. המחקר בחן 28 סוגי תאי חיסון שונים סביב גידולי המעי ומצא שינויים נרחבים בהשוואה לרקמה תקינה. תאי חיסון מסוימים התנהגו באופן שונה או היו בשפע רב יותר בגידולים, כגון תאי B מופעלים ותתי‑אוכלוסיות של תאי T. מטרותיו העיקריות של נארירוטין, במיוחד ABCC1, ABCG2 ו‑PTGS1, הראו קשרים חזקים לשינויים החיסוניים הללו. ממצאים אלה מציעים כי על‑ידי פעולה על גנים אלה, נארירוטין עשוי לא רק להשפיע ישירות על תאי הסרטן, אלא גם לכוון את התגובה החיסונית המקומית — ואולי להפוך את הסביבה לפחות ידידותית לצמיחה הגידולית.
תקווה, אך דרוש עוד מחקר
במילים פשוטות, מחקר זה מציע כי פלבנואיד טבעי מההדרים עשוי "לשבש את המשאבות" שתאי הסרטן משתמשים בהן כדי להימנע מכימותרפיה ולעזור לאתחל את הנוף החיסוני סביב גידולי המעי הגס. העבודה מתבססת על ניתוחים ממוחשבים רבי‑עוצמה ומאגרי נתונים גנטיים גדולים, ולא על ניסויים במעבדה או בניסויים קליניים, ולכן היא מייצגת שלב ראשוני אך חשוב. אם ניסויים עתידיים בתאים, בחיות ובחולים יאשרו את התחזיות הללו, נארירוטין — או תרופות בהשראתו — עשויים יום אחד להיכלל בטיפולים משולבים שיעשירו את היעילות של הטיפולים הסטנדרטיים לסרטן המעי הגס ויצמצמו עמידות לתרופות.
ציטוט: Bian, R., Wang, H., Zhang, H. et al. Integrative machine learning and molecular docking reveal Narirutin targets ABCC1/ABCG2 for immune microenvironment remodeling in colorectal cancer. Sci Rep 16, 7649 (2026). https://doi.org/10.1038/s41598-026-37181-y
מילות מפתח: סרטן המעי הגס, נארירוטין, עמידות לתרופות, מיקרו‑סביבה של הגידול, מודולציה חיסונית