Clear Sky Science · he
ניתוח השוואתי של מודלים מונחים וצוותיים עם חקירה בלתי מונחית לחיזוי מחלת אלצהיימר
מדוע התרעה מוקדמת חשובה
מחלת אלצהיימר חותרת בהדרגה לזיכרון ולחירות של אנשים, לעתים זמן רב לפני שאבחון ברור ניתן. משפחות, רופאים ומערכות בריאות מרוויחים כאשר סימני אזהרה מתגלים מוקדם, שכן זאת התקופה שבה טיפול, תכנון ותמיכה יכולים לעשות את ההבדל הגדול ביותר. המחקר הזה שואל שאלה מעשית: האם תוכניות מחשב שתוכננו בקפידה, ואומנו על מידע קליני שגרתי וסריקות מוח, יכולות לזהות דמנציה ביתר אמינות מכלי התקן הנוכחיים — ובה בעת לחשוף דפוסים נסתרי בדרך שבה המחלה מתפתחת?
הפיכת רשומות מטופלים לאותות שימושיים
החוקרים התבססו על אוסף נתונים ידוע בשם OASIS-2, שעוקב אחרי 150 מבוגרים בגילאי 60 עד 96 לאורך מספר שנים. עבור כל ביקור, המאגר כולל מידע בסיסי כגון גיל, שנות השכלה ומעמד סוציו-אקונומי, וכן ציוני מבחנים קוגניטיביים ומדידות שנגזרו מסריקות MRI של המוח, כמו נפח מוח כללי. לפני כל חיזוי, הצוות ניקה את הנתונים, הסיר מזהים ומקרים לא ברורים, השלים מספר קטן של ערכים חסרים והעמיד את כל המדידות המספריות על סקלת מידה משותפת. הם גם התמודדו עם בעיה מעשית מרכזית: הרבה יותר אנשים במאגר היו בריאים מאשר חולים בדמנציה. כדי למנוע מהמודלים לנחש ברוב המכריע של המקרים «אין דמנציה», החוקרים השתמשו בסכמות משקל שמעניקות חשיבות גדולה יותר לשגיאות בקבוצה הקטנה יותר של החולים בדמנציה בזמן האימון.
השוואת כלים קלאסיים עם צוותי מודלים
עם מערך הנתונים המוכן הזה, המחברים השוו כלי למידת מכונה מוכרים עם «אנצמבל» מתקדם יותר, שמחבר כמה מודלים לנבאי חזק אחד. הקבוצה הקלאסית כללה רגרסיה לוגיסטית, עצי החלטה, מכונות וקטור תמיכה ויער אקראי. קבוצת האנסמבל כללה AdaBoost, XGBoost ומודל הצבעת רוב ששילב שלושה מסווגים מכוילים. כל המודלים אומנו על חלק אחד של הנתונים ונבחנו על מקרים שהוחזקו בצד, כשהביצועים נמדדו באמצעות דיוק, היכולת לזהות נכון יחידים בדמנציה (recall) ושטח תחת העקומה ROC, סיכום של כמה טוב המודל מפריד בין מקרים בריאים לחולים. 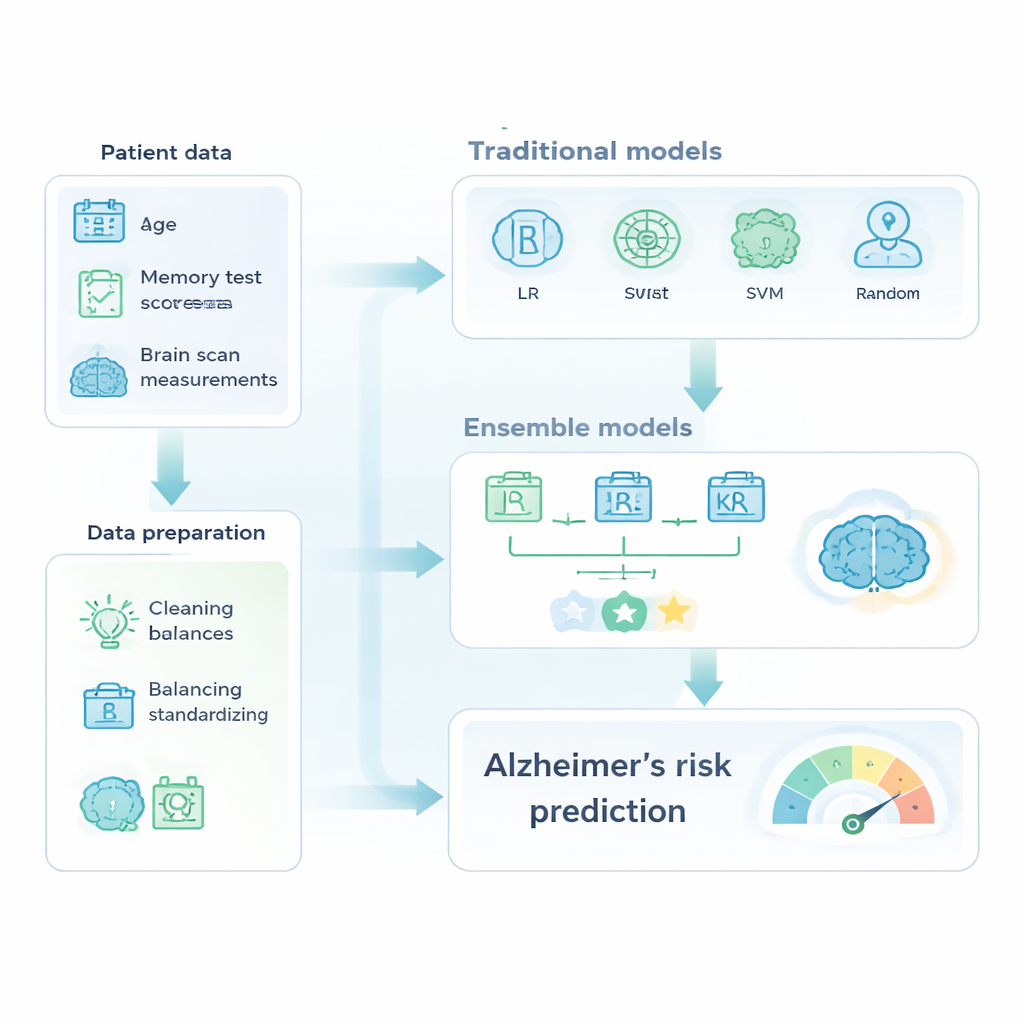
כשרב־מוחות גוברים על אחד
התוצאות הישירות היו ברורות. בעוד ששיטות מסורתיות מובחרות הופיעו עם ביצועים סבירים, הן הגיעו לרוויה סביב הרמה שדווחה במחקרים קודמים, עם דיוקים במבחן בטווח הנמוך־בינוני של 80 אחוזים. לעומת זאת, מודל הצבעת הרוב הגיע לכ־95 אחוז דיוק ולדירוג ROC גבוה דומה, ועבר את הסף הנפוץ של 92 אחוז. AdaBoost ומודלים צוותיים אחרים גם ביצעו טוב יותר מכל מודל מסורתי יחיד. יתרון זה נוצר מכיוון שאלגוריתמים שונים לוכדים היבטים שונים מהנתונים; באמצעות מתן אפשרות להם «להצביע», האנסמבל ממתן תכונות ספציפיות מדי והתאמה יתר של מודל בודד, מה שמוביל לחיזויים יציבים יותר. המחיר של השדרוג הזה הוא שקיפות מופחתת: קשה יותר להבין במבט אחד מדוע אנסמבל קיבל החלטה מסוימת בהשוואה לרגרסיה פשוטה או לעץ בודד. 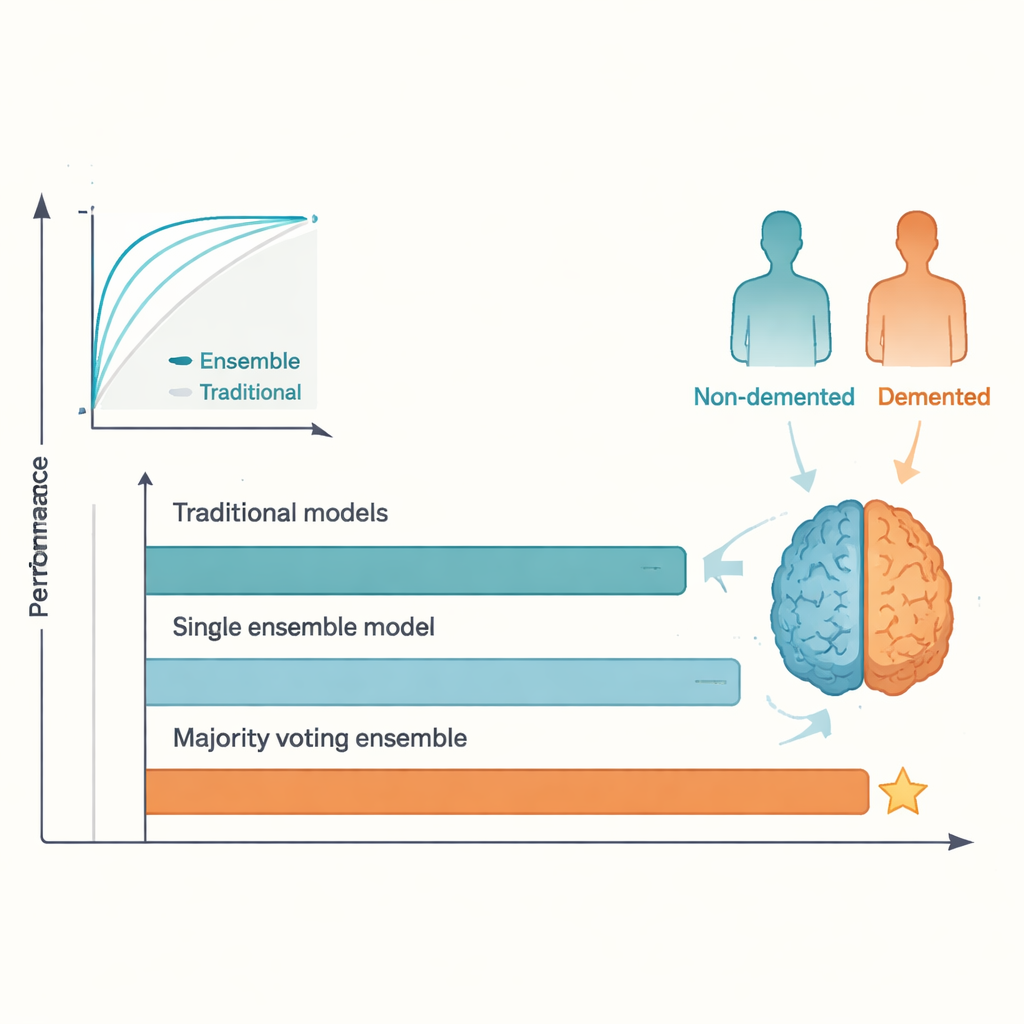
חיפוש קיבוצים טבעיים בנתונים
מעבר לשאלה מי חולה בדמנציה, החוקרים גם בדקו כיצד החולים מקובצים באופן טבעי, ללא התייחסות לתויות אבחון. לשם כך הפכו את כל המשתנים הרציפים לקטגוריות מסודרות — כגון טווחי גיל או נפח מוח — והשתמשו בטכניקה הנקראת ניתוח התאמה מרובה (multiple correspondence analysis) כדי לדחוס את המידע העשיר הזה למספר מצומצם של ממדים תת־בסיסיים. לאחר מכן השתמשו באשכולות k‑means כדי לחלק את הנקודות הללו למספר קטן של קבוצות משכּללות. חלק מהאשכולות נשלטו על ידי אנשים עם נפח מוח נשמר וציוני קוגניציה תקינים, בעוד שאחרים כללו יחידים עם נפח מוח נמוך, תוצאות מבחן ירודות ודירוגי דמנציה חמורים יותר. העובדה שהאשכולות הבלתי־מונחים הללו השוו היטב למצב הקליני מרמזת שהנתונים נושאים אות חזקה ועקבית על סיכון המחלה והתפתחותה.
מה משמעות הדבר לחולים ולצוותים קליניים
ללקוח מן השורה, המסקנה פשוטה: כשמעצבים בקפידה, צוותים של מודלי למידת מכונה יכולים לזהות דמנציה קשורה לאלצהיימר בנתונים קליניים מובנים בדיוק גבוה יותר משיטות ישנות, והם יכולים לעשות זאת באמצעות מידע שרבים מהמרפאות כבר אוספים. באותו הזמן, טכניקות חקירה מגלות שאנשים נופלים לפרופילים מובחנים של בריאות מוחית ותפקוד קוגניטיבי, דבר שמרמז על מסלולים שונים שהמחלה עשויה לקחת. אף על פי שהמחקר מוגבל בגודלו ובמורכבות פרשנות מודלי האנסמבל, הוא מראה ששילוב של חיזוי עוצמתי עם ניתוח חוקרני זהיר יכול גם לחדד זיהוי מוקדם וגם להעמיק את הבנתנו לגבי אופן התפתחות האלצהיימר.
ציטוט: Amr, Y., Gad, W., Leiva, V. et al. Comparative analysis of supervised and ensemble models with unsupervised exploration for alzheimer’s disease prediction. Sci Rep 16, 7322 (2026). https://doi.org/10.1038/s41598-026-37122-9
מילות מפתח: מחלת אלצהיימר, חיזוי דמנציה, למידת מכונה, מודלים צוותיים, הדמיית מוח