Clear Sky Science · he
מחקר השוואתי לחיזוי גרורות מרוחקות לאחר ניתוח בסרטן הריאות על בסיס מודלי למידת מכונה
מדוע חיזוי התפשטות הסרטן חשוב
סרטן הריאות נותר אחד מסוגי הסרטן הקטלניים ביותר, גם כאשר המנתחים מסירים את כל הגידולים הנראים לעין. מטופלים רבים מפתחים מאחורי הקלעים מאגרי סרטן שמופיעים מאוחר יותר במוח, בעצמות, בכבד או באיברים אחרים. רופאים מעוניינים לדעת, זמן קצר לאחר הניתוח, אילו מטופלים סביר יותר שיחוו התפשטות מרוחקת כדי להתאים את ביקורי המעקב והטיפולים. המחקר הזה בוחן האם תוכנות מחשב מודרניות, המכונות מודלי למידת מכונה, יכולות לעזור לחזות מי בסיכון גבוה יותר, בהתבסס על מידע שבבתי החולים כבר נאסף במסגרת הטיפול השגרתי.
מבט מעמיק על מאגר גדול של מטופלים
החוקרים בדקו תיקים של 3,120 אנשים עם סרטן ריאות שלבים I–III שעברו הסרת הגידול במרכז אונקולוגי בודד בסין. לכל מטופל היה לפחות שנתיים של מעקב. עבור כל מטופל נאספו 52 סוגי מידע, כולל גיל, מין, משקל גוף, היסטוריית עישון, ממצאי סריקות, פרטי הניתוח, בדיקות מעבדה והאם קיבל טיפולים נוספים כגון כימותרפיה או הקרנות לאחר הניתוח. לאורך זמן, 596 מהמטופלים הללו פיתחו גרורות מרוחקות, בעוד 2,524 לא פיתחו. התמהיל הזה במציאות קלינית איפשר לצוות לזהות אילו תכונות נקשרו להתפשטות עתידית.
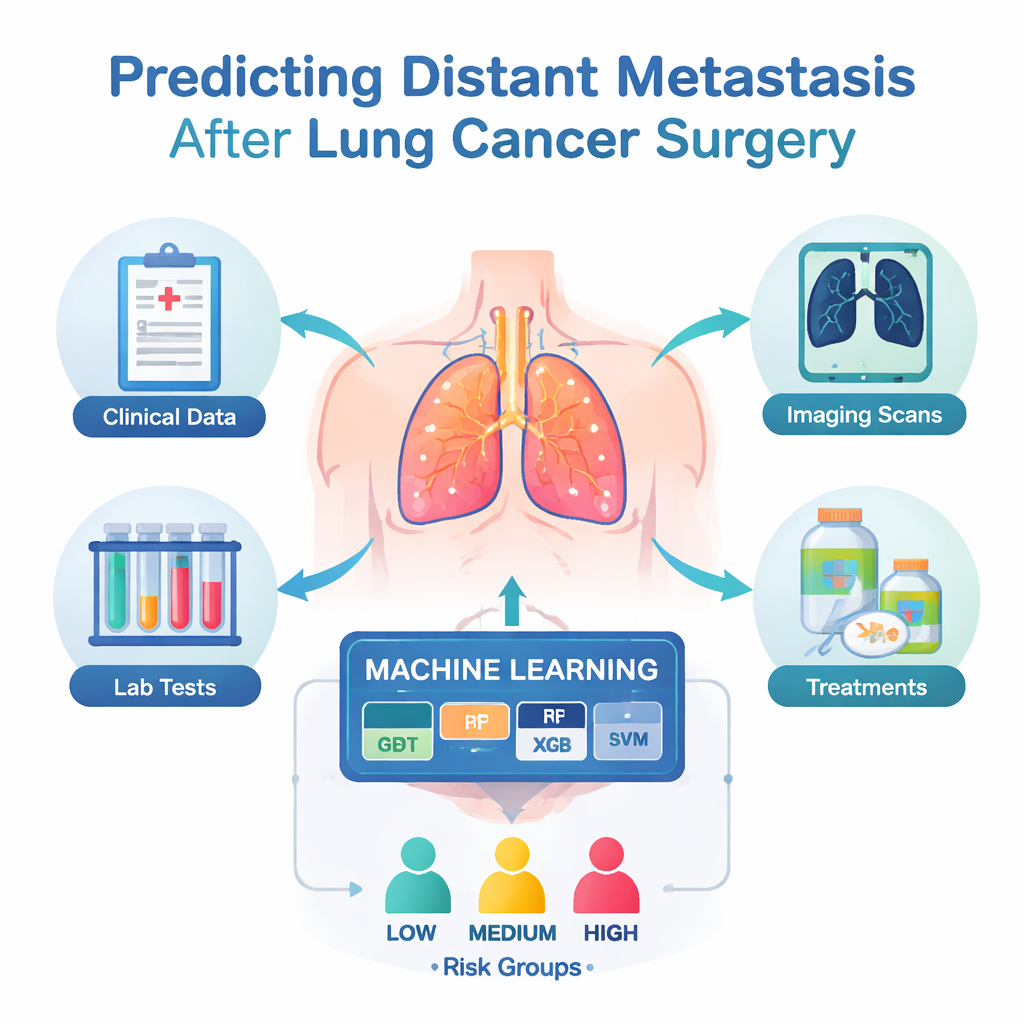
לימוד מחשבים לזהות דפוסי סיכון
במקום להסתמך על נוסחה בודדת, המדענים השוו תשע שיטות למידת מכונה שונות, מעצים החלטה פשוטות ועד טכניקות מתקדמות שמאחדות מודלים קטנים רבים. תחילה השתמשו בסינון מתמטי כדי לצמצם את 52 המשתנים המקוריים לקבוצה קטנה ומידעית יותר. לאחר מכן, בסבבים חוזרים, אימנו כל מודל על חלק מהנתונים ובחנו אותו על מטופלים שהוא מעולם לא "ראה". מאחר שרק כשיעור של אחד מכל חמישה מטופלים פיתח גרורות, התאימו את האימון כך שהמחשב לא יבחין בפשטות ב"סיכון נמוך" עבור כולם. הערכת הביצועים נעשתה באמצעות מספר מדדים, כולל עד כמה המודלים מפרידים בין מטופלים בסיכון גבוה לנמוך ועד כמה הסיכונים החזויים תואמים את מה שקרה בפועל.
מציאת המודל האמין ביותר
מתוך התשעה, מודל בשם Gradient Boosting Decision Tree (GBDT) בלט. על נתוני המבחן הוא דירג את המטופלים נכון בדיוק כולל של כ-77%, וציון הסכמתי שלו להבחנה (שטח מתחת לעקומת ROC) עמד על 0.81, נתון הנחשב חזק לכלי חיזוי רפואי. המודל היה מצוין במיוחד בזיהוי מטופלים שישארו ללא גרורות (ערך ניבוי שלילי גבוה), כלומר תוצאה של סיכון נמוך הייתה לרוב מרגיעה. כשצוות החוקרים בחן את התנהגות המודל לאורך חלוקות אקראיות רבות של הנתונים, הביצועים נשארו יציבים, מה שמעיד שהמודל לא זכר פשוט אנומליות של תת-קבוצה מסוימת.
מה מניע את החלטות המודל
ביקורת נפוצה על למידת מכונה היא שהיא עלולה להיות "קופסה שחורה". כדי להתמודד עם זה, המחברים השתמשו בשיטת הסבר הנקראת SHAP, שמקצה לכל גורם תרומה לאומדן הסיכון הסופי עבור כל מטופל. ניתוח זה הראה שהאותות החזקים ביותר היו האם המטופל קיבל כימותרפיה או הקרנות לאחר הניתוח, כמה קשריות לימפה היו מעורבות במחלה, גיל, מדד מסת הגוף (BMI) וספירת נויטרופילים לפני הניתוח, סוג של תאי דם לבנים. מטופלים עם מעורבות קשריות לימפה מתקדמת וסימני דלקת מערכתית נטו לקבל חיזוי של סיכון גבוה יותר. המחברים מדגישים שתרומות גבוהות מצד כימותרפיה והקרנות אינן אומרות שטיפולים אלה גורמים לגרורות; להפך, הן מעידות שרופאים כבר העריכו שהמחלה אגרסיבית יותר, ולכן מטופלים אלה היו בסיכון גבוה מלכתחילה.
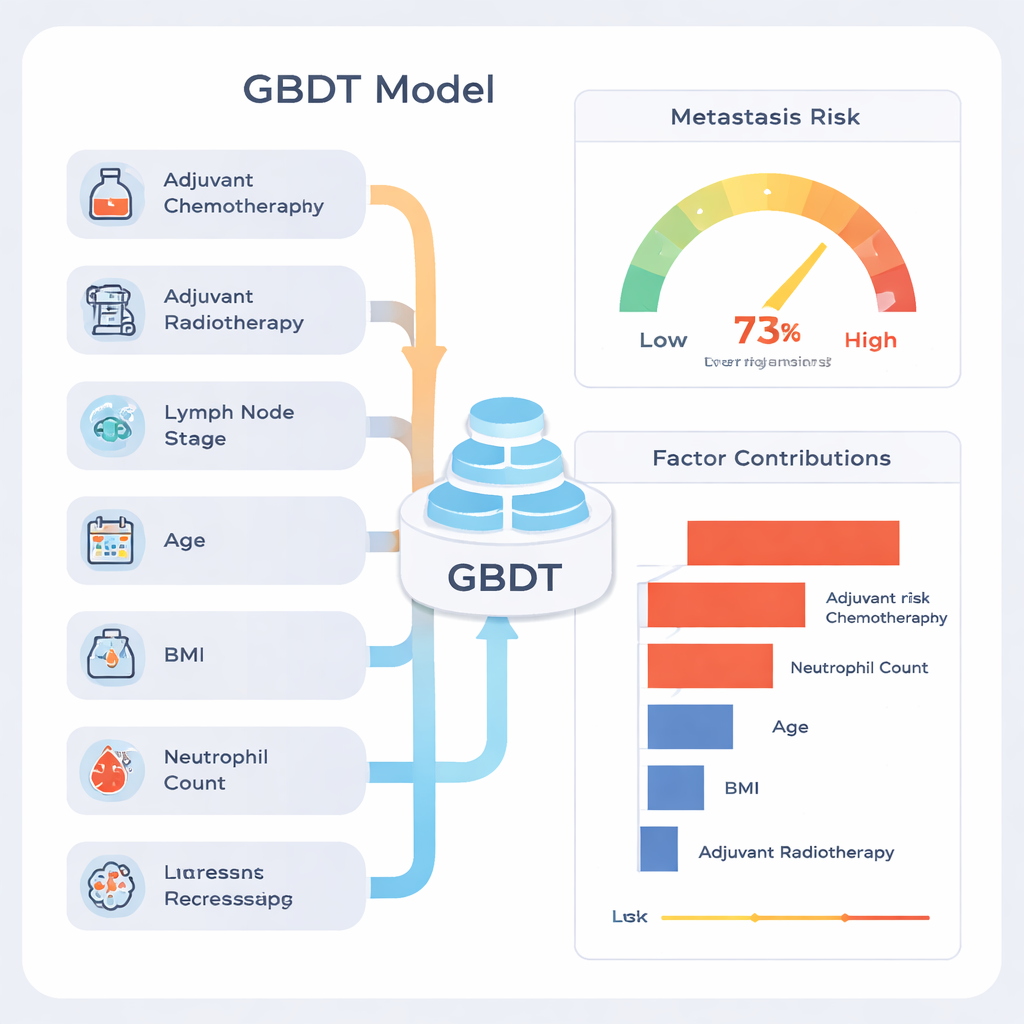
איך זה עשוי לעזור למטופלים בפועל
מכיוון שהמודל משתמש במידע שרוב מרכזי הסרטן כבר רושמים, הוא יכול, לאחר בדיקות נוספות, להשתלב בתוכנת בית החולים. עבור מטופל חדש שעבר ניתוח ריאה זה עתה, המערכת תוכל למשוך את הנתונים שלו ולהפיק הסתברות אישית לגרורות מרוחקות, יחד עם הסבר פשוט אילו גורמים מעלים או מורידים את הסיכון. קלינאים יוכלו להשתמש בכך כדי להחליט מי זקוק למעקב הדמיה צמוד יותר, לייעוץ נוסף או לרישום בניסויים קליניים, ומי עשוי להימנע בבטחה ממעקב אינטנסיבי. המחקר נערך בבית חולים בודד, לכן הכלי עדיין צריך לעבור בדיקות וכיול באזורים ומערכות בריאות אחרות. עם זאת, הוא מציע מתווה מבטיח לשילוב נתונים קליניים שגרתיים עם למידת מכונה שקופה לשיפור הטיפול לטווח הארוך במטופלים עם סרטן ריאות.
ציטוט: Guo, X., Xu, T., Luo, Y. et al. Comparative study on predicting postoperative distant metastasis of lung cancer based on machine learning models. Sci Rep 16, 6468 (2026). https://doi.org/10.1038/s41598-026-37113-w
מילות מפתח: סרטן ריאות, גרורות מרוחקות, למידת מכונה, חיזוי סיכון, מעקב לאחר ניתוח