Clear Sky Science · he
כימות אוטומטי של לימפוציטים חודרים גידול בעזרת למידת מכונה חושף תכונות פרוגנוסטיות ואימונו־גנומיות בסרטן הריאה
מדוע חשוב לספור תאים חיסוניים קטנטנים בגידולי ריאה
סרטן הריאה נותר אחד הסרטנים הקטלניים ביותר, אך לא כל הגידולים מתנהגים אותו דבר. בחלקם יש שגרה אינטנסיבית של תאים חיסוניים החודרים לתוך הגידול, בעוד אחרים נשארים כמעט בלתי נגיעים. לימפוציטים חודרי גידול (TILs) יכולים לרמוז כיצד המצב יתקדם ואילו מטופלים עשויים להרוויח מתרופות אימונותרפיות מודרניות. האתגר הוא שהיום ספירת ה‑TIL נעשית בדרך כלל בעין תחת מיקרוסקופ, היא איטית ותלויה במתבונן. המחקר הזה שואל שאלה רלוונטית: האם נוכל להשתמש בלמידת מכונה כדי למדוד אוטומטית תאים אלה על פתקים פתולוגיים שגרתיים, ומה זה מגלה על ביולוגיית סרטן הריאה וההישרדות של המטופלים?
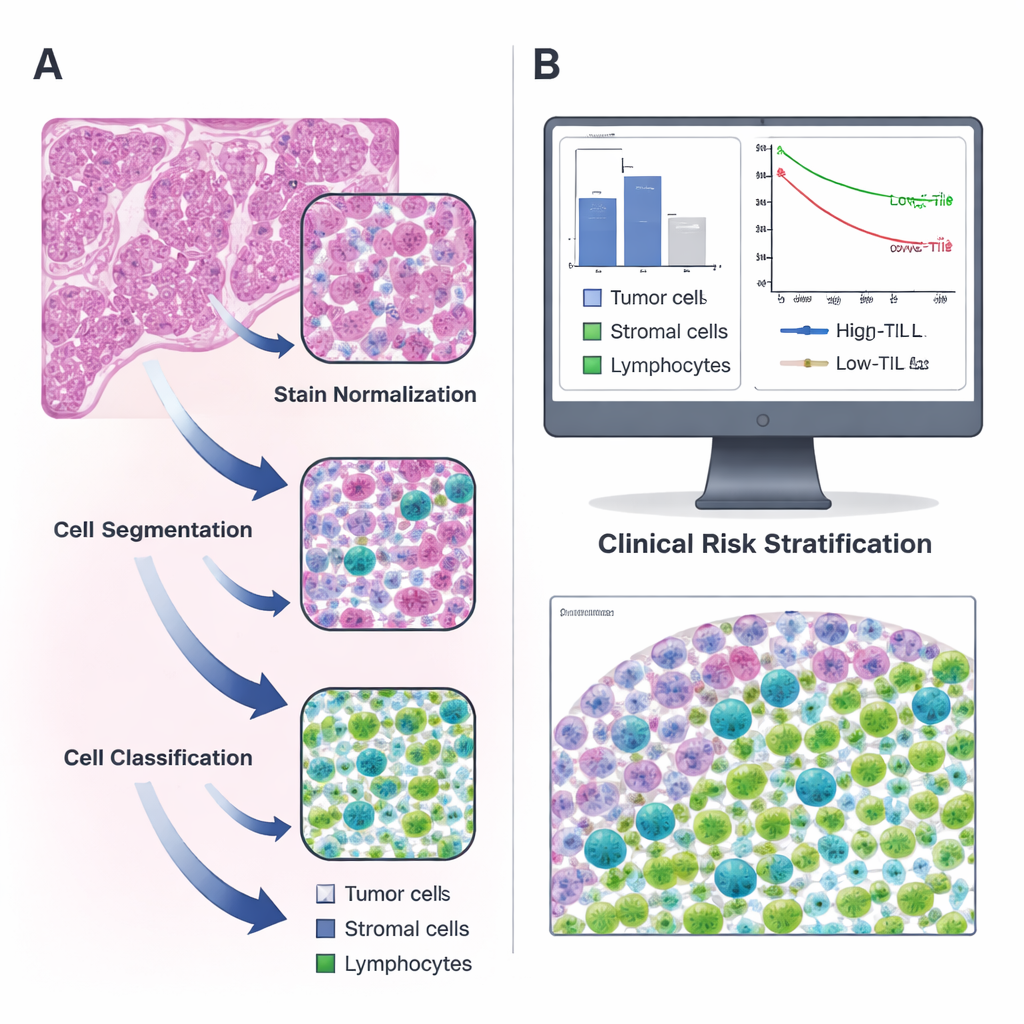
הפיכת פרוסות שגרתיות למפות דיגיטליות
החוקרים התמקדו באדנוקרצינומה של הריאה, סוג נפוץ של סרטן ריאה, והשתמשו בנתונים ציבוריים ממאגר The Cancer Genome Atlas בנוסף לקבוצת אימות ממטופלים בב院 שלהם. עבור כל מטופל הם ניתחו פרוסות רקמה צבועות המטוקסילין ואאוזין (H&E) — התמונות הורודות‑סגולות המוכרות לכל פתולוג. עם התוכנה הקוד‑פתוח QuPath הם בנו צנרת שלבים: תחילה תיקנו הבדלי צבע בין הפרוסות; לאחר מכן השתמשו באלגוריתם מים‑מפרידים (watershed) כדי להפריד גרעיני תאים חופפים; ולבסוף סיווג ממוחשב מאומן תייג כל תא שנתגלה כגידול, רקמת תמיכה (סטומה) או לימפוציט. שני פתולוגים מומחים סקרו ותיקנו שוב ושוב את עבודת המכונה עד שהיא זיהתה באופן אמין את סוגי התאים השונים בעצמה.
קישור בין ספירת תאים חיסוניים לתוצאות מטופלים
כאשר המערכת יכלה לזהות תאים בביטחון, הצוות חישב כמה לימפוציטים נמצאים לכל מילימטר רבוע של רקמת גידול יותר מ‑300 מטופלים. הם מצאו שרמות ה‑TIL שונות במידה רבה ובממוצע מהוות רק חלק קטן מכלל התאים. באמצעות גישה סטטיסטית למציאת נקודת הסף המידע‑ית ביותר, בחרו ב‑135 TILs למילימטר רבוע כתוחם שממנו מגדירים גידולים כ"גבוהים" או "נמוכים" ב‑TIL. מטופלים שאצלם רמת ה‑TIL חרגה ממגבלה זו חיו יותר זמן לעומת אלו עם חוסר חודרנות חיסונית, ותבנית זו התקיימה גם בקבוצת המקור וגם בקבוצת האימות. במלים אחרות, מספר פשוט שמפיק כלי אוטומטי תפס הבדלים משמעותיים בהישרדות, בהדהוד לממצאים קודמים שדרשו עבודה ידנית רבה.
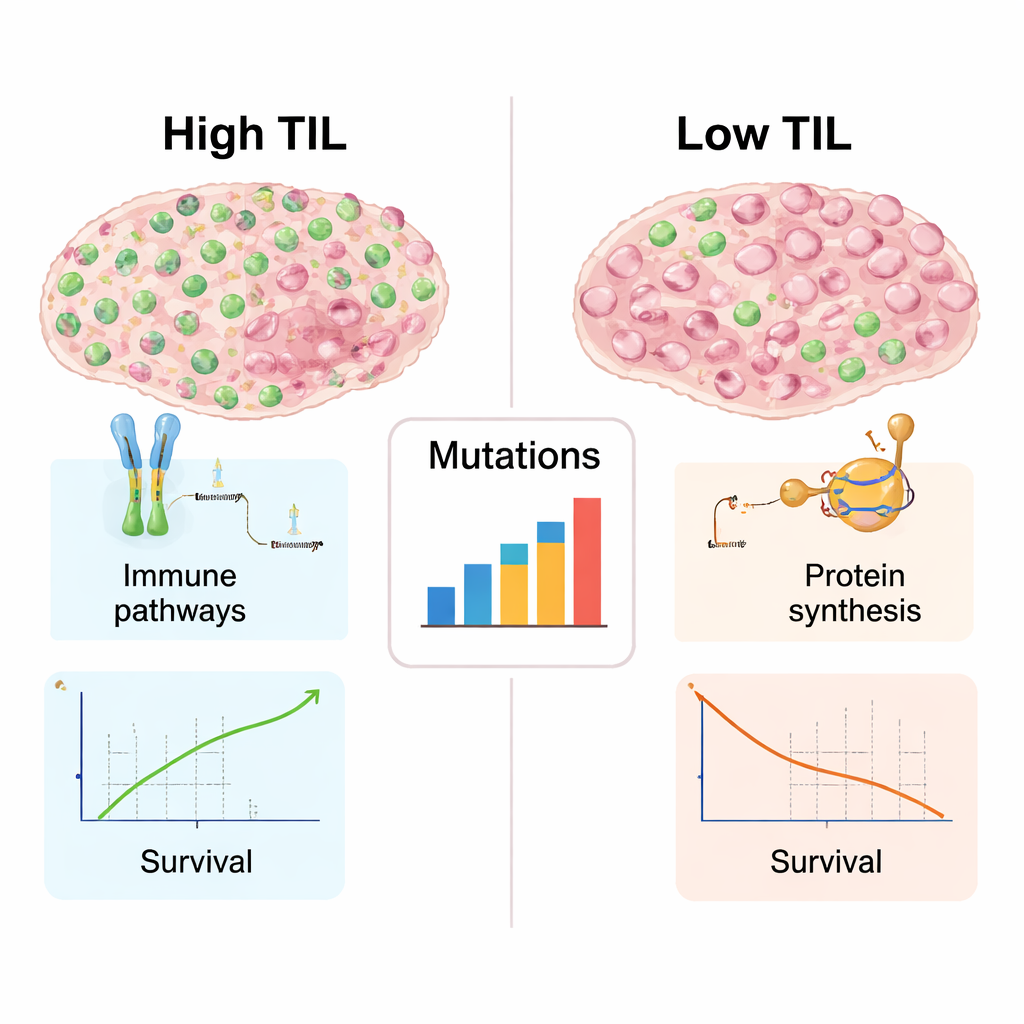
איך נראים גידולים עשירים בחיסון מתחת למכסה המנוע
מכיוון שנתונים גנומיים ומולקולריים היו זמינים עבור רבים מהגידולים הללו, המחברים יכלו לחקור מה מבדיל בין גידולי בעלות TIL גבוהה לאלה עם TIL נמוכה מעבר לספירות התאים הפשוטות. גידולים ששטופים בלימפוציטים הראו חתימות חזקות יותר של פעילות חיסונית: גנים המעורבים בזיהוי חלבונים לא תקינים, בהצגתם לתאי T ובתיאום התקפה חיסונית היו פעילים יותר. לגידולים אלה הייתה גם תמהיל רחב יותר של מוטציות DNA, שיכולות ליצור מטרות חדשות למערכת החיסון. לעומת זאת, גידולים עם TIL נמוך הראו על נטייה לגנים הקשורים לבניית ריבוזומים ולסינתזת חלבונים — סימן למכונת גדילה אינטנסיבית אך למעורבות חיסונית שקטה יחסית. הפיצול הזה משקף את הניגוד המוכר כיום בין גידולים "חמים" — עשירים בתאים חיסוניים וסביר שיגיבו לאימונותרפיה — לבין גידולים "קרים" שהמערכת החיסונית מתעלמת מהם ברובו.
להדריך מחשב לחזות מצב חיסוני
הצוות צעד צעד נוסף ושאל האם קבוצה קומפקטית של תכונות תמונה יכולה לחזות אם גידול ייכלל בקטגוריית TIL גבוהה או נמוכה מבלי לספור כל לימפוציט במפורש. הם תמצתו דפוסי מרקם עדינים בפרוסות — כיצד עוצמות הפיקסלים משתנות על פני שכונות קטנות — לתכונות כך בשם Haralick, ושילבו אותן עם שלב הקליני של הגידול במודל יער אקראי (random forest). באימות מצטלב הממיין הזה הפריד נכונה בין גידולים בעלי TIL גבוהה לנמוכה בדיוק חזק, ושמר על ביצועים סבירים גם בקבוצת אימות עצמאית מבית‑חולים אחר. חשוב לציין שכל הגישה רצה על מחשבים סטנדרטיים תוך שימוש בתוכנה חופשית, מה שמרמז שמעבדות פתולוגיה רבות עשויות, עקרונית, לאמץ אותה ללא חומרה מיוחדת.
מה משמעות הדבר לטיפול העתידי בסרטן הריאה
עבור קורא לא‑מומחה, המסר המרכזי הוא שמחשב יכול ללמוד לקרוא פרוסות שגרתיות של סרטן ריאה באופן שתופס עד כמה מערכת החיסון היגרה בגידול. רמות גבוהות של לימפוציטים חודרים מסמנות קרב חיסוני פעיל יותר, נוף מוטציות עשיר יותר והישרדות כוללת טובה יותר. אף שדרוש עוד מחקר — במיוחד במטופלים שטופלו בפועל באימונותרפיה — שיטה אוטומטית זו עשויה בסופו של דבר לסייע לרופאים למיין במהירות ובעקביות גידולים לקטגוריות אימוניות "חמות" ו"קרות". דבר זה, בתורו, עשוי לכוון החלטות מי סביר להרוויח מטיפולים מבוססי חיסון ולעודד אסטרטגיות חדשות להחדרת חום לגידולים קרים.
ציטוט: Li, A., Pang, Y., Zhang, H. et al. Automated quantification of tumor-infiltrating lymphocytes by machine learning reveals prognostic and immunogenomic features in lung cancer. Sci Rep 16, 7006 (2026). https://doi.org/10.1038/s41598-026-37076-y
מילות מפתח: אדנוקרצינומה של הריאה, לימפוציטים חודרי גידול, למידת מכונה, פתולוגיה דיגיטלית, אימונותרפיה של סרטן