Clear Sky Science · he
אבחון אוטומטי של צורת Plus ושלבים מוקדמים של ROP באמצעות מודלים של למידה עמוקה
מדוע עיניים קטנות ומחשבים חכמים משמעותיים
בכל שנה אלפי תינוקות פגים נמצאים בסיכון לאבד את הראייה מכיוון שכלי הדם בחלק האחורי של העין אינם גדלים באופן תקין — מצב שנקרא רטינופתיה של הפגות מוקדמת (ROP). גילוי הבעיה בשלבים מוקדמים יכול להציל את הראייה, אך הדבר דורש בדיקות עיניים תכופות על ידי מומחים מיומנים — מומחים שמספרם מוגבל בחלקים רבים של העולם. המחקר הזה בוחן כיצד בינה מלאכותית (AI) מודרנית יכולה לסייע לרופאים לזהות סימני אזהרה מוקדמים בצילומי רשתית, ובכך להציע סקר ברמת מומחה לבתי חולים ומרפאות שאין בהם מומחים בתחום העיניים.
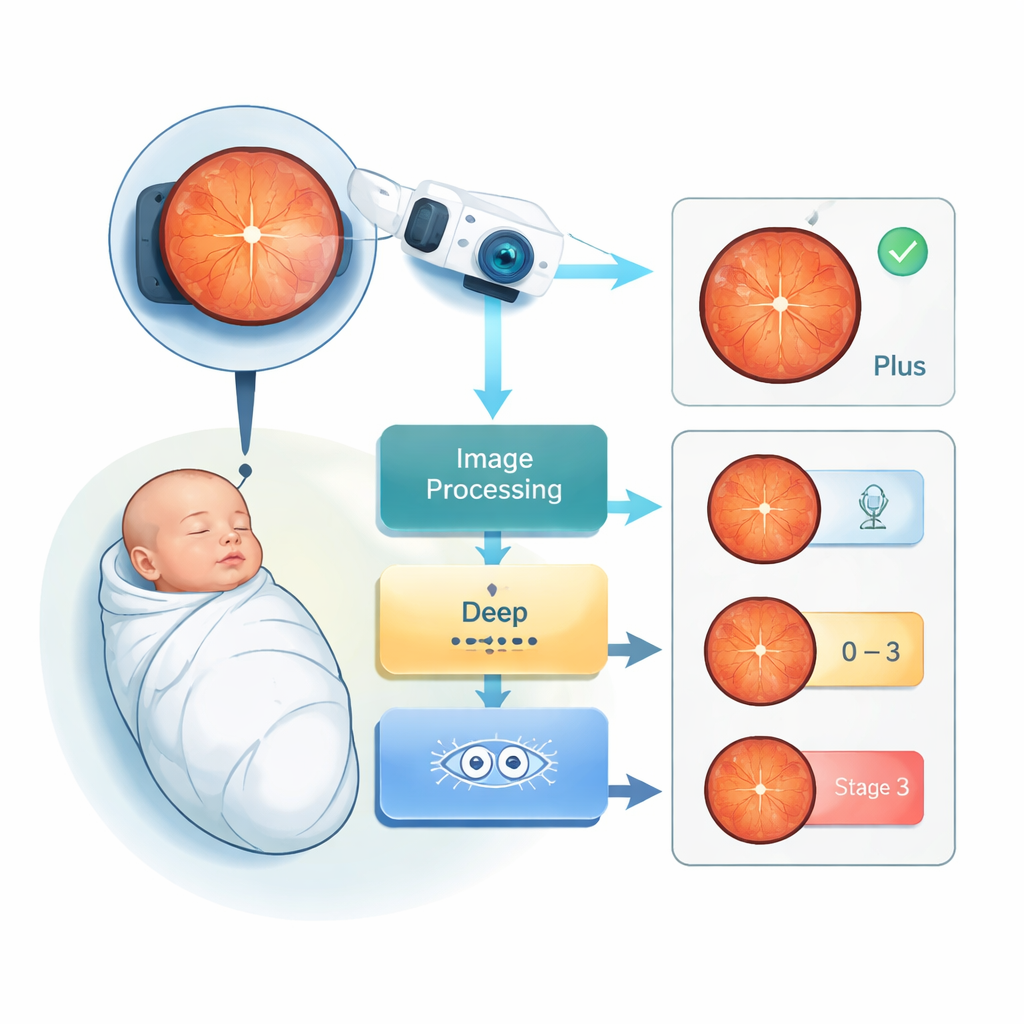
הבעיה: ראייה פגיעה אצל החולים הקטנים ביותר
ROP מתפתחת כאשר לידה מוקדמת מפסיקה את הצמיחה התקינה של כלי הדם ברשתית, השכבה הרגישה לאור בחלק האחורי של העין. תינוקות שנולדו מוקדם מאוד או במשקל לידה נמוך במיוחד נמצאים בסיכון הגבוה ביותר. במקרים קלים העין עשויה להחלים לבד. במקרים חמורים כלי דם בלתי תקינים יכולים למתוח את הרשתית ולגרום לעיוורון קבוע. ברחבי העולם ROP עיוור קרוב ל-50,000 אנשים, במיוחד באזורים שבהם הטיפול הנאונאטלי שיפר את ההישרדות אך תוכניות סקר העין והמומחים לא צעדו בקצב. הבדיקות הקיימות תובעניות מבחינת עבודה, יקרות וסובייקטיביות: לעיתים שני מומחים יכולים שלא להסכים לגבי חומרת המחלה של תינוק.
מה הרופאים מחפשים: כלי דם עקומים ושלבים מוקדמים
רופאי עיניים מעריכים ROP באמצעות שתי רמזים עיקריים בתמונות רשתית. האחד הוא השלב הכולל של המחלה, משלב 0 (ללא שינויים נראים) דרך שלבי הבעיה המוקדמים (1–3). השני הוא "Plus disease", סימן אזהרה שבו כלי הדם ברשתית מתרחבים ומסתלסלים בצורה לא שגרתית. Plus disease מסמן סיכון גבוה יותר לנזק חמור ולעיתים מפעיל טיפול כמו טיפול בלייזר או הזרקות של תרופות. הערכת תכונות אלה בעין היא מאתגרת, במיוחד כאשר התמונות מטושטשות או כאשר תינוקות זקוקים לבדיקות חוזרות שבוע אחרי שבוע. מערכת שיכולה לזהות באופן אוטומטי Plus disease ולהעריך את שלב ה-ROP רק מתמונות תהיה כלי תמיכה רב-עוצמה לרופאים.
כיצד ה-AI רואה: יצירת מפות כלי דם מתוך צילומי העין
החוקרים בנו צינור עבודה של AI בשתי שלבים באמצעות יותר מ-6,000 תמונות רשתית מ-188 תינוקות. בראשית, הם אימנו רשת נוירונים לצייר "מפת כלי דם" מדויקת של כל רשתית, המדגישה כל כלי דם נראה, אפילו הענפים הדקים ביותר. בין מספר מודלים של עיבוד תמונה מתחרים, גרסה בשם U-Net++ הראתה ביצועים הטובים ביותר בלכידת דפוסי כלי דם מפורטים, במיוחד בתמונות רועשות או בעלות ניגוד נמוך. לשיפור הבהירות הצוות חיזק כל תמונה באמצעות פילטרים להגברת ניגוד ולהפחתת רעש לפני המקטע. לזיהוי Plus disease הם הזינו לרשת השנייה רק את מפות כלי הדם — לא את התמונות המלאות בצבע — כיוון ש-Plus disease מוגדר כמעט אך ורק לפי עובי ועיקול כלי הדם.
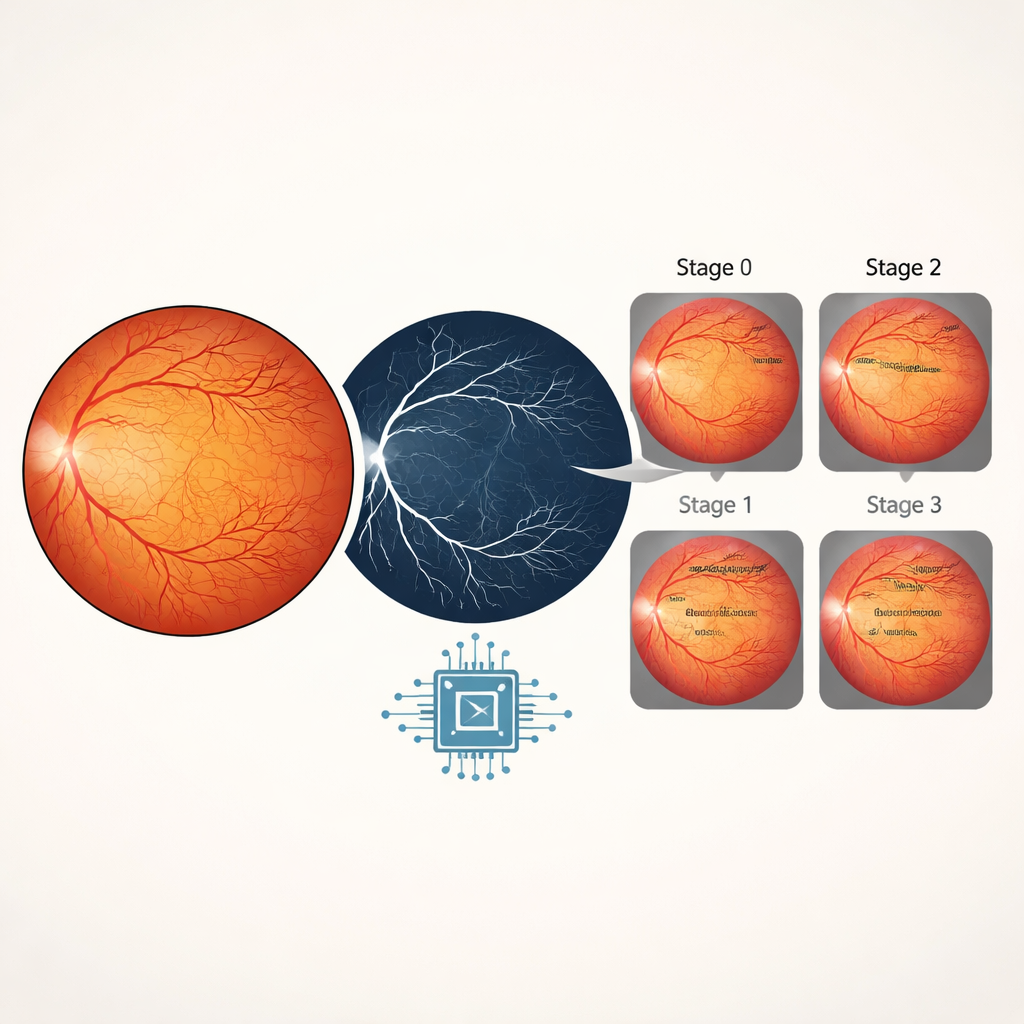
לימוד הרשת לדרג את חומרת המחלה
להערכת שלב ה-ROP ה-AI נזקק ליותר מצורת כלי הדם בלבד. המערכת שילבה לכן את תמונות הרשתית הצבעוניות המקוריות עם מפות כלי הדם המתאימות להן, מה שנתן למודל גם תמונה כוללת של הרשתית וגם מיקוד מחודד בכלי הדם. הצוות בדק מספר גבי למידה עמוקה ידועים ומצא שמודל בשם EfficientNetB4 הציע את האיזון הטוב ביותר בין דיוק ליעילות. על תמונות וולידציה שלא שימשו באימון, גלאי Plus disease הגיע לדיוק של 99.6 אחוז, בעוד שמסווג השלבים השיג דיוק של 98 אחוז עבור שלבים 0 עד 3. בדיקות נוספות, כולל עקומות דיוק-טריפה (precision-recall) ועקומות ROC, הראו שהמודל שומר על רגישות גבוהה (נדיר שיחמיץ מחלה) וספציפיות גבוהה (נדיר שיעורר אזעקות שווא), אף על פי ש-Plus disease היה נדיר יותר מתמונות תקינות.
מביטים בתוך ה"תיבה השחורה"
מפני שרופאים חייבים להאמין לכל כלי המשפיע על החלטות טיפול, המחברים בדקו כיצד ה-AI מקבל את החלטותיו. באמצעות שיטות ויזואליזציה כמו t-SNE הם הראו שתמונות מהקטגוריות השונות (למשל Plus מול תקין או שלב 1 מול שלב 3) יצרו אשכולות מופרדים היטב במרחב התכונות הפנימי של המודל. בטכניקות מפות חום בשם Grad-CAM הם הדגימו אילו חלקים בכל רשתית השפיעו חזק ביותר על תחזית. עבור Plus disease המודל התמקד באזורים שבהם כלי הדם היו רחבים או מסולסלים בצורה בלתי רגילה, בהתאמה למה שמומחים מחפשים. עבור דירוג השלבים המודל גם שם לב לאזורים אחרים כמו דיסק הראייה והמקולה, מה שמעיד שהנימוק שלו תאם באופן הדוק קריטריונים רפואיים מבוססים ולא ארטיפקטים מקריים בתמונה.
מה זה אומר לתינוקות ולמרפאות
במילים פשוטות, עבודה זו מראה שמערכת AI מתוכננת בקפידה יכולה לקרוא תמונות רשתית של תינוקות פגים ברמת דיוק הקרובה למומחה, הן לזיהוי שינויים מסוכנים בכלי הדם והן להערכת התקדמות המחלה. המחקר נערך במרכז רפואי יחיד וכלל רק שלבים מוקדמים עד בינוניים, ולכן נדרשים ניסויים רחבים יותר בבתי חולים מרובים ונתונים מהמקרים המתקדמים יותר. עם זאת, התוצאות מרמזות שעם אימות נוסף ושילוב זהיר בפלטפורמות טלה-רפואה, כלים כאלה יכולים לעזור למערכות בריאות עמוסות לסקר הרבה יותר תינוקות בעקביות רבה יותר ובעלות נמוכה יותר. משמעות הדבר יכולה להיות טיפול מוקדם יותר וסיכוי טוב יותר לשימור הראייה עבור חלק מהחולים הפגיעים ביותר בטיפול הנאונאטלי.
ציטוט: Vahidmoghadam, M., Ghorbani, P., Ahmadi, M.J. et al. Automated diagnosis of plus form and early stages of ROP using deep learning models. Sci Rep 16, 7234 (2026). https://doi.org/10.1038/s41598-026-37064-2
מילות מפתח: רטינופתיה של הפגות מוקדמת, בינה מלאכותית, למידה עמוקה, דימות רפואי, מחלת עין נאונאטלית