Clear Sky Science · he
תת‑אוכלוסייה של נויטרופילים פרו‑דלקתיים מייצרת פגיעה איסכמית‑שיחזורית במעי דרך נתיב מתח הרטיקולום־אנדופלסמי המתווך על‑ידי ATF4
כשזרימת דם פוגעת במעי
מנתחים ורופאי טיפול נמרץ התלבטו זמן רב על פרדוקס מסוכן: כשהאספקת הדם למעי נקטעת ואז משוחזרת, עצם שחזור הזרימה יכול להזיק קשות לרירית המעי. תהליך זה, הנקרא פגיעה איסכמית‑שיחזורית של המעי, עלול להוביל לסיבוכים מאיימי‑חיים כמו זיהום דם וכישלון רב‑איברי. המחקר שמתואר כאן מגלה שלא כל תאי החיסון המהווים תגובה הם שווים — תת‑קבוצה אחת של תאי דם לבנים אגרסיביים במיוחד ממלאת תפקיד מרכזי בהפיכת תגובה מצילת חיים לנזקית.
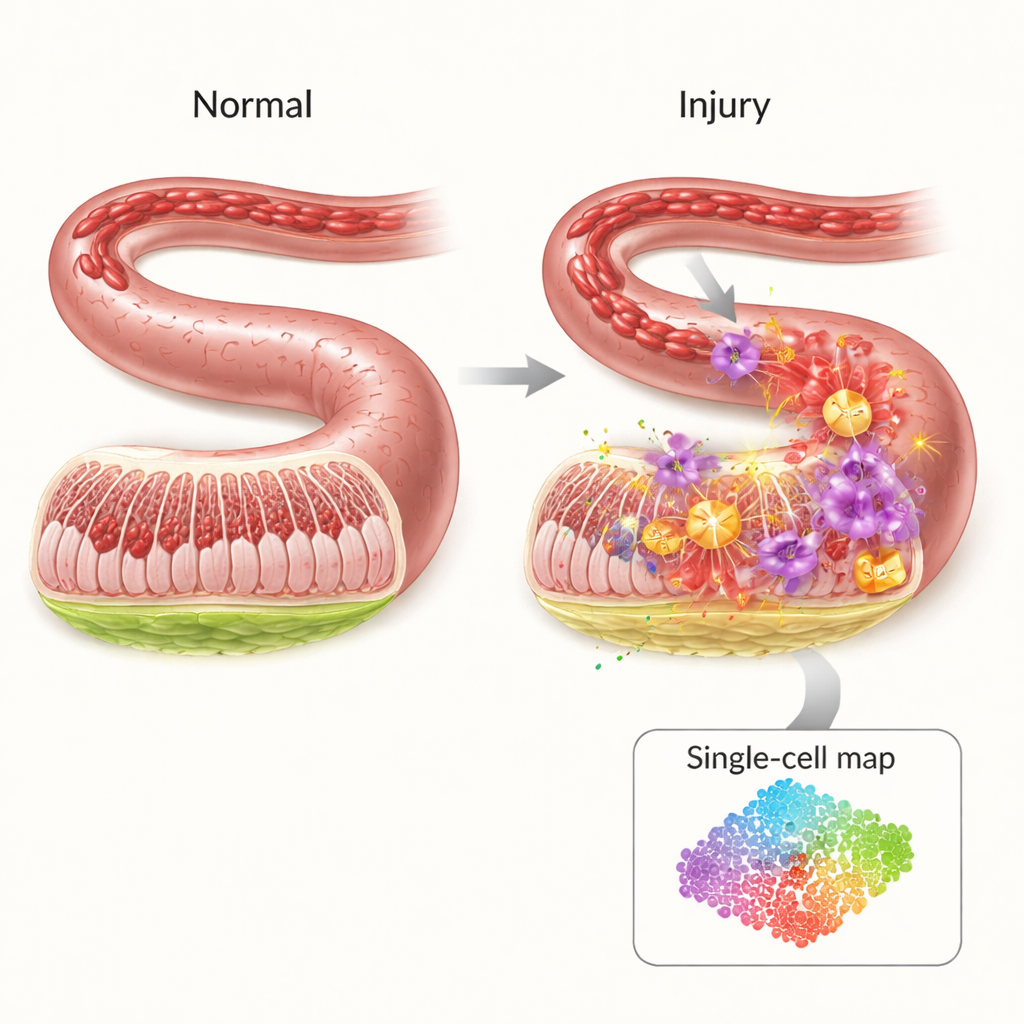
החומה המגנה השברירית של המעי
הפנים של המעי מצופה במחסום דק אך מאורגן היטב שמגן על הגוף מפני חיידקים ורעלנים ומאפשר מעבר של חומרים מזינים. כאשר זרימת הדם מופרעת — למשל בזמן הלם, ניתוח גדול או טראומה קשה — המחסום הזה נותר חסר חמצן. מפתיע לראות שרוב הנזק אינו מתרחש בזמן חוסר הדם עצמו אלא כאשר המעגל חוזר לפעולה. הפרץ הפתאומי של חמצן ותאי חיסון משחרר סערת אותות דלקתיים ומולקולות תגובתיות שיכולות לחורר את דופן המעי ולגרום לדליפה של פתוגנים למחזור הדם. על אף חשיבותו הקלינית, לרופאים כיום יש מעט טיפולים ממוקדים למניעת המפל של אירועים זה.
התמקדות בתאים בודדים
כדי לחשוף מי עושה מה במהלך המשבר הזה, החוקרים השתמשו בריצוף RNA בתא‑יחיד, טכניקה שקוראת אילו גנים פעילים באלפי תאים בודדים במקביל. במודל עכבר של איסכמיה‑שיחזור במעי הם השוו מעיים פגועים לבריאים ומיפו 19 סוגי תאים עיקריים. הם מצאו שתאי חיסון מסוימים — במיוחד נויטרופילים ומונוציטים דלקתיים — התרחבו באופן דרמטי לאחר הפגיעה, בעוד שתאים מגן כגון תאי T, תאי B ותאי Natural Killer הופחתו. גם רשתות התקשורת בין סוגי התאים השתנו, כאשר נויטרופילים בלטו כצמתים מרכזיים שמשדרים ומקבלים מאותות דלקת רבים, מה שמצביע עליהם כגורמי מפתח בנזק.
תת‑קבוצה מזיקה של תאי המגיב הראשון
נויטרופילים הם מהנגרים המהירים של הגוף, שנעים דרך מחזור הדם להתמודדות עם זיהומים ולניקוי שאריות. אך המחקר מראה שבתוך אוכלוסיית הנויטרופילים קיימת תת‑קבוצה אגרסיבית שאחראית לרוב הנזק הצדדי במעי. כאשר המדענים השמיטו נויטרופילים בעכברים לפני גרימת איסכמיה‑שיחזור, לבעלי החיים נצפו פחות התקצרויות במעי, רמות נמוכות יותר של סמני פגיעה בדם, מראה רקמתי טוב יותר במיקרוסקופ וחלבוני אטימה חזקים יותר ברירית המעי. בניסויים של קו‑תרבית, נויטרופילים שהופקו מעכברים פגועים פגעו ישירות בתאי המעי — הורידו את הישרדותם, הגדילו מוות תאי והפריעו לחלבוני "רוכסן" מרכזיים ששומרים על שלמות המחסום המעי.
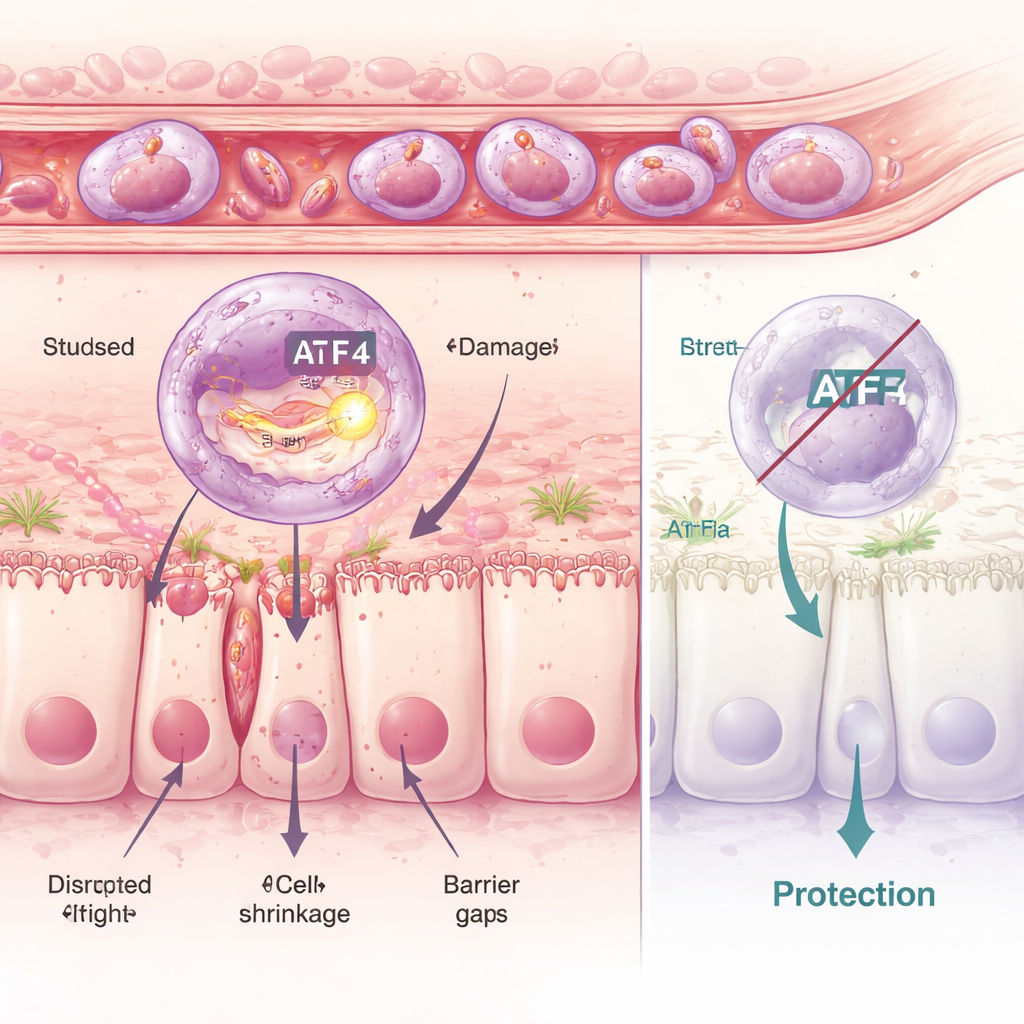
מתח בתוך התאים: כשהבקרה האיכותית מתקלקלת
בהתעמקות נוספת בחנו החוקרים נויטרופילים אחד‑אחד וזיהו שש תת‑קבוצות שונות. אחת מהן, שכונה אשכול C5, בלטה בפרופיל דלקתי חזק ובהפעלת תוכנית מולקולרית של מתח בתוך מבנה הנקרא רטיקולום‑אנדופלסמי, סדנת קיפול החלבונים של התא. בקרה מרכזית של תוכנית זו מופעלת על‑ידי החלבון ATF4. בתאים המזיקים מסוג C5, ATF4 וגני המטרה שלו היו פעילים מאוד. באמצעות תרופות שהגבירו או דיכאו את תגובת המתח הפנימית הזו הצוות הראה שעצמת המתח קשורה לעוצמת הנזק במעי — הגברה של המתח הגדילה את הנזק, וחסימתו שמרה על שלמות המחסום. עכברים מהונדסים גנטית חסרי ATF4 הוגנו במידה ניכרת: גם כאשר נתנו להם תרופות המעוררות מתח, נויטרופיליהם לא יכלו עוד לבצע במלואם את תוכנית הנזק, ורירית המעי נשמרה במידה רבה יותר.
מה משמעות הדבר לטיפולים עתידיים
ביחד, הממצאים מציירים תמונה ברורה לקהל הרחב: בין ההמון של תאי החיסון השוטפים את המעי כשזרימת הדם חוזרת, תת‑קבוצה מסוימת של נויטרופילים המוכנה למתח פועלת כמו צוות ניקיון מוגזם שמחריב את הבניין יחד עם הפסולת. כושר ההרס שלהם תלוי בנתיב מתח פנימי הנשלט על‑ידי ATF4 בתוך התאים. השקטת נתיב זה — מבלי להשליט חיסול מוחלט של כל הנויטרופילים — עלולה להציע דרך להגן על המעי באירועים בסיכון גבוה כמו ניתוחים גדולים, זיהומים קשים או טראומה. אף שמחקר נוסף נדרש כדי לאשר את הממצאים בבני אדם ולמצוא תרופות בטוחות ומדויקות, המחקר פותח מסלול מבטיח לעבר טיפולים שישמרו את מחסום המעי כשהמטופלים זקוקים לו ביותר.
ציטוט: Yang, Y., Zhou, Q., Liu, S. et al. A pro-inflammatory neutrophil subpopulation drives intestinal ischemia–reperfusion injury via the ATF4-mediated endoplasmic reticulum stress pathway. Sci Rep 16, 6117 (2026). https://doi.org/10.1038/s41598-026-36938-9
מילות מפתח: מחסום המעי, איסכמיה‑שיחזור, נויטרופילים, מתח ברטיקולום‑אנדופלסמי, ATF4