Clear Sky Science · he
ננוליפוזומים ממושכי מחזור מצומדי פפטיד CKAAKN להובלה ממוקדת של אורידונין לסרטן הלבלב
מדוע המחקר הזה חשוב
סרטן הלבלב הוא אחד הסרטנ�ים הקטלניים ביותר, חלקית כי הוא בדרך כלל מאובחן בשלב מאוחר ולעתים קרובות עמיד לכימותרפיה סטנדרטית. במחקר זה נבדקת שיטה חכמה יותר להובלת תרופה אנטי‑סרטנית שמקורה בצמחים, אורידונין, ישירות לגידולי הלבלב באמצעות בועיות שומן זעירות הנקראות ננוליפוזומים. על‑ידי סיוע לכך שיותר מהתרופה יגיע אל הגידול תוך שמירה על רקמות בריאות, העבודה מצביעה על אפשרויות טיפול עדינות ויעילות יותר לסרטן שזקוק לכך בדחיפות.
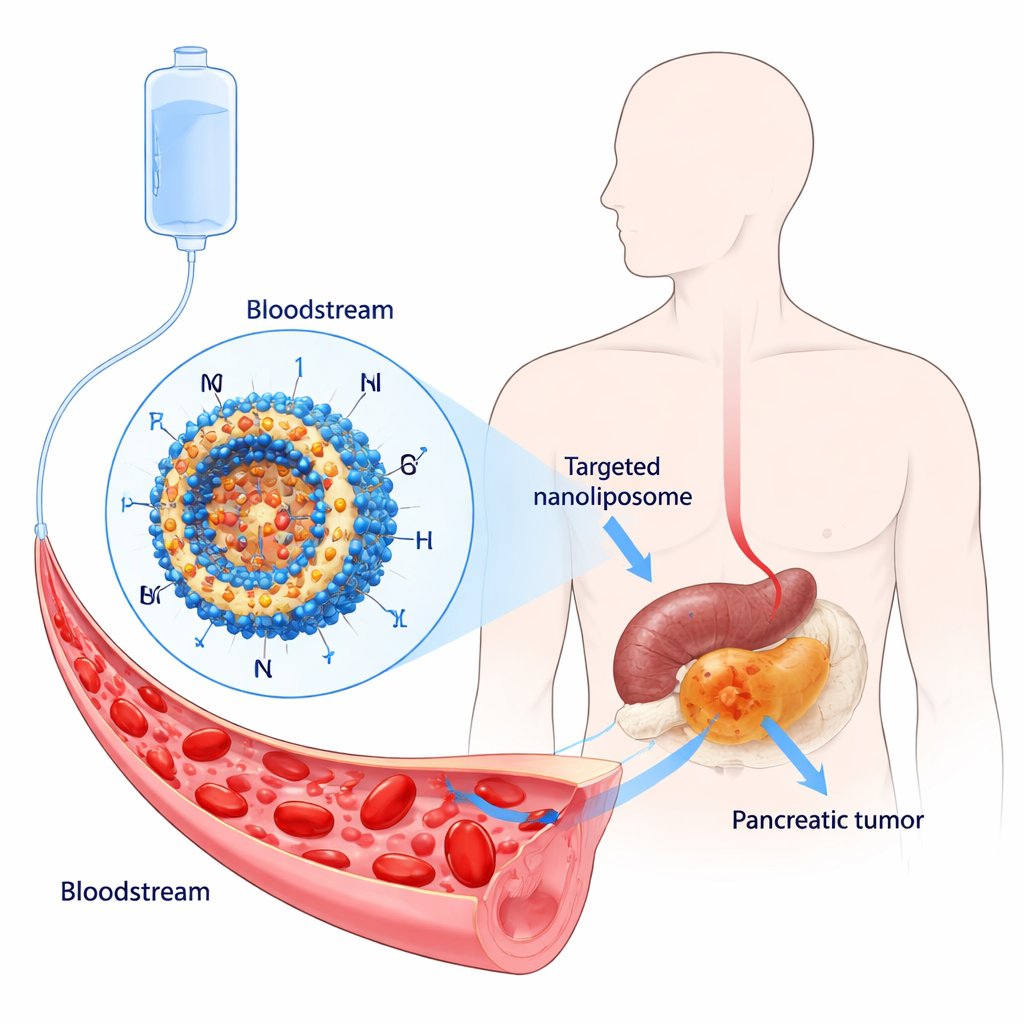
סרטן קטלני שקשה לטפל בו
סרטן הלבלב הרוויח את הכינוי הקודר «מלך הסרטנים» משום ששיעורי ההישרדות נשארים בספרות היחידות עבור רוב המטופלים. רק אחוז קטן מהאנשים זכאים לניתוח, ואף אז רבים מהגידולים חוזרים. תרופות כימותרפיות כגון פקיטקסל וציספלטין יכולות להאט את המחלה, אך הן גורמות לתופעות לוואי קשות ולעתים הגידולים מפתחים עמידות. לכן החוקרים מחפשים תרופות שיהיו מדויקות ופחות רעילות, יחד עם מערכות הובלה היכולות לרכז את התרופה בתוך הגידול במקום להציף את כל הגוף.
הפיכת מולקולה צמחית לתרופה מודרנית
אורידונין הוא תרכובת טבעית המופקת מהצמח הרפואי הסיני המסורתי Rabdosia rubescens. מחקרים במעבדה הראו כי היא מסוגלת להמית או להאט את גדילתם של סוגים רבים של תאי סרטן, כולל תאי לבלב, על ידי התערבות בחלוקת התאים והפעלת תהליכי מוות תאי מתוכנתים. עם זאת, אורידונין כשלעצמה קשה לשימוש כתרופה: היא לא מתמוססת היטב במים, נספגת בצורה לקויה ויכולה להיות רעילה במינונים גבוהים. כדי לממש את הפוטנציאל שלה, המחברים שיקמו את אורידונין בתוך ננוליפוזומים—כדורים זעירים עשויים ליפידים דומים לאלו בממברנות התא—שנועדו לשאת את התרופה בבטחה בדם ולשחרר אותה באיטיות באתר הגידול.
עיצוב אריזה "חסרת זיהוי" והמכוונת לגידול
הקבוצה תכננה מערכת הובלה דו‑שכבתית. תחילה ייצרו ליפוזומים ממושכי מחזור על ידי ציפוי פני השטח שלהם בפוליאתילן גליקול (PEG), פולימר גמיש הידרופילי המסייע לחלקיקים להסתירם מתאי מערכת החיסון ולהישאר במחזור הדם זמן רב יותר. לאחר מכן הוסיפו פפטיד קצר, CKAAKN, המשמש כתג כיוון עבור סרטן הלבלב. פפטיד זה מחקה חלק מאיתות Wnt, שנוטה להיות פעיל בצורה חריגה ברבים מהגידולים הלבלביים, מה שמאפשר לליפוזומים המותאמים (הנקראים ORI@CPD-Lipo) להתמקד בתאי סרטן הפונים לקולטנים מתאימים. החלקיקים הסופיים היו בקוטר של כ‑100 ננומטר, נשאו כמויות גבוהות של אורידונין ושחררו את התרופה לאט במשך שעות רבות במקום לפתיחה מיידית של כל המטען.
כיצד החלקיקים הממוכנים מתנהגים בתאים ובבעלי חיים
בניסויים בתרביות תאים, הליפוזומים המסומנים ב‑CKAAKN נלקחו בצורה יעילה בהרבה על ידי תאי סרטן לבלב אנושיים בהשוואה לתאי לבלב תקינים, במיוחד בשעות הראשונות של המגע. כאשר נוסף עודף של פפטיד CKAAKN חופשי כמריח, תאי הסרטן ספגו פחות חלקיקים, מה שתומך ברעיון שיש שלב קשירה ספציפי. ליפוזומים ריקים הראו רעילות נמוכה ולא פגעו בתאי דם אדומים, מה שמעיד על בטיחות טובה. בעת טעינה באורידונין, הליפוזומים הממוכנים הרגו תאי סרטן ביעילות רבה יותר מאשר אורידונין חופשי או ליפוזומים ללא כיוון, והאטו באופן חזק יותר את תנועת תאי הסרטן בחציבה על הצלחת. בעכברים הנושאים גידולי לבלב, ליפוזומים ממוכנים שסומנו בפלואורסצנציה הצטברו בגידול למשך עד 48 שעות והצטברו שם יותר מליפוזומים ללא כוונה, בעוד שעדיין נוקו בעיקר דרך הכבד והטחול כפי שמצופה.
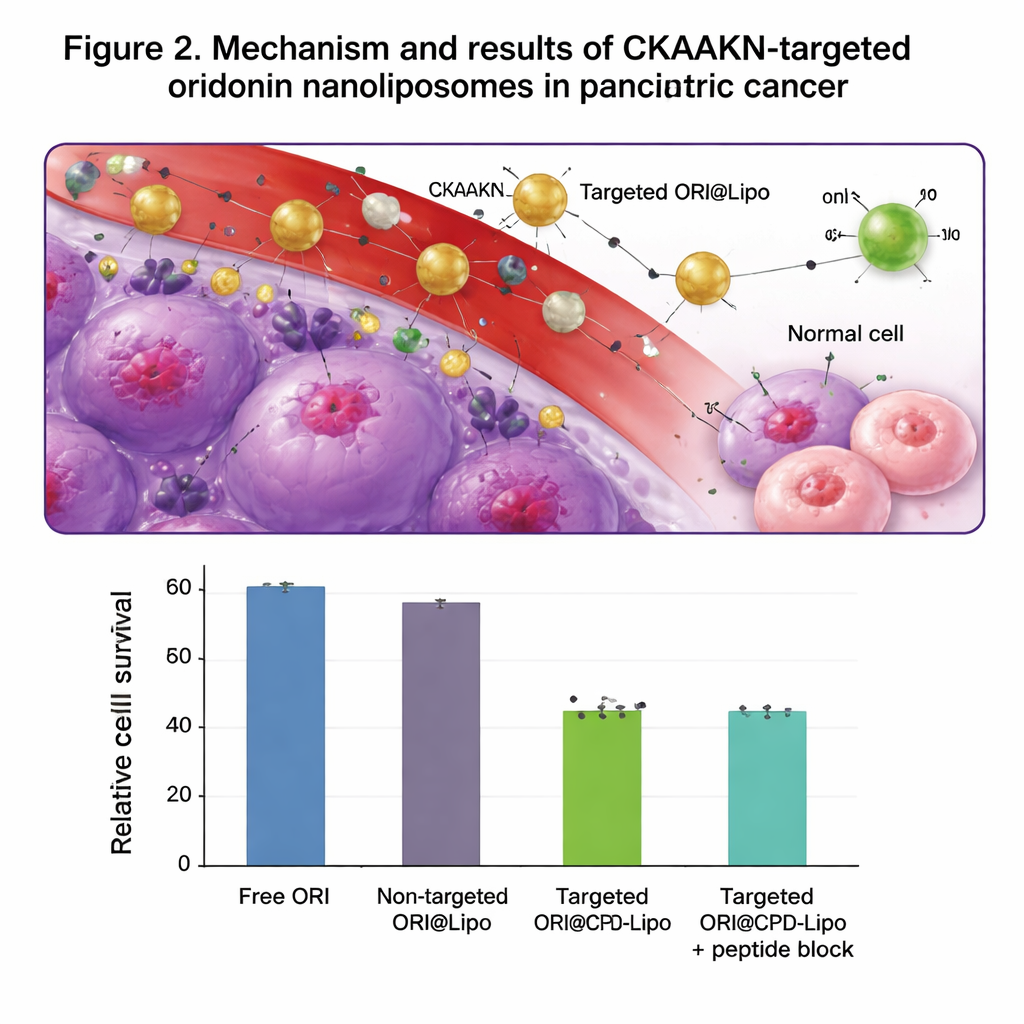
מה זה יכול לומר על טיפולים עתידיים
במכלול, התוצאות מראות ששילוב של תרכובת צמחית מסורתית עם כלי הובלה מודרני ומדויק יכול להגביר משמעותית את העוצמה האנטי‑גידולית שלה במודלים מעבדתיים. הננוליפוזומים הממושכים ומעוטרים ב‑CKAAKN מכוונים יותר אורידונין אל תאי סרטן הלבלב תוך הגבלת החשיפה לרקמות תקינות, מחזקים את מוות תאי הסרטן ומפחיתים תנועה שעלולה להוביל להתפשטות. אף על פי שממצאים אלה עדיין פרה‑קליניים והמחברים מציינים כי נדרשים מחקרים טיפוליים מלאים בבעלי חיים וניסויים קליניים, העבודה מספקת בסיס מוצק לגישות ננו‑רפואיות ממוקדות לסרטן הלבלב ומציעה אסטרטגיה כללית להפיכת מולקולות טבעיות מבטיחות לתרופות המחפשות גידולים.
ציטוט: Zhang, F., Luo, K., Xuan, S. et al. CKAAKN peptide-conjugated long-circulating nanoliposomes for the targeted delivery of oridonin to pancreatic cancers. Sci Rep 16, 6065 (2026). https://doi.org/10.1038/s41598-026-36920-5
מילות מפתח: סרטן הלבלב, ננוליפוזומים, הובלת תרופות ממוקדת, אורידונין, פפטיד המוביל לגידול