Clear Sky Science · he
סינתזה והערכת פעילות אנטי‑סרטנית של נגזרות תיאו‑אימידאזול חדשות הנושאות קבוצת טרימטוקסי־פניל
כלים כימיים חדשים במלחמה בסרטן
תרופות הכימותרפיה פוגעות לעיתים קרובות גם בתאים בריאים לצד הגידולים, והדבר מוביל לתופעות לוואי קשות. המחקר הזה בוחן משפחה חדשה של מולקולות המוכנות במעבדה שמטרתן לפגוע בתאי סרטן ביתר עוצמה ובמיקוד גבוה יותר מרקמה רגילה. על‑ידי שילוב חכם של שתי יחידות כימיות הידועות כיעילות בתרופות, החוקרים יצרו תרכובות שמגלות יכולת חיסול ממוקדת וחזקה של תאי סרטן במודלים מבחנה ובמודלים תלת‑ממדיים של גידולים, תוך השארת תאים בריאים במידה רבה ללא פגע.
בניית מולקולות קטלניות חכמות יותר לסרטן
הצוות התרכז בשתי תבניות כימיות "מועדפות" שמופיעות לעתים קרובות בתרופות מצליחות. האחת היא אימידאזול, טבעת קטנה שמתאימה היטב להרבה מטרות ביולוגיות. השנייה היא קבוצת טרימטוקסי‑פניל (TMP), תבנית של שלוש קבוצות המכילות חמצן על טבעת ארומטית שמרכזית לכמה תרופות אנטי‑סרטניות המפריעות לחלוקת התאים. על‑ידי הכנסת אטום גופרית ללב האימידאזול (יצירת תיאו‑אימידאזול) וקישורו לקבוצת TMP, כימאים קיוו לכוונן את תנועת המולקולות בגוף ואת קשירתן החזקה לחלבונים הקשורים לסרטן. באמצעות מסלול סינתטי בשלבים הם בנו ספרייה של תרכובות קשורות, שכל אחת שונתה במקצת כדי לבחון אילו תכונות הן החשובות ביותר לפעילות אנטי‑סרטנית. 
בחינת תאי סרטן תוך שמירה על רקמות בריאות
התרכובות החדשות נבחנו בארבעה קווי תאים אנושיים של סרטן — אוסטאוסרקומה (עצם), צוואר הרחם, מעי וריאה — וכן בפיברובלסטים ריאתיים לא‑ממאירים. רבות מהתרכובות האטו או עצרו את גדילת תאי הסרטן, אך אחת מהן במיוחד, בשם 13b, בולטת. היא הרגה תאי סרטן בעצם ובצוואר הרחם בריכוזים נמוכים מאוד, ובאותו הזמן לא הראתה רעילות ניתנת לזיהוי כלפי הפיברובלסטים התקינים אפילו במינונים הגבוהים פי יותר מ‑60. כמה תרכובות נוספות היו מבודדות עוצמתית אך פחות סלקטיביות, דבר הממחיש כיצד שינויים מבניים קטנים — כמו הוספת אטום כלור או קבוצת ניטרו בעמדות ספציפיות — יכולים להטות את המאזן בין רעילות רחבה לפעולה ממוקדת בסרטן.
איך התרכובת המובילה דוחפת תאי סרטן להתאבדות
כדי להבין מה 13b עושה בתוך התאים, החוקרים חיפשו סממנים של מוות תאי מתוכנת, כלומר אפופטוזיס. תאי סרטן שטופלו ב‑13b הפכו לחיוביים ל‑Annexin V והפעילו את האנזימים קאספאז‑3 ו‑7, סמנים קלאסיים לכך שהתא נדחף לתוכנית התאבדות מסודרת ולא פשוט התנפץ. במיקרוסקופ נצפו נקודות בוהקות של γH2AX, אות לשבירת גדילי DNA, בגרעיני התאים המטופלים. עם הזמן, השלד הפנימי של התאים החל להתארגן מחדש ולהתפורר, במיוחד בתאי סרטן צוואר הרחם, שהתעגלו והתנתקו — רמזים ויזואליים לכך שאפופטוזיס נמצא בעיצומו. יחד, ממצאים אלה מראים כי 13b פוגע ב‑DNA של תאי הסרטן ואז דוחף אותם לאורך מסלול מות מבוקר.
ממרחובות שטוחות של תאים למיני‑גידולים תלת‑ממדיים
רוב הבדיקות במעבדה מגדלות תאי סרטן בשכבות דקות, שאינן מדמות במלואן את המבנה הצפוף והשכבתי של גידולים אמיתיים. כדי להתמודד עם זה, הצוות גדל את תאי הסרטן לספֵרוֹאידים תלת‑ממדיים — מצבורי כדור קטנים שמדמים טוב יותר את ארכיטקטורת הגידול ואת אתגרי החדירה של תרופות. כאשר ספֵרוֹאידים אלה טופלו ב‑13b, הם התקצרו בהתאם למינון. ספֵרוֹאידים של סרטן העצם היו רגישים במיוחד, והפכו לקטנים, רופפים ומפוררים ברמות תרופה גבוהות יותר. צביעה פלואורסצנטית הראתה גלי אפופטוזיס שנעו מהחוץ אל פנים הספֵרוֹאיד עם העלאת הריכוז, מה שמוכיח כי 13b יכול לחדור ולהרוג תאים לאורך מבנים קומפקטיים אלה. 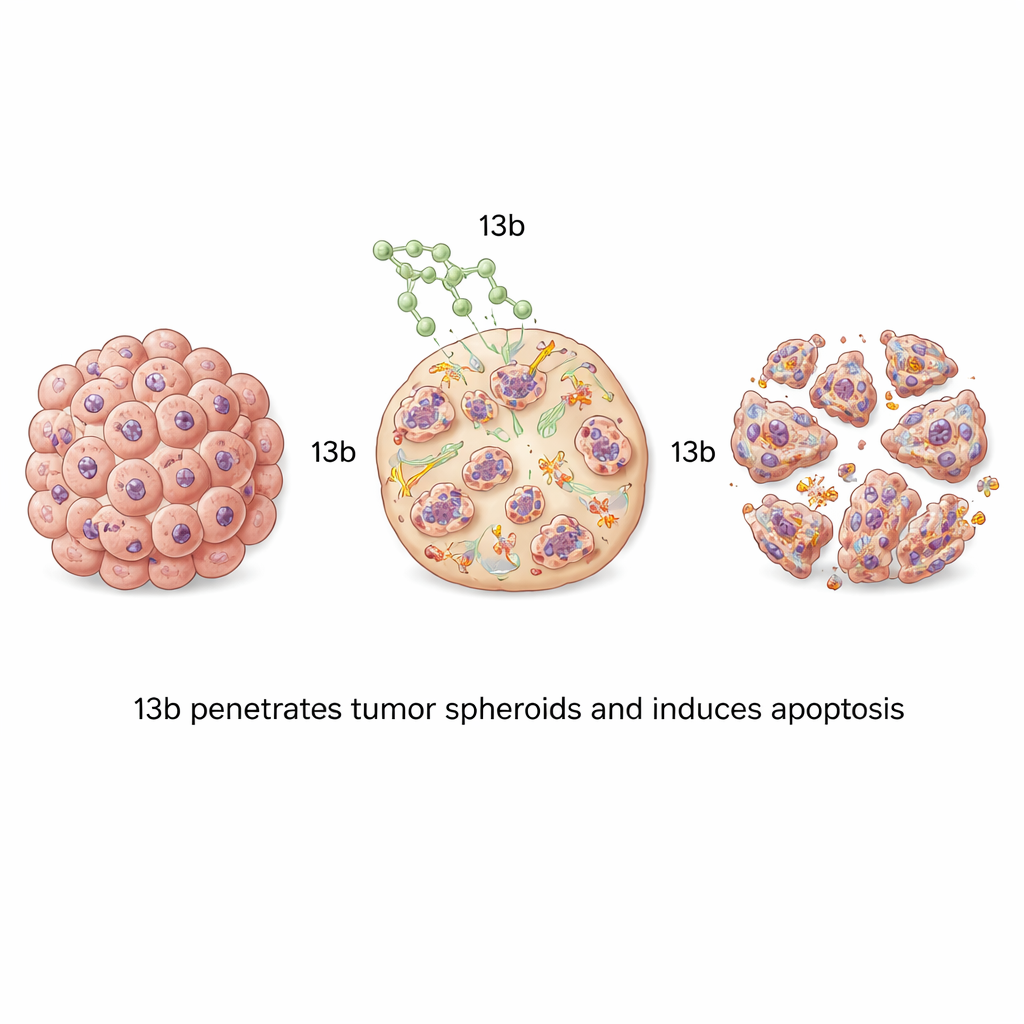
מדוע עבודה זו חשובה לטיפולים העתידיים בסרטן
עבור הקורא הלא‑מומחה, המסר המרכזי הוא שהחוקרים יצרו מחלקה חדשה של מולקולות קטנות שמאגדות את התכונות הטובות של שני רכיבי תרופות מוכחים לעיצוב היברידי אחד. התרכובת המובילה שלהם, 13b, יודעת לזהות ולהשמיד תאי סרטן ביעילות תוך חיסכון יחסי בתאים בריאים בניסויים מעבדתיים, והיא ממשיכה להיות פעילה גם במודלים תלת‑ממדיים ריאליסטיים יותר. למרות שיש עוד עבודה רבה — כמו זיהוי יעדי המולקולה המדויקים, שיפור המסיסות שלה וניסויים בבעלי‑חיים — המחקר מראה ששילוב מסגרות תיאו‑אימידאזול ו‑TMP הוא אסטרטגיה מבטיחה לפיתוח סוכנים אנטי‑סרטניים סלקטיביים ועוצמתיים יותר.
ציטוט: Maciejewska, N., Grybaitė, B., Anusevičius, K. et al. Synthesis and anticancer evaluation of novel thioimidazole derivatives bearing a trimethoxyphenyl moiety. Sci Rep 16, 6271 (2026). https://doi.org/10.1038/s41598-026-36890-8
מילות מפתח: סוכנים אנטי‑סרטניים, נגזרות אימידאזול, טרימטוקסי‑פניל, אפופטוזיס, ספֵרוֹאידים תּוּמּוּר תלת־ממדיים