Clear Sky Science · he
YTHDC1 משנה את הפנוטיפ הממאיר של רטינובלסטומה דרך אוטופאגיה מתווכת על־ידי SQSTM1
מדוע זה חשוב לסרטן העין בילדים
רטינובלסטומה היא סוג הסרטן השכיח ביותר בעין של ילדים קטנים. רופאים יכולים לעתים קרובות לרפא אותה אם היא נתפסת מוקדם, אך ברגע שהגידול מתחיל לחדור לרקמות מסביב לעין או להתפשט לכיוון המוח, הצלת חיי הילד והראייה הופכת הרבה יותר קשה. המחקר חוקר "בלם" מולקולרי בתוך תאי הגידול — שני מולקולות בשם YTHDC1 ו‑SQSTM1 — שנראות כאילו הן מסייעות לשמור על רטינובלסטומה פחות אגרסיבית. הבנת אופן פעולתו של הבלם הזה יכולה לפתוח נתיבים חדשים לטיפולים ממוקדים ועדינים יותר.
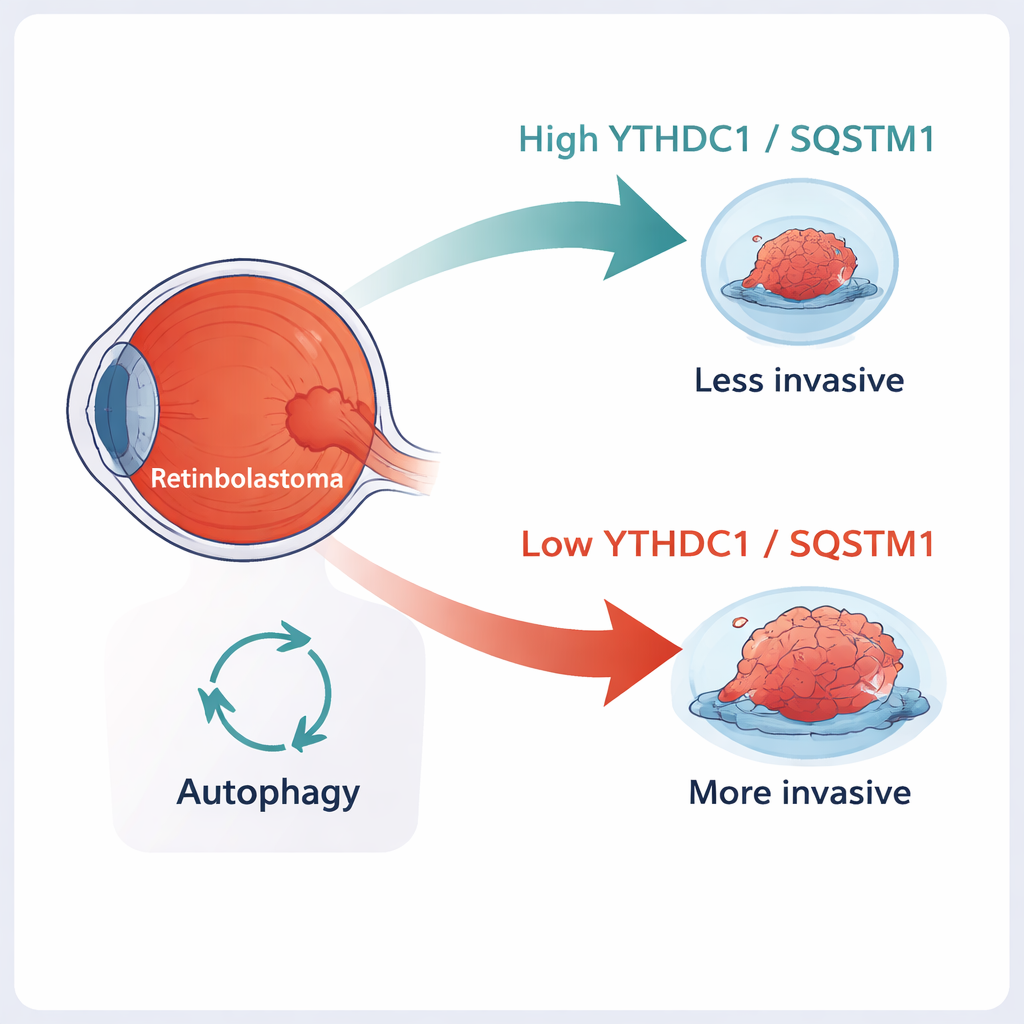
מבט מעמיק על גידולי עין בילדות
רטינובלסטומה נובעת משכבת קולטני האור בעין, הרשתית, בדרך כלל אצל ילדים מתחת לגיל חמש. באופן קלאסי, המחלה מתחילה כאשר שתי העותקים של גן השומר, RB1, אובדים. אך אובדן RB1 לבדו אינו מסביר במלואו מדוע גידולים מסוימים נשארים ממוקמים בתוך העין בעוד שאחרים חודרים לרקמות סמוכות או מתפשטים לאורך העצב הראייתי. יותר ויותר חוקרים מבינים כי תגובות כימיות המוצמדות ל‑RNA — ההודעות החולפות שאומרות לתאים אילו חלבונים לייצר — יכולות להשפיע בעוצמה על התנהגות הסרטן. אחת התגיות הנפוצות היא m6A, שיכולה לשנות כמה יציבות יש להודעות אלו וכמה זמן הן נשארות בתוך התא.
גילוי ה"בלם" המולקולרי החסר
המחברים התחילו בהשוואת פעילות גנטית בגידולים שנשארו בתוך העין לאלה שהפכו כבר לאינוואסיביים. באמצעות מאגר נתוני ריצוף RNA ציבורי של מדגמי רטינובלסטומה, הם זיהו אלפי גנים שהפעילות שלהם שונות בין שתי הקבוצות ואז התמקדו ב"מווסתי" m6A חשובים. אלה כוללים אנזימים שמוסיפים או מסירים m6A וחלבוני "קורא" שמפענחים את התג. מתוך עשרה רגולטורים מרכזיים, הם מצאו כי אחד המלמדים, YTHDC1, היה באופן עקבי נמוך יותר בגידולים פולשניים. כאשר בחנו דגימות מ‑50 ילדים וביצעו מבחנים במעבדה על רקמות הגידול, הם אישרו שרמות YTHDC1 — גם RNA וגם חלבון — היו מופחתות בסרטן האגרסיבי יותר.
בדיקת YTHDC1 בפועל
כדי לראות מה YTHDC1 עושה בפועל, הצוות שינה את רמתו בשתי שורות תאים של רטינובלסטומה אנושית. כאשר הורידו את YTHDC1 באמצעות כלים גנטיים, התאים התרבו מהר יותר והיו מסוגלים לנוע טוב יותר דרך ממברנות מלאכותיות המדמות מחסומי רקמה — סימנים לגידול אגרסיבי יותר. בעכברים, תאים חסרי YTHDC1 יצרו גידולים גדולים וכבדים יותר. ההפך היה נכון גם כן: כיפוף התאים לייצור YTHDC1 נוסף האט את צמיחתם והפחית את יכולתם להגר ולהחדור. ניסויים אלה מצביעים על כך ש‑YTHDC1 פועל כמדכאי גידול, מסייע בעיכוב ההתנהגויות המסוכנות ביותר של רטינובלסטומה.
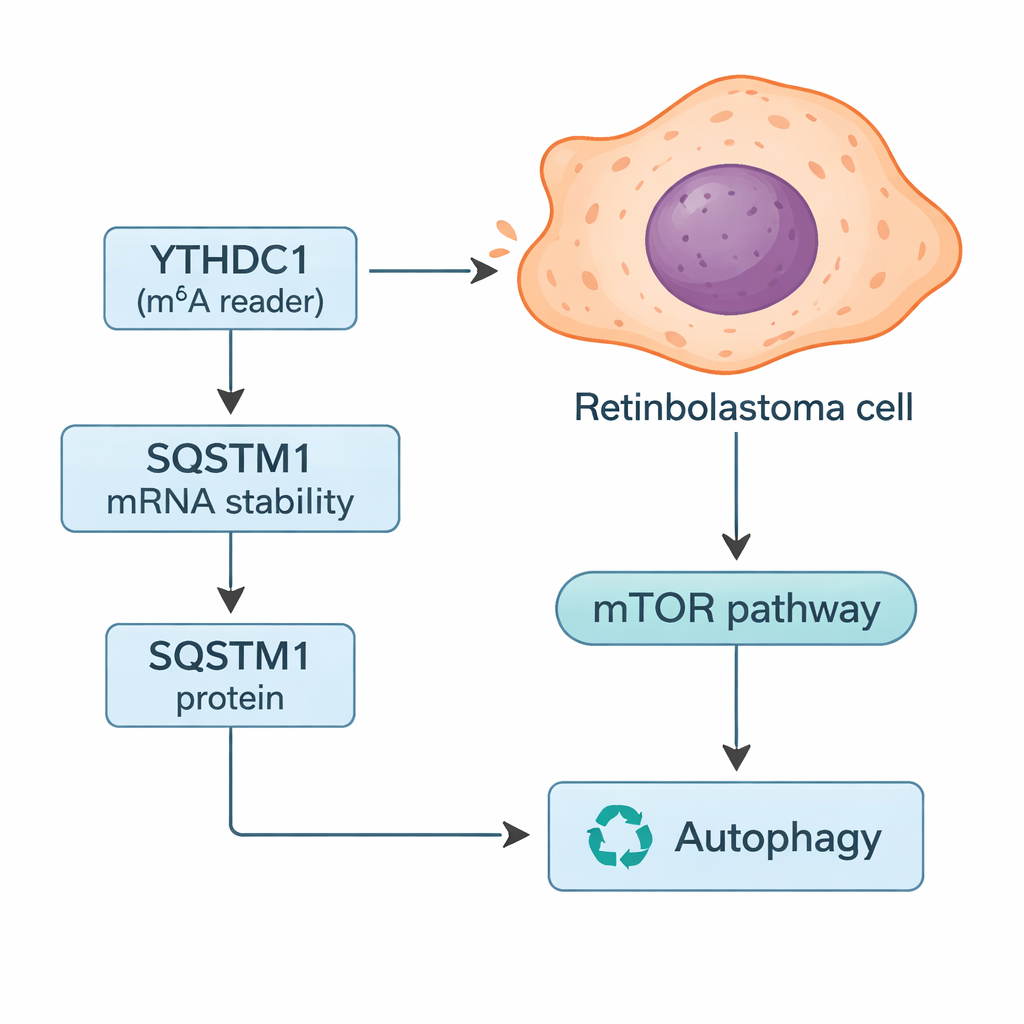
כיצד YTHDC1 שולט במערכת המחזור של התא
בהעמקה נוספת, החוקרים חיפשו גנים ספציפיים שאולי נשלטים על‑ידי YTHDC1. על ידי שילוב חיפושים במאגרי מידע עם נתוני הגידולים שלהם, הם התרכזו ב‑SQSTM1, חלבון הידוע יותר כ‑p62. SQSTM1 עוזר לנהל את האוטופאגיה, מערכת המחזור של התא שמפרקת רכיבים פגומים ויכולה לספק דלק כשמשאבים דלים. המחקר הראה כי YTHDC1 נקשר פיזית ל‑RNA של SQSTM1 ומייצב אותו, מה שמאפשר לייצר יותר חלבון SQSTM1. כאשר YTHDC1 הוקטן, רמות SQSTM1 ירדו וה‑RNA שלו מתפרק מהר יותר. השתקת SQSTM1 לבדה גרמה לתאי רטינובלסטומה לצמוח ולהיות פולשניים יותר, והיא מחקה חלקית את ההשפעות המגוננות שנצפו כאשר YTHDC1 הועשר, מה שממקם את SQSTM1 כשחקן־ביניים מרכזי במסלול זה.
אוטופאגיה, אנרגיה ואגרסיביות של הגידול
מכיוון ש‑SQSTM1 הוא מרכזי לאוטופאגיה, הצוות בדק כיצד שינוי YTHDC1 ו‑SQSTM1 משפיע על תהליך המחזור הזה. באמצעות שילוב של סמנים פלואורסצנטיים ומדידות חלבון, הם מצאו שהפחתה של YTHDC1 או SQSTM1 הגבירה את "הזרימה" האוטופגית — יותר חומר תאי הובל לתוך ומחוץ למערכת הממחזרת. הם גם שימו לב לשינויים במסלול mTOR, מתג חישה של מזון שעוצרת בדרך כלל את האוטופאגיה. עם פחות SQSTM1, פעילות mTOR ירדה, תואם להגברה של האוטופאגיה. במחלת רטינובלסטומה פולשנית, המחברים מציעים כי הפחתת YTHDC1 גורמת לאיתות SQSTM1 מוחלש, ירידה בפעילות mTOR והגברה של האוטופאגיה שמסייעת לתאי הגידול לשרוד לחץ ולהתפשט.
מה זה אומר לטיפולים עתידיים
ללא רקע מיוחד, המסר המרכזי הוא שמחקר זה מזהה שרשרת אירועים בתוך תאי רטינובלסטומה — YTHDC1 ששולט ב‑SQSTM1, אשר מעצב בתורו את מכונת המחזור של התא — שמשפיעה על מידת האגרסיביות של הסרטן. כאשר השרשרת הזו מוחלשת, הגידולים גדלים מהר יותר וחודרים יותר. למרות שנדרש עוד עבודה רבה לפני שממצאים אלה יגיעו לקליניקה, המסלול מציע רעיונות חדשים לטיפול: לשקם את תפקוד YTHDC1, לייצב את SQSTM1, או לכוונן את האוטופאגיה ופעילות mTOR עשויים יום אחד להשלים כימותרפיות קיימות. עבור ילדים המתמודדים עם סרטן עין זה, אסטרטגיות ממוקדות כאלה עשויות לעזור להגביל את התפשטות הגידול תוך שמירה על יותר ראייה והפחתת תופעות הלוואי של הטיפול.
ציטוט: Ding, J., Sun, J., Wang, J. et al. YTHDC1 modulates the malignant phenotype of retinoblastoma via SQSTM1-mediated autophagy. Sci Rep 16, 6292 (2026). https://doi.org/10.1038/s41598-026-36833-3
מילות מפתח: רטינובלסטומה, YTHDC1, SQSTM1, אוטופאגיה, מסלול mTOR