Clear Sky Science · he
אימות קליני של ארכיטקטורות CNN קלות משקל לסיווג רב-מעמדי אמין של סרטן ריאה באמצעות טכניקות הדמיה היסטופתולוגיות
מדוע המחקר הזה חשוב למטופלים ולרופאים
סרטן הריאה לעיתים קרובות קטלני כי הוא מתגלה באיחור או מסווג באופן שגוי, מה שעלול לעכב את הטיפול הנכון. מחקר זה חוקר כיצד תוכנות מחשב קטנות ויעילות—במקום מודלים עצומים הצרכניים באנרגיה—יכולות לזהות באופן אמין סוגים שונים של סרטן הריאה מתמונות מיקרוסקופיות של רקמות. אם כלים קלי־משקל כאלה יעבדו היטב, הם יכולים לשמש בבתי חולים ברחבי העולם, כולל במקומות עם משאבי חישוב מוגבלים, ולתמוך בפתולוגים בקבלת אבחנות מהירות ועקביות יותר.
מבט מקרוב על סרטן במיקרוסקופים דיגיטליים
כאשר נוקר חשוד בריאה מוסר או מבוצעת ביופסיה, פתולוגים בוחנים פרוסות דקות וצבועות של רקמה תחת מיקרוסקופ כדי להחליט האם הן חסרות סכנה או שייכות לאחד מסוגי הסרטן. בעבודה זו המחברים מתמקדים בשלוש קטגוריות מרכזיות: רקמה ריאתית שפירה, אדנוקרצינומה של הריאה, וסרקומה קשקשית של הריאה (squamous cell carcinoma). תתי־הסוגים הללו חשובים מכיוון שהם מגיבים באופן שונה לטיפולים. הצוות משתמש בצילומים דיגיטליים של זכוכיות ההיסטופתולוגיה—תמונות היסטופתולוגיות—ושואל האם רשתות נוירונים קומפקטיות יכולות ללמוד את הדפוסים הוויזואליים העדינים שמבדילים כל קטגוריה, מצורות התאים ועד לארכיטקטורת הרקמה, באמינות הדומה לזו של מודלים גדולים בהרבה.
בניית מסווגים דיגיטליים קטנים אך חכמים יותר
רוב מערכות זיהוי התמונה המתקדמות הן עצומות ודורשות מעבדי גרפיקה יקרים, מה שמקשה על פריסתן במרפאות רבות. החוקרים פיתחו במקום זאת ארבעה מודלים "קלילים" לניתוח תמונות, הנקראים Lite-V0, Lite-V1, Lite-V2 ו‑Lite-V4, כשכל אחד הוא גרסה מזורזת של רשת עצבית קונבולוציונית (CNN). כל הארבעה פועלים לפי מתכון בסיסי זהה: הם מפיקים בהדרגה תכונות חזותיות דרך ערימה של יחידות בנייה פשוטות, מסכמים את התמונה ולבסוף מפיקים אחת משלוש התוויות של רקמת הריאה. מה שמשתנה בין הגרסאות הוא מספר הבלוקים ושיעור הרוחב שלהם—בעצם, כמה קיבולת יש למודל ללמוד דפוסים מורכבים. עיצוב מבוקר זה מאפשר לצוות ללמוד כמה מורכבות באמת נדרשת לסיווג אמין של סרטן.
אימון, בדיקה ובחירת המודל ההוגן ביותר
כדי ללמד ולבדוק את המודלים, המחברים אוספים אוסף מאוזן של 15,000 תמונות של רקמת ריאה, המחולקות בקפידה לקבוצות אימון, ולידציה ובדיקה עם מספרים שווים מכל כיתה. לפני האימון, כל תמונה משנה גודל, מנורמלת ומעוטרת בעדינות עם שיקופים, סיבובים קטנים וזומי על־מנת לדמות איך פרוסות עשויות להיראות בתנאים שונים. באופן קריטי, הצוות לא שופט מודלים לפי דיוק גולמי בלבד, כי מדד זה יכול להסתיר ביצועים רעים עבור כיתה אחת. במקום זאת הם מסתמכים על ציון "מקרו‑F1", שמכריח את המודל להצליח בכל שלוש סוגי הרקמה, ולא רק בקלים ביותר. פרוצדורת אימון מותאמת אישית עוקבת ברצף אחרי ציון מאוזן זה ועוצרת את האימון אוטומטית כשהשיפורים מתייצבים, ושומרת את הגרסה הטובה ביותר של כל מודל להשוואה. 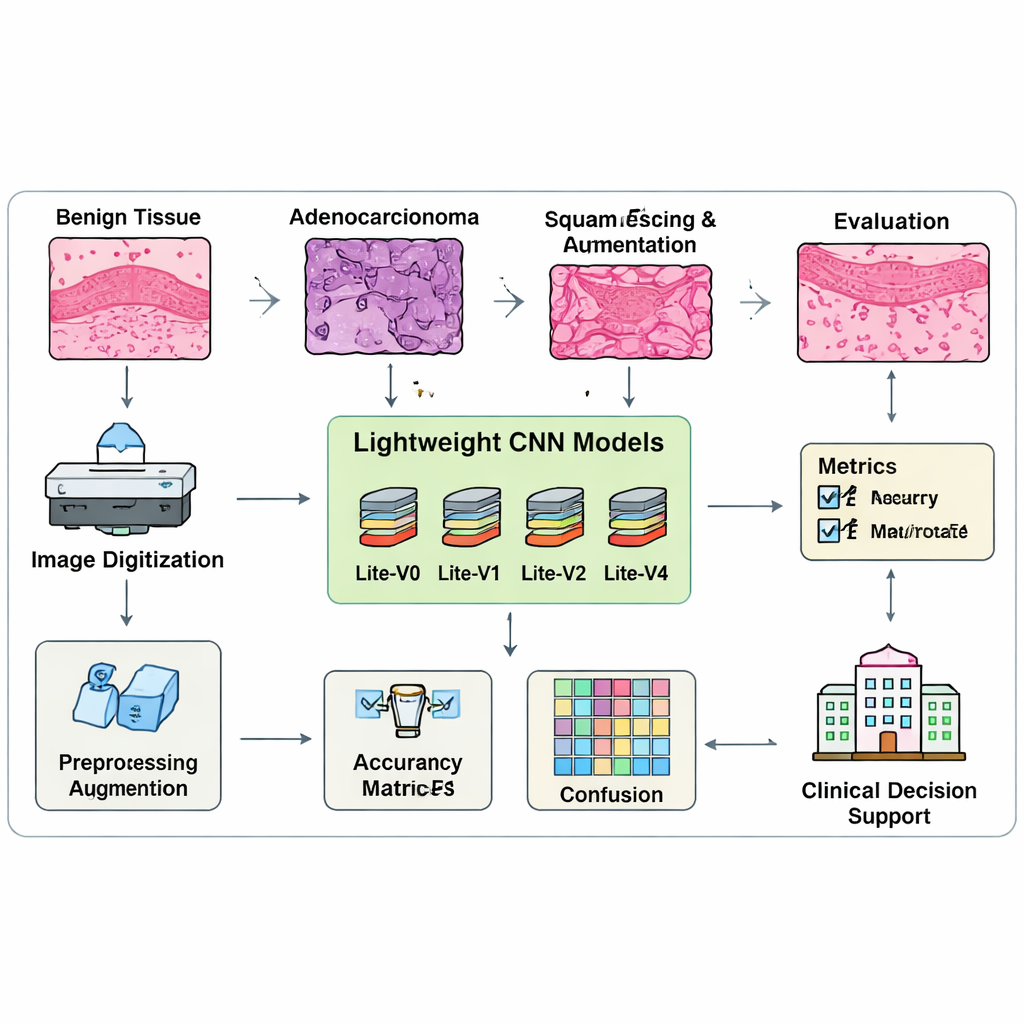
מה המודל הקליל הטוב ביותר יכול באמת לעשות
בסיכום, וריאנט אחד—Lite-V2—בולט במיוחד. הוא לא הרשת הקטנה ביותר ולא הגדולה ביותר, אלא ממוקם באמצע ומשיג את האיזון הטוב ביותר בין דיוק ליעילות. על תמונות מבחן שלא נראו קודם, Lite-V2 מסווג נכון רקמה שפירה, אדנוקרצינומה וקארצינומה קשקשית בביצועים גבוהים ומפוזרים באופן שווה, כשהוא מגיע לציון מקרו‑F1 סביב 0.96. תרשימי מטריצת הבלבול מראים שהוא כמעט ואינו מבלבל בין שלוש הקטגוריות, בעוד שגרסאות עמוקות יותר נוטות "להתאים יתר על המידה" (overfit), לזכור את נתוני האימון אך לאבד אמינות על מקרים חדשים. המחברים מפעילים מחדש את Lite-V2 מספר פעמים עם נקודות התחלה אקראיות שונות ומשתמשים בבדיקה סטטיסטית כדי לאשר שיתרונו על פני הווריאנטים האחרים אינו מקרי. 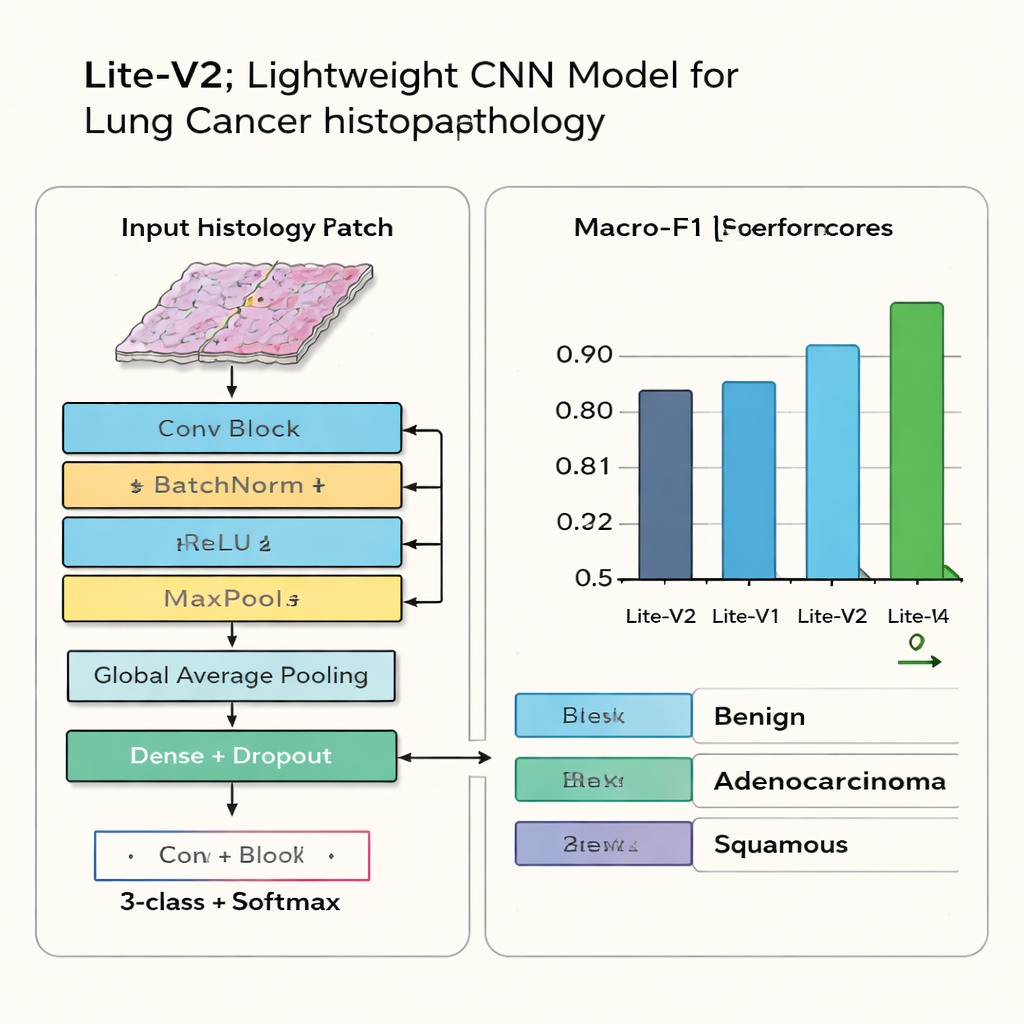
מקודמחקר לתמיכה בעולם האמיתי
מעבר למספרי ביצועים, המחקר מדגיש פריסה מעשית. מאחר ש‑Lite-V2 ואחיו קומפקטיים, הם יכולים לפעול על חומרה צנועה בבתי חולים או אפילו על מכשירי edge ללא צורך בשיגור תמונות רגישות לענן. המחברים מפרסמים מסגרת חזרה על‑ניתוח (reproducible) המתעדת כל פרט ניסויי, מעיבוד הנתונים ועד עקומות האימון ודפוסי השגיאות, כדי שקבוצות אחרות יוכלו לאמת או להרחיב את העבודה. למטופלים ולרופאים, המסקנה המרכזית היא שעיצוב שקול של בינה קלת‑משקל יכול לקדם את הגעת סיווג אמין של סרטן ריאה לשגרת הפרקטיקה ההיסטופתולוגית, ולתמוך בקבלת החלטות מהירה ועקבית יותר—אפילו במרפאות חסרות כוח חישוב משוכלל.
ציטוט: Raza, A., Hanif, F. & Mohammed, H.A. Clinical validation of lightweight CNN architectures for reliable multi-class classification of lung cancer using histopathological imaging techniques. Sci Rep 16, 6512 (2026). https://doi.org/10.1038/s41598-026-36652-6
מילות מפתח: סרטן ריאה, היסטופתולוגיה, רשתות עצביות קונבולוציוניות, בינה מלאכותית בהדמיה רפואית, אבחון בעזרת מחשב