Clear Sky Science · he
ניקוטינאמיד מנטרל פגיעה מיטוכונדריאלית ועיכוב נוירונלי שנגרמים על־ידי רוטנון במודל תרגומי של תקופת חיים מוקדמת
מדוע מנועי התא הזעירים חשובים למוח המתפתח
במהלך התפתחות המוח, מיליארדי תאי עצב צעירים צריכים לגדול ענפים ארוכים וליצור חיבורים מדויקים. המחקר בוחן כיצד "תחנות הכוח" של התא — המיטוכונדריות — מעצבות את התהליך הזה ומה קורה כשהן מורעלות בעדינות על ידי תרכובת בדומה לחומר קוטל־חרקים. החוקרים גם בודקים האם מולקולה נפוצה הקשורה לוויטמינים, ניקוטינאמיד, יכולה להגן על תאי מוח מתפתחים מפני הלחץ האנרגטי החבוי הזה, עם השלכות אפשריות למצבים כמו סקיזופרניה.
ממודל קוטל־חרקים לניסוי בתאי מוח
הצוות בנה על עבודות קודמות שהראו כי חולדות צעירות שנחשפו זמנית לרוטנון, קוטל־חרקים החוסם שלב מרכזי בייצור אנרגיה מיטוכונדריאלי (קומפלקס I), מפתחות מאוחר יותר התנהגויות המזכירות סקיזופרניה. כדי להבין מה קורה ברמת התא הבודד, הם בודדו תאי עצב לא בשלים מקורטקס של חולדה וחשפו אותם לריכוז המדויק של רוטנון שנמדד במוחות בעלי־החיים. גישה "תרגומית" זו אפשרה לשאול: במינונים נמוכים ריאליסטיים שאינם הורגים תאים, האם רוטנון עדיין משבש את הדרך שבה נוירונים צומחים ומתחברים?
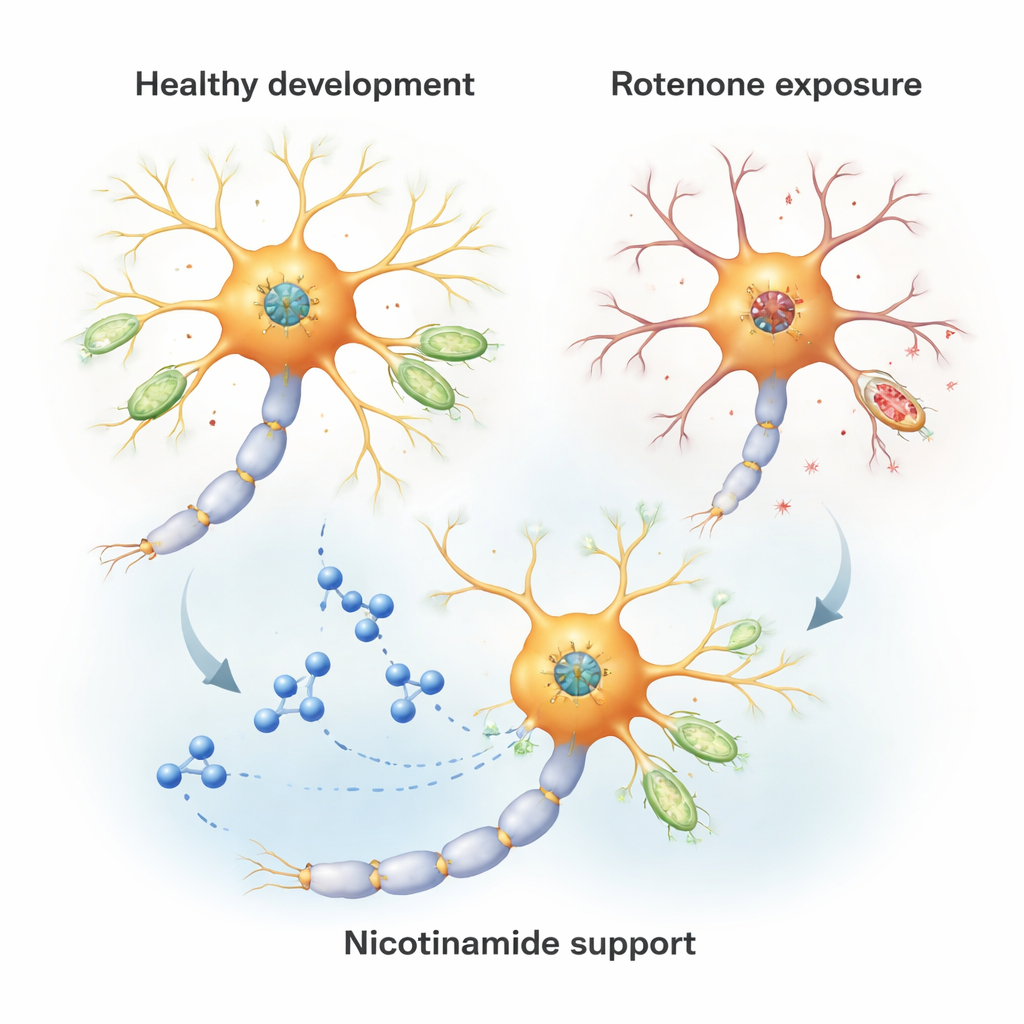
אטימת אנרגיה ללא מוות תאי גלוי
למפתיע, מינון הרוטנון הנמוך לא גרם למוות של הנוירונים ולא שיבש את מאזן הסידן הבסיסי או את המטען החשמלי על ממברנת המיטוכונדריה — תופעות שבדרך כלל נצפות במצוקה אקוטית של תאים. במקום זאת נוצר שינוי שקט אבל חשוב במטבוליזם. המיטוכונדריות ייצרו פחות אנרגיה (ATP) וצרכו פחות חמצן, ופעילות הקומפלקס I ירדה. במקביל, תוצר של ריאקטיביות מסוימת, סופראוקסיד מיטוכונדריאלי, ירד במקום לעלות. ממצא זה מנוגד למחקרים עם מינונים גבוהים של רוטנון, שמדווחים בדרך כלל על קפיצה רעילה בסוגי חמצן תגובתיים. כאן התמונה היא של "מנוע איטי" ולא של מנוע מעשן ומתחמם מדי.
שינויים בבקרת איכות ובצורת התא
כאשר ביצועי המיטוכונדריה מתערערים, תאים בדרך כלל משנים צורה ומחזרים את האורגנלות האלה. החוקרים מצאו סימנים שמערכת בקרת האיכות הזאת הופרעה. חלבונים המעורבים בחיתוך ובשחזור מיטוכונדריות, וכן כאלה המסמלים כמה מיטוכונדריות קיימות, השתנו לאחר החשיפה לרוטנון. רכיבים של מסלול המחזור התאי (אוטופאגיה) גם הצטברו בדפוסים שמרמזים שחבילות הפסולת נוצרו אך לא נוקו ביעילות. במקביל, הנוירונים עצמם הפכו לפשוטים יותר במבנם: הדנדריטים, הדמויי־עץ, קוצרו ופחתו במספרם. מכיוון שדנדריטים חיוניים לקבלת אותות, ההתמעטות הזו מרמזת שגם לחץ מיטוכונדריאלי קל כרוני יכול להשאיר חותם ארוך טווח על מעגלי המוח.
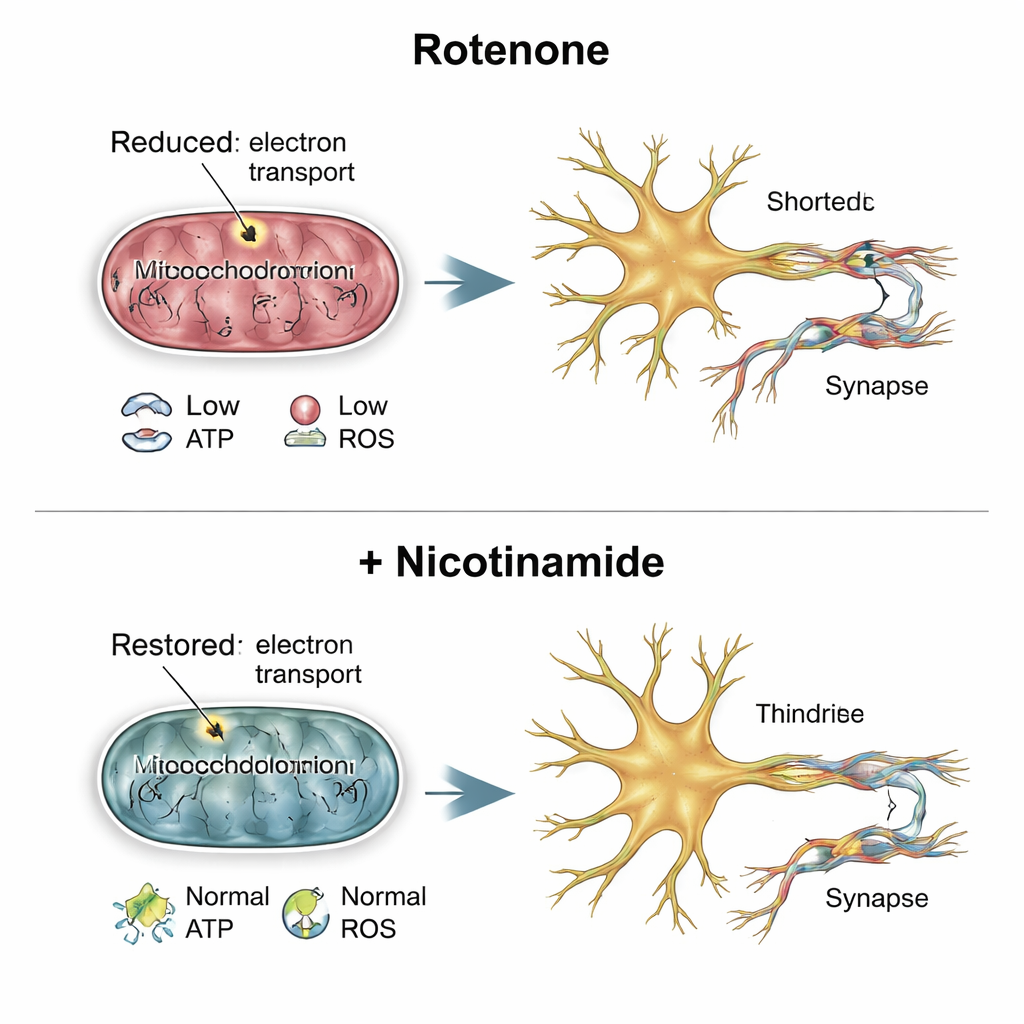
סינפסות מוחלשות וכיצד ניקוטינאמיד מסייע
הצוות חקר לאחר מכן האם נקודות התקשורת בין הנוירונים — הסינפסות — הושפעו. באמצעות סימנים זוהרים לחלבוני פרה־ופּוסט־סינפטיים, הם ראו כי הנוירונים שטופלו ברוטנון הצטברו בהם יותר רכיבים סינפטיים אך הייתה בין הרכיבים התאמה לקויה, דבר שמרמז שהמכונות נערמות בלי ליצור חיבורים פונקציונליים מלאים. הכנסת ניקוטינאמיד לפני החשיפה לרוטנון שינתה את התמונה. ניקוטינאמיד, אבני־בניין למולקולת האנרגיה NAD, השיב את הנשימה המיטוכונדריאלית, רמות ה‑ATP ותפוקת הסופראוקסיד לכיוון ערכים נורמליים. הוא גם נרמל סימני מחזור תאי, הקטין את הצטברות החלבונים הסינפטיים החריגה, שיפר את ההתאמה ביניהם והחזיר את מספר ואורך הדנדריטים לרמות דומות לאלה של תאים שלא טופלו.
מה משמעות הדבר להפרעות מוחיות
במכלול, התוצאות מציעות שגם פגיעות מתונות ולא קטלניות לתפקוד המיטוכונדריה במהלך החיים המוקדמים יכולות להתפשט ולפגוע בצורת הנוירון וביצירת הסינפסות — תהליכים הנחשבים לשונים בהפרעות כמו סקיזופרניה. ניקוטינאמיד לא איפס את כל השינויים המולקולריים באופן קסום, אך הספיק כדי להציל את מאזן האנרגיה, מערכות הניקוי, הארכיטקטורה הדנדריטית והארגון הסינפטי במודל התרביתי הזה. עבור הקורא הכללי, המסר המרכזי הוא שהשימור על "תחנות הכוח" של התא בריאות בתקופת ההתפתחות עשוי להיות מכריע לבניית מעגלי מוח חזקים, ותמיכה בדרכי הדלק המיטוכונדריאליות עם מולקולות הקשורות לוויטמין B3 יכולה להיות דרך להתמודד עם פגיעות מוקדמות עדינות. אמנם נדרשת עבודה רבה לפני שניתן יהיה לשקול טיפול באנשים, אך המחקר מספק גשר מכוניסמי בין חשיפות סביבתיות, לחץ מיטוכונדריאלי ובריאות מוחית לטווח הארוך.
ציטוט: Siena, A., Souza e Silva, L.F., Araujo, V.C. et al. Nicotinamide counteracts Rotenone-induced mitochondrial and neuronal dysfunction in a translational early-life model. Sci Rep 16, 7159 (2026). https://doi.org/10.1038/s41598-026-36651-7
מילות מפתח: מיטוכונדריה, התפתחות המוח, סקיזופרניה, ניקוטינאמיד, רוטנון