Clear Sky Science · he
הכוח הטיפולי והמנגנון המשויך של דינואקסנטין במודלים ניסיוניים של מחלת חניכיים בחיות ובתאים
מדוע חשוב להגן על החניכיים
דימום מהחניכיים ושיניים רופפות עשויים להיראות כטרדות מינוריות, אך דלקת חניכיים כרונית, או פריודונטיטיס, יכולה באופן שקט לשחוק את העצם שמחזיקה את השיניים ואפילו להשפיע על הבריאות הכללית. מחקר זה בוחן פיגמנט אנטי‑אוקסידנטי טבעי בשם דינואקסנטין, המיוצר על‑ידי חיידק יוצא דופן בעמידותו, כדי לראות האם הוא יכול להגן על החניכיים והלסת מנזק במודלים ניסיוניים של מחלת חניכיים קשה.
מולקולה צבעונית ועוצמתית
דינואקסנטין הוא פיגמנט קרוטנואידי צהוב‑כתום המיוצר על‑ידי המיקרוב העמיד לקרינה Deinococcus radiodurans. הקרוטנואידים שייכים לאותה משפחה של תרכובות שמעניקה לגזר ולפירות מסוימים את צבעם, ורבים מהם פועלים כאנטי‑אוקסידנטים חזקים, הסופגים מינים חמצן פעילים — מולקולות לא יציבות שיכולות לפגוע בתאים. מחקרים קודמים הראו כי דינואקסנטין יעיל במיוחד בנטרול רדיקלים חמצניים מסוימים. החוקרים תהו האם האנטי‑אוקסידנט החזק הזה יוכל להתנגד לשתי הכוחות שמניעים פריודונטיטיס: דלקת בלתי נשלטת ולחץ חמצוני ברקמות התומכות בשיניים.
בדיקת דינואקסנטין בחניכיים חולות
כדי לדמות מחלת חניכיים אנושית מתקדמת, הצוות חסם ליגטורות דקות סביב שן אחורית בעכברים לאחר שציפו אותן בחיידק הפתוגני הידוע Porphyromonas gingivalis. סידור זה מעורר דלקת, גדילה חיידקית ואובדן עצם סביב השן. לאחר שבוע, חלק מהעכברים קיבלו מנה אוראלית יומית של דינואקסנטין במשך שבועיים, בעוד שאחרים קיבלו רק את השמן ששימש כנשא. סריקות רנטגן תלת‑ממדיות ברזולוציה גבוהה חשפו כי בעלי החיים החולים שלא טופלו איבדו כמות משמעותית של עצם תומכת, בעוד שבעלי החיים שקיבלו דינואקסנטין שמרו על יותר מוקדי עצם ונפח עצם, קרובים למה שנצפה בקבוצת הביקורת הבריאה. בדיקה מיקרוסקופית הראה שחניכיים שטופלו בדינואקסנטין הכילו פחות תאים דלקתיים פולשים ומרחקים קצרים יותר בין משטח השן לשפת העצם — שניהם סימנים לשימור הרקמה.
השתקת הדלקת ופירוק העצם
החוקרים שאלו מדוע העצם והרקמות הרכות השתקמו טוב יותר עם דינואקסנטין. בדיקות דם וצביעות של רקמות הראו כי פריודונטיטיס שנגרמה על‑ידי הליגטורה הגבירה שליחים דלקתיים קלאסיים כגון TNF‑α, IL‑1β ו‑COX‑2, שכולם קשורים בחוזקה לפירוק רקמות וכאב. דינואקסנטין הוריד באופן מובהק אותות אלה הן בזרם הדם והן ברצועה שמחזיקה את השן. בעצם הלסת עצמה, המחלה הגדילה את מספר וגודל התאים האוכלי עצם (אוסטאוקלסטים) והגברה של מולקולות שמעודדות את היווצרותם, כולל RANKL וקטפטסין K. דינואקסנטין הפחית את התאים המפרקי עצם ואת הסמנים שלהם, ובמקביל שיקם חלבונים הקשורים לבניית עצם חדשה — כגון RUNX2, BMP2, osterix, osteocalcin ו‑osteopontin — וחיזק מסלול פנימי מגן (Nrf2/HO‑1) שעוזר לתאים להתמודד עם לחץ חמצוני.
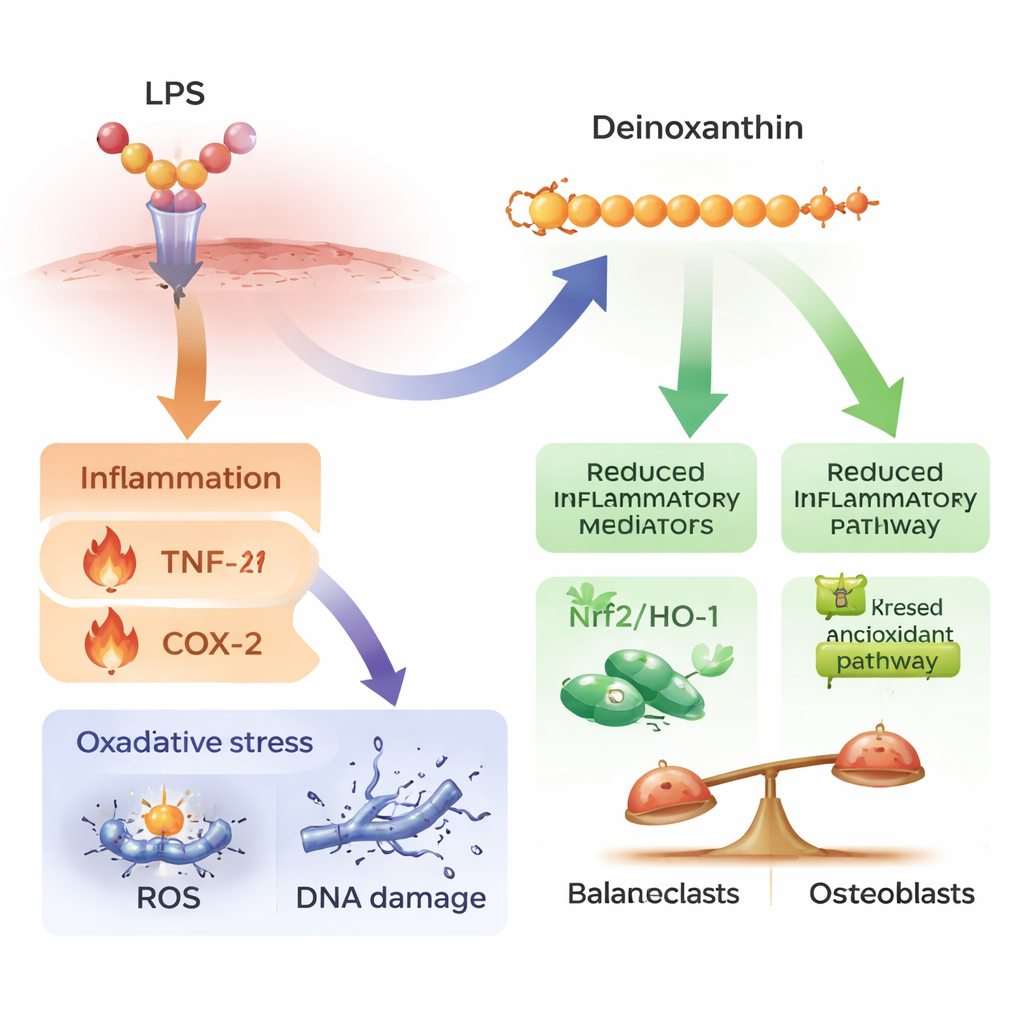
התמקדות בתאים אנושיים
מאחר שמחקרים בעכברים אינם מסבירים במלואם כיצד תרכובת עשויה לפעול בבני אדם, הצוות חקר בתרבית תאי הרצועה הפריודונטלית האנושית וקו תאי מערכת חיסון אנושי במעבדה. הם אתגרו תאים אלו עם מרכיבי חיידק שמפעילים בדרך כלל תגובות דלקתיות חזקות ונזק חמצוני. תחת לחץ זה, התאים ייצרו יותר גורמי דלקת, צברו מינים חמצן פעילים, הראו נזק DNA ואיבדו חלק מיכולתן לגדול, לנוע ולתמוך ביצירת עצם. הוספת מנה נמוכה ולא רעילה של דינואקסנטין שיקמה את גדילת התאים, צמצמה את הלחץ החמצוני ונזקי ה‑DNA, ושיפרה ריפוי דמוי‑פצע במצלחות תרבית. כמו כן היא הזיזה את פעילות הגנים הרחק מכימוקינים וציטוקינים שמגייסים ומפעילים תאים דלקתיים וכיוון אותה לתכניות אנטי‑אוקסידנטיות ותיקון הרקמה.
מפיגמנט לטיפול פוטנציאלי
בסיכומו של דבר, המחקר מציע כי דינואקסנטין יכול לפעול על מספר חזיתות: הוא מרסן מולקולות דלקת מרכזיות, מצמצם לחץ חמצוני, מעכב תאים מאריכים על‑ידי פירוק עצם ותומך בתאי בניית עצם ברקמות החניכיים. בעוד שממצאים אלו נובעים מניסויים בבעלי חיים ומתאים אנושיים בתרבית — ועדיין נותר עבודת המשך לאימות הבטיחות, המינון והיעילות בבני אדם — הם מעלים את האפשרות שפיגמנט אנטי‑אוקסידנטי שמקורו בטבע עשוי יום אחד להשלים את הטיפול הסטנדרטי בפריודונטיטיס כרוני, ולעזור למטופלים לשמר טוב יותר את שיניהם והעצם התומכת בהן.
ציטוט: Bhattarai, G., An, YH., Shrestha, S.K. et al. Therapeutic potency and the related mechanism of deinoxanthin in experimental animal and cell models of periodontitis. Sci Rep 16, 5735 (2026). https://doi.org/10.1038/s41598-026-36514-1
מילות מפתח: מחלת חניכיים, דינואקסנטין, טיפול אנטי‑אוקסידנטי, דלקת חניכיים, אובדן עצם