Clear Sky Science · he
שינויים m6A במארח מעצבים את המיקרוביום שמניע פרוטוזה תאית ספציפית כנתיב סיבתי למחלות נשימה כרוניות
מדוע המיקרובים שלכם חשובים לריאות
בעיות נשימה כרוניות כמו אסתמה ומחלת ריאה חסימתית כרונית (COPD) מאשימים בדרך כלל בעישון, זיהום או אלרגיות. המחקר הזה מצביע על שחקן נוסף, פחות ברור: הטריליוני המיקרואורגניזמים החיים במעיים ועל העור שלנו. באמצעות נתוני גנום בקנה מידה רחב, המחברים מראים שמיקרובים מסוימים עשויים לא רק ללוות מחלת ריאות אלא גם לתרום לה — באמצעות שינויים כימיים עדינים בתאים וצורת נזק תאית המונעת על ידי ברזל. הבנת הרשת הנסתרת הזו עשויה בסופו של דבר להוביל לדרכים חדשות למנוע או לטפל במחלות נשימתיות כרוניות על ידי כיוונון המיקרובים שלנו ואת המסלולים המולקולריים שלהם לכיוון בריא יותר.
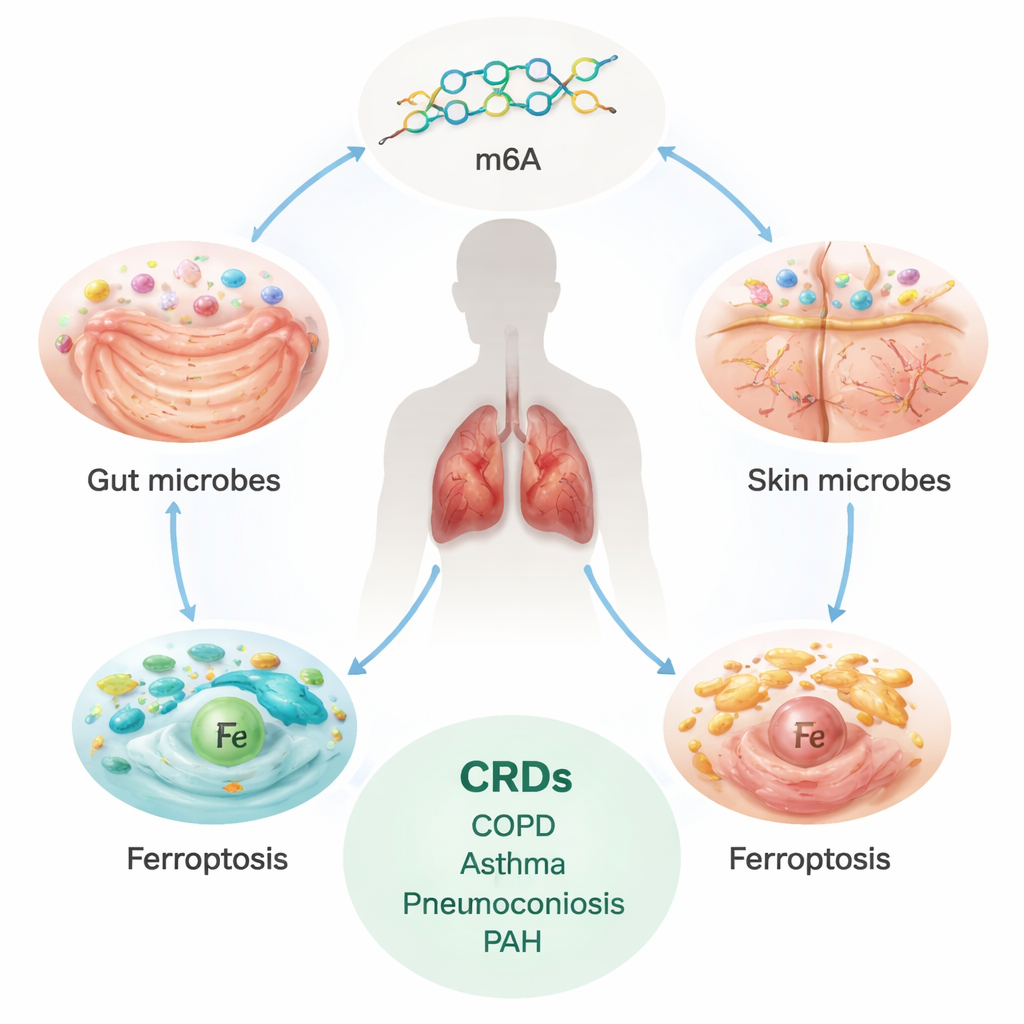
הנטל הנסתר של מחלות ריאה כרוניות
מחלות נשימה כרוניות, כולל COPD, אסתמה, מחלת ריאה אינטרסטיציאלית (ILD), פנמוקוניאוזיס ויתר לחץ דם עורקי ריאתי (PAH), משפיעות על מאות מיליוני אנשים ברחבי העולם וגורמות למיליוני מקרי מוות מדי שנה. מצבים אלה מתקדמים לעיתים באיטיות אך לעקב, גורמים לצלקת או לשינוי מבני בריאות ובכלי הדם ומשאירים אנשים עם קוצר נשימה. הטיפולים הנוכחיים בעיקר מנהלים תסמינים; הם אינם עוצרים או הופכים לגמרי את הנזק הבסיסי. זה דחף את המדענים לחפש סיבות עמוקות יותר, בעיקר כאלו הניתנות לשינוי לפני שמחלה חמורה מתפתחת.
שכנינו המיקרוביאליים במעי ועל העור
כיום ידוע שמערכת העיכול והעור מאכסנות קהילות מיקרוביאליות מורכבות שעוזרות לאמן את מערכת החיסון, לעצב מטבוליזם ולשמר מגני מחסום. אך האם מיקרובים אלה באמת מניעים מחלת ריאה, או שהם משתנים כשאנשים חולים? כדי להפריד סיבה מתוצאה, החוקרים השתמשו בשיטה הנקראת רנדומיזציה Mendelian (Mendelian randomization), שמנצלת הבדלים גנטיים טבעיים בין אנשים כמעין "ניסוי" לחיים. הם שילבו נתונים גנטיים על מאות סוגי מיקרובים במעי ובעור עם נתונים על חמש מחלות ריאה כרוניות עיקריות ממחקרים אירופיים גדולים, ובחנו האם נטיות תורשתיות לרמות גבוהות או נמוכות של מיקרובים ספציפיים מקושרות לסיכון לכל מחלה.
מיקרובים שמזיקים או מועילים לריאות
הניתוח זיהה עשרות מיקרובים במעי שהגבירו או הפחיתו את הסיכון לכל מחלת נשימה, לעתים בדפוסים ייחודיים למחלה. למשל, חיידקים מסוימים במעי נראו כמגנים מפני COPD, אסתמה או PAH, בעוד אחרים הגדילו את הסיכויים ל-ILD או COPD. מיקרובים בעור הראו קשרים מתונים יותר אך עדיין ניתנים לזיהוי, כאשר מינים מסוימים נקשרו לסיכון גבוה ואחרים לסיכון נמוך במצבים שונים. הצוות גם הפך את כיוון הניתוח ומצא שסיכון גנטי ל-COPD, אסתמה ומחלות ריאה אחרות חזה בשינויי המיקרוביום הן במעי והן בעור. תנועה דו-כיוונית זו מרמזת על לולאת משוב: המיקרובים יכולים לעצב מחלת ריאה, ומחלת הריאה יכולה לשנות את האקוסיסטמות המיקרוביאליות שלנו.
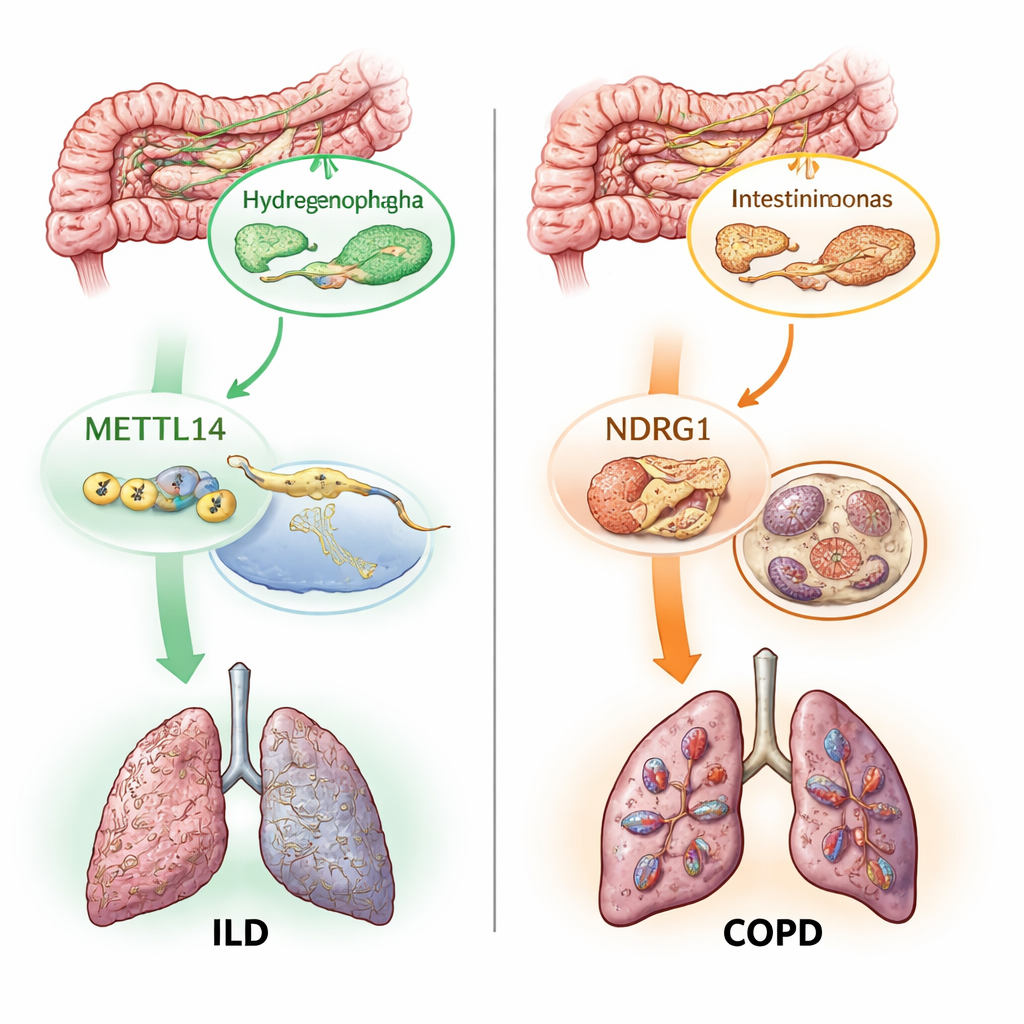
שני מתגים מולקולריים: סימני RNA ומוות תאי מונע ברזל
מעבר למיפוי אילו מיקרובים חשובים, המחברים חקרו כיצד שותפים זעירים אלה עלולים להשפיע על רקמות הריאה. הם התמקדו בשני תהליכים מולקולריים שכבר חשודים בנזק ריאתי. הראשון, הנקרא שינוי m6A, הוא תג כימי קטן המתווסף ל-RNA ומכוון כיצד גנים נדלקים או נכבים. השני, פרוטוזה (ferroptosis), היא צורת מוות תאי התלויית ברזל המונעת על ידי חמצון בלתי נשלט של שומנים בממברנות התאים. באמצעות פרוקסים גנטיים ל-19 גנים הקשורים ל-m6A ולמאות גנים הקשורים לפרוטוזה, הם בדקו האם שינויים במסלולים אלה קשורים באופן סיבתי למחלת ריאה. הם מצאו שגן כותב אחד של m6A, METTL14, קשור לסיכון נמוך יותר ל-ILD, וכמה גני פרוטוזה, כולל NDRG1, נקשרו לסיכון גבוה יותר ל-COPD, ILD ולאסתמה.
חיבור הנקודות: מהמיקרובים לתאים ועד למחלה
החלק החדשני ביותר בעבודה היה מעקב אחר האופן שבו החלקים הללו משתלבים בשרשרות של סיבה ותוצאה. ניתוחי תיווך סטטיסטיים הציעו שחלק מהאפקט המגן של METTL14 על ILD עובר דרך שינויים שהוא גורם במיקרוב מסוים במעי הנקרא Hydrogenophaga. במסלול אחר, חיידק מעי ספציפי, Intestinimonas massiliensis, נראה משפיע על סיכון ל-COPD בחלקו על ידי הפעלת NDRG1 ותוכנית המוות הפרוטוטית. הצוות בדק אז נתוני רקמת ריאה אנושית ואישר ש-METTL14 ו-NDRG1 מבטאים באופן שונה בדגימות חולות לעומת בריאות. לבסוף, בעזרת מפות גנטיות בתא יחיד של תאים חיסוניים, הם זיהו את ההשפעה המזיקה של NDRG1 על COPD לתת-קבוצה מסוימת של תאים חיסוניים, סוג של מונוציט, מה שמרמז שתרופות עתידיות המכוונות גן זה עשויות להזדקק לפעול באופן ספציפי לתא.
מה משמעות הדבר לטיפולים עתידיים
עבור קוראים לא-מומחים, המסר המרכזי הוא שבריאות הריאה אינה רק מה שאנו נושמים אלא גם המיקרובים החיים בתוכנו ועלינו והמתגים המולקולריים שהם מפעילים בתוך התאים שלנו. מחקר זה אינו יכול להוכיח כל שלב בניסוי מעבדתי, והוא מוגבל בעיקר לאנשים ממוצא אירופי, אך הוא מציע רמזים גנטיים חזקים שמיקרובי מעיים, סימני RNA כמו m6A ומוות תאי מונע ברזל יוצרים נתיב מחובר המוביל לנזק ריאתי כרוני. בטווח הארוך, קו מחקר זה עשוי לעודד אסטרטגיות חדשות שמשלבות טיפולים מבוססי מיקרוביום עם תרופות המכוונות METTL14, NDRG1 או פרוטוזה, במטרה לא רק להקל על תסמינים אלא לקטוע את המעגלים הביולוגיים שגורמים להתקדמות המחלות הנשימתיות הכרוניות.
ציטוט: Zhang, J., Liu, X., Liu, X. et al. Host m6A modifications shape microbiota that drives cell specific ferroptosis as a causal pathway to chronic respiratory diseases. Sci Rep 16, 5809 (2026). https://doi.org/10.1038/s41598-026-36513-2
מילות מפתח: מיקרוביום המעי, מחלת ריאה כרונית, אסתמה ו-COPD, אפיגנטיקה של RNA, מסלולי מוות תאי