Clear Sky Science · he
ATF4 מסדיר תפקוד מיטוכונדריאלי לקוי ומיטופגיה, התורמים לאפופטוזה של האנדותל הקרניתי
למה החלון של העין עלול להתעכר
הקרניות שלנו — החלונות השקופים הקדמיים של העיניים — נשארות שקופות בזכות שכבה דקה ועובדת קשה של תאים על פני השטח הפנימי שלהן. בניוון האנדותל הקרניתי של פוכס (FECD), מיליוני אנשים מאבדים בהדרגה את התאים הללו, מה שמוביל לנפיחות, ראייה מעומעמת ולעיתים זקוק להשתלות קרנית. המחקר הזה שואל שאלה בסיסית אך מכרעת: מה גורם לתאים אלה להחליט למות, והאם כיבוי של "מפתח" מולקולרי אחד יכול להציל אותם?
שכבה תאית עדינה ששומרת על ראייה ברורה
האנדותל הקרניתי הוא גיליון יחיד של תאים המשושים שמשאבת באופן מתמיד נוזלים החוצה מהקרנית כדי לשמור על שקיפותה. ב‑FECD, תאים אלה נכנסים למתח ונעלמים בהדרגה, בעוד שכיחים בולטים של חומר בלתי תקין, הנקראים guttae, מצטברים על הממברנה התת‑ממדית. מאחר שאין תרופות מאושרות ל‑FECD והשתלות קרנית הן הטיפול העיקרי, החוקרים מנסים להבין בדיוק כיצד מתח בתוך התאים האלה דוחף אותם לעבר מוות. מחקרים קודמים הצביעו בנפרד על עומס בשני תאים‑מחסנים מרכזיים — הרשת האנדופלסמטית (מפעל קיפול החלבונים של התא) והמיטוכונדריה (תחנות הכוח של התא) — אבל לא היה ברור כיצד שתי תגובות הלחץ הללו מתקשרות זו עם זו.
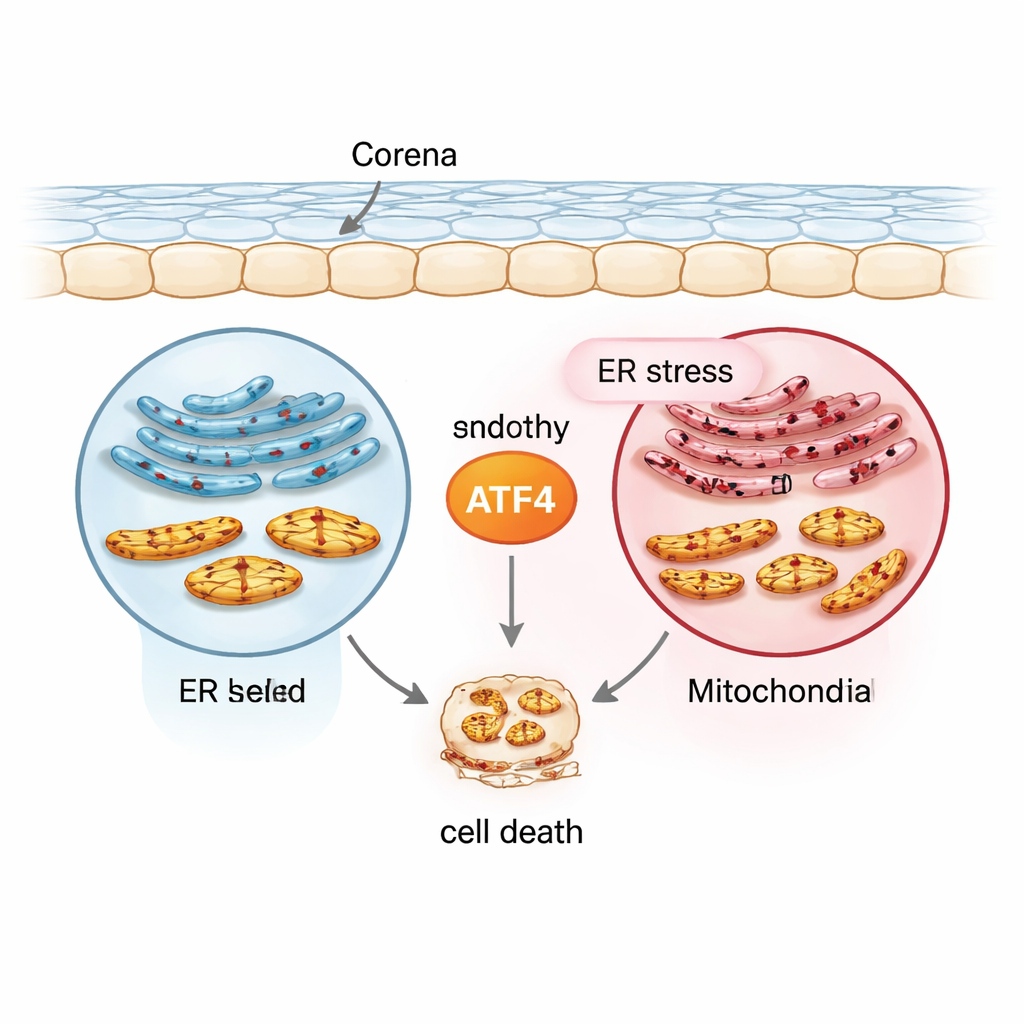
שליח המתח במרכז: ATF4
הצוות התרכז בחלבון בשם ATF4, פקטור שעתוק שמפעיל או מדכא שורה של גני תגובת־מתח. באמצעות קו תאי אנדותל קרנית אנושי נורמלי (21T), קו תאים הדומה ל‑FECD הנושא את הרחבת החזרות ב‑TCF4 הקשורה למחלה (F35T), תאי אנדותל קרנית ראשוניים של בני אדם ומודלים עכבריים החשופים לאור אולטרה‑סגול A (UVA), הם יצרו מגוון תנאים המדמים מתח כרוני. הם גרמו למתח ברשת האנדופלסמטית בעזרת התרופה טוניקאמיצין ואז מדדו את ATF4 וסמנים נוספים. בהשוואה לתאים נורמליים, תאי דמויי‑FECD התחילו עם רמות גבוהות יותר של ATF4 וחלבוני מתח קשורים, ו‑ATF4 עלה עוד יותר תחת מתח כרוני גם בתאים בתרבית וגם ברקמות קרנית של בני אדם. דפוס זה הציב את ATF4 בצומת בין תגובות הגנה מוקדמות לאיתותים הרסניים מאוחר יותר.
מכשלת כוח למוות מתוכנת
בהמשך בדקו החוקרים כיצד מתח זה משפיע על המיטוכונדריה. בתאי דמויי‑FECD המיטוכונדריה ייצרו פחות ATP, איבדו את פוטנציאל הממברנה החשמלי שלהן והתפרקו מצורות ארוכות ורשתיות לחתיכות רבות וקטנות. שינויים אלה החמירו כאשר מתח הרשת האנדופלסמטית התמשך. במקביל, חלבוני מוות תא קלאסיים — כמו קספאזות מופעלות וחלבון תיקון ה‑DNA PARP בצורה המסולקת שלו המקדמת מוות — הפכו לשכיחים יותר, בעוד שחלבונים מגן כמו Bcl‑2 ירדו. יחדיו, שינויים אלה מצביעים על כך שתאי אנדותל קרנית נלחצים לעבר אפופטוזה מונעת‑מיטוכונדריה, צורת התאבדות מתוכננת מסודרת אך בלתי הפיכה.
מנגנון הניקוי נתקע תחת מתח כרוני
במצב תקין, מיטוכונדריות שנפגעו קשה מוסרות בתהליך מחזורי הנקרא מיטופגיה, שבו הן מתייגות ומתעגלות לשקיקים קטנים להסרה. הצוות מצא שמולקולות "ההפעלה" המוקדמות של מיטופגיה (Parkin ו‑LC3) הופעלו גם בתאים נורמליים וגם בתאי דמויי‑FECD, במיוחד אחרי מתח. אך חלבונים תומכים מרכזיים הופחתו, ומיקרוסקופ אלקטרוני הראה הצטברות של מיטוכונדריות שחוטזו חלקית ותפוסות בתוך וסיקולות. זה מציע שלמרות שהתהליך הניקוי התחיל, הוא נכשל להסתיים, והשאיר את התאים מלאים בתחנות כוח פגומות שמזינות עוד את המתח והמוות במקום לשקם.
כיבוי ATF4 להצלת תאים
כדי לבדוק האם ATF4 מכתיב את הספירלה הזו, החוקרים השתמשו ב‑siRNA להשתקה חלקית של ATF4 בתאי אנדותל קרנית בתרבית. תחת אותו מתח כרוני, תאים עם ATF4 מופחת הראו רמות נמוכות יותר של חלבוני קידום מוות, פוטנציאל ממברנה מיטוכונדריאלי בריא יותר, פחות פירוק ושרידות טובה יותר בניסויים של יכולת קיום. חשוב מכך, מספר מבני מיטופגיה התקועים ירד, מה שמעיד שהפחתת ATF4 סייעה לשחזר איזון יעיל יותר בין נזק לניקוי. בעכברים מהונדסים שהחזיקו עותק עובד אחד בלבד של הגן ATF4, חשיפת UVA גרמה לפחות הפעלה של חלבון שותף מקדם־מוות, CHOP, ושמרה על יותר תאים אנדותליים בצורות תקינות בהשוואה לעכברים עם כמות ATF4 מלאה.
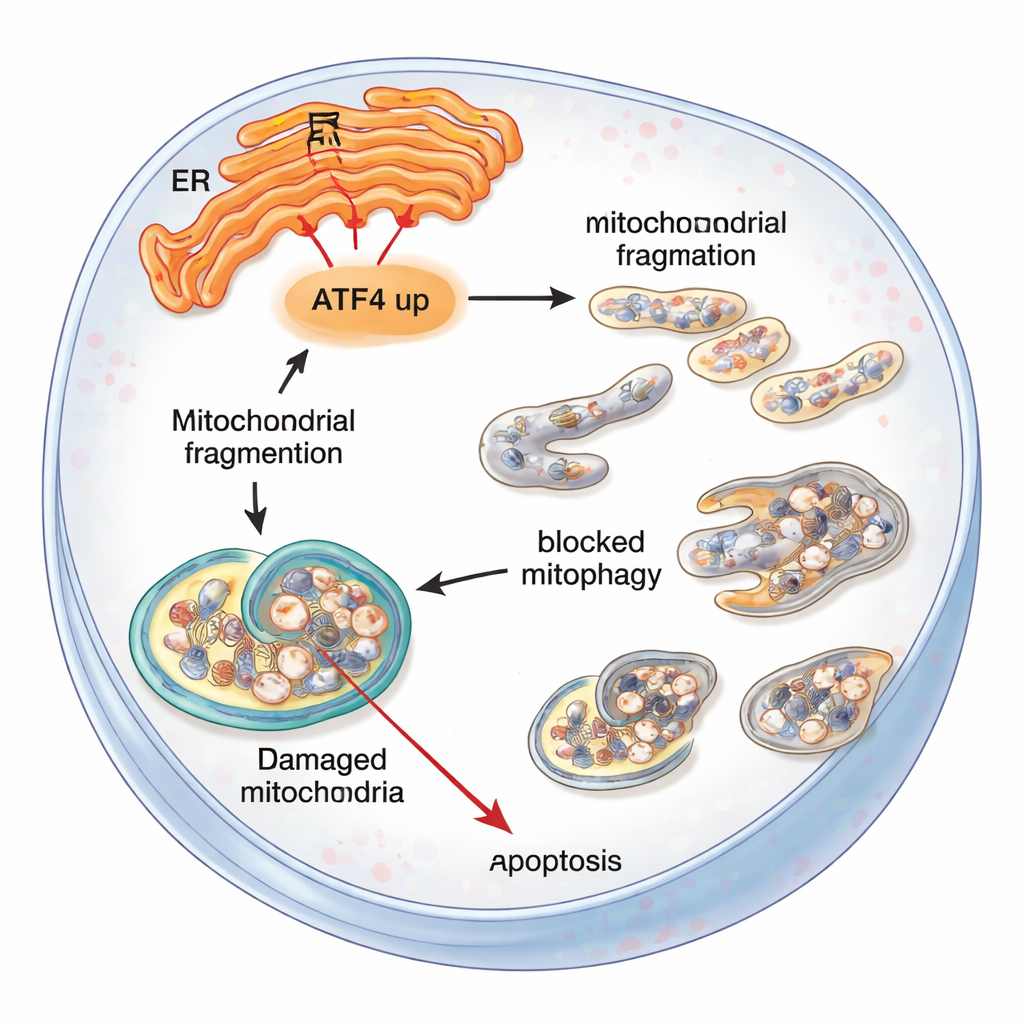
מה משמעות הדבר לאנשים עם FECD
ללא‑מומחים, המסר הוא ששליח מתח אחד, ATF4, יכול להטות את תאי האנדותל הקרניתי ממצב התמודדות לקריסה. כאשר מתח הרשת האנדופלסמטית ממושך, ATF4 תורם להפרעה במיטוכונדריה, מעכב את מנגנון הניקוי של התא ובסופו של דבר מעודד תאים חיוניים אלה להתנקש בעצמם. הורדת פעילות ATF4 — בין אם גנטית בעכברים ובין אם באמצעות כלים מולקולריים ממוקדים בתאים — מגנה על המיטוכונדריה, משפרת את הסילוק של הפסולת ומשאירה יותר תאים בחיים. בעוד שעבודה זו נמצאת עדיין בשלב המעבדה והחיות, היא מדגישה את ATF4 ונתיבי הלחץ הקשורים אליו כיעדי תרופות מבטיחים שעשויים יום אחד להאט או למנוע את התקדמות ניוון פוכס ולהפחית את הצורך בהשתלות קרנית.
ציטוט: Qureshi, S., Kim, S.Y., Lee, S. et al. ATF4 regulates mitochondrial dysfunction and mitophagy, contributing to corneal endothelial apoptosis. Sci Rep 16, 5960 (2026). https://doi.org/10.1038/s41598-026-36453-x
מילות מפתח: ניוון האנדותל הקרניתי של פוכס, אנדותל הקרנית, מתח מיטוכונדריאלי, מיטופגיה, ATF4