Clear Sky Science · he
גישה אינטגרטיבית לזיהוי רשתות אינטראקציה חדשות בין miRNA ל-mRNA בקרדיומיופתיה הנגרמת על ידי LMNA
מדוע רגולטורים זעירים של הלב חשובים
קרדיומיופתיה מורחבת היא מחלה חמורה שבה הלב מתרחב ונחלש, לעתים קרובות מובילה לכשל לב, להפרעות קצב מסכנות חיים ואף למוות פתאומי. אצל משפחות רבות המחלה תורשתית, ושינויים בגן בשם LMNA הם גורם שכיח. המחקר הזה שואל שאלה שנראית פשוטה אך בעלת השלכות גדולות: בלביים שנפגעו ממוטציות ב-LMNA, אילו גנים הופעלו או כובו, ואילו מולקולות RNA זעירות הן אלו שמנהלות את המתגים האלה? על ידי מיפוי השיחות המולקולריות הללו בפרטנות, העבודה מצביעה על דרכים חדשות לחזות, לנטר ואולי יום אחד לטפל בצורה בחומרה זו של מחלת הלב.
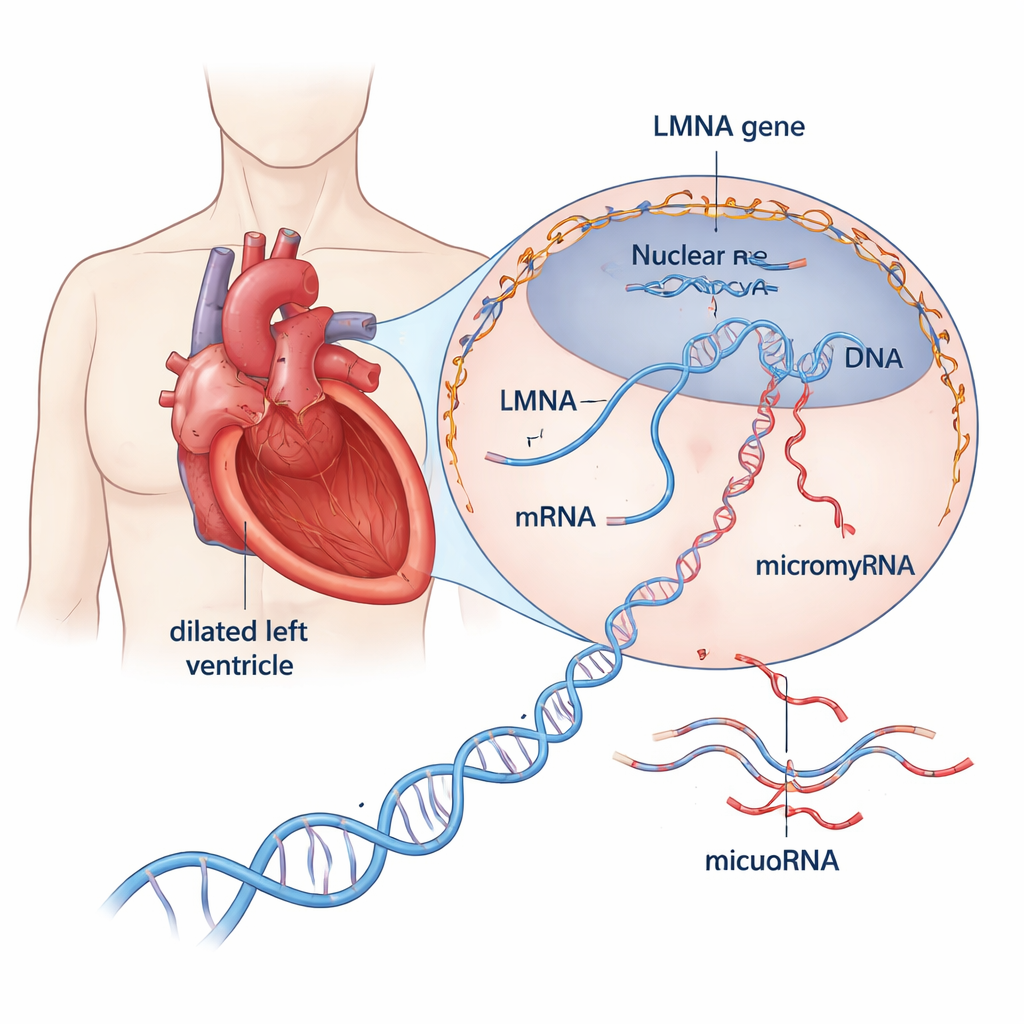
מבט קרוב על מחלת לב מסוכנת
קרדיומיופתיה מורחבת מפריעה וממעטת את דופן חדר המליטה המרכזי של הלב, מה שמחליש את יכולתו לשאוב דם דרך הגוף. בערך שליש עד מחצית מהמקרים שעד כה סווגו כ"אידיופתיים" מתבררים כבעלי בסיס גנטי. מתוך יותר מ-30 הגנים המעורבים, LMNA בולט: וריאנטים מזיקים בגן זה אחראים לכ-10% מהמקרים התורשתיים וקושרים להתקדמות מהירה של המחלה, לבעיות קצב מוקדמות ולסיכון גבוה למוות לבבי פתאומי. LMNA מייצר חלבוני מבנה היוצרים תושבת סביב ה-DNA של התא, המסייעת לשמור על צורת הגרעין ומושפעת מתי אילו גנים פעילים. עם זאת, כיצד חלבוני LMNA פגומים דוחפים את הלב לכשל נותר עד כה לא מובן דיו.
לעקוב אחר ההודעות בתוך לבבות עכבר
כדי לחקור זאת, החוקרים השתמשו במודל עכבר הנושא מוטציה ידועה ב-LMNA (R249W) המפתחת צורה של קרדיומיופתיה מורחבת הדומה למחלה האנושית. בגיל 50 שבועות — כשהעכברים מראים הרחבת חדרים, תפקוד שאיבה מקוטע וצלקות פיברוטיות — הצוות חילץ רקמת לב ובחן שני סוגי RNA: RNA שליח (mRNA), הנושא הוראות לייצור חלבונים, ו-microRNA (miRNA), רצועות קצרות שאינן מקודדות המכוונות באופן עדין את פעילות הגנים על ידי חסימה או פירוק של mRNA מסוימים. באמצעות רצף-יתר בעל קיבולת גבוהה וסינונים סטטיסטיים מדויקים זוהו 2,148 גנים שהפעילות שלהם השתנתה בלבבות המוטנטים ו-53 miRNA שהיו מוגברים או מוקטנים בהשוואה לעכברים בריאים.
מה משתנה בתאי הלב החולים
כאשר החוקרים קבוצו את הגנים ששונו למסלולים ביולוגיים, עלו מספר נושאים מרכזיים. רבים מהגנים המשתנים קשורים לדרך שבה תאי שריר הלב מתכווצים, לאופן שבו הם דבוקים זה לזה ולמטריצה התומכת שסביבם, לאופן שבו אותות חשמליים עוברים דרך הלב ולדרך שבה התאים מעבדים שומנים לייצור אנרגיה. ממצאים אלה תואמים את התמונה הקלינית של מחלת LMNA: רקמה נוקשה ופיברוטית; הולכה חשמלית מופרעת המעדיפה אריתמיות; ואיזון אנרגטי לקוי. ניתוחי מסלולים בעזרת מאגרים מבוססים אישרו העשרה במערכות של עיבוד מטריצה חוץ-תאית, תעלות יוניות התלויות מתח, תקשורת דמויית סינפסה בלב וחילוף חומרים של חומצות שומן — מה שמרמז שהמוטציה ב-LMNA משבשת מערכות מרובות ומחוברות זו לזו במקום שלב תקול יחיד.
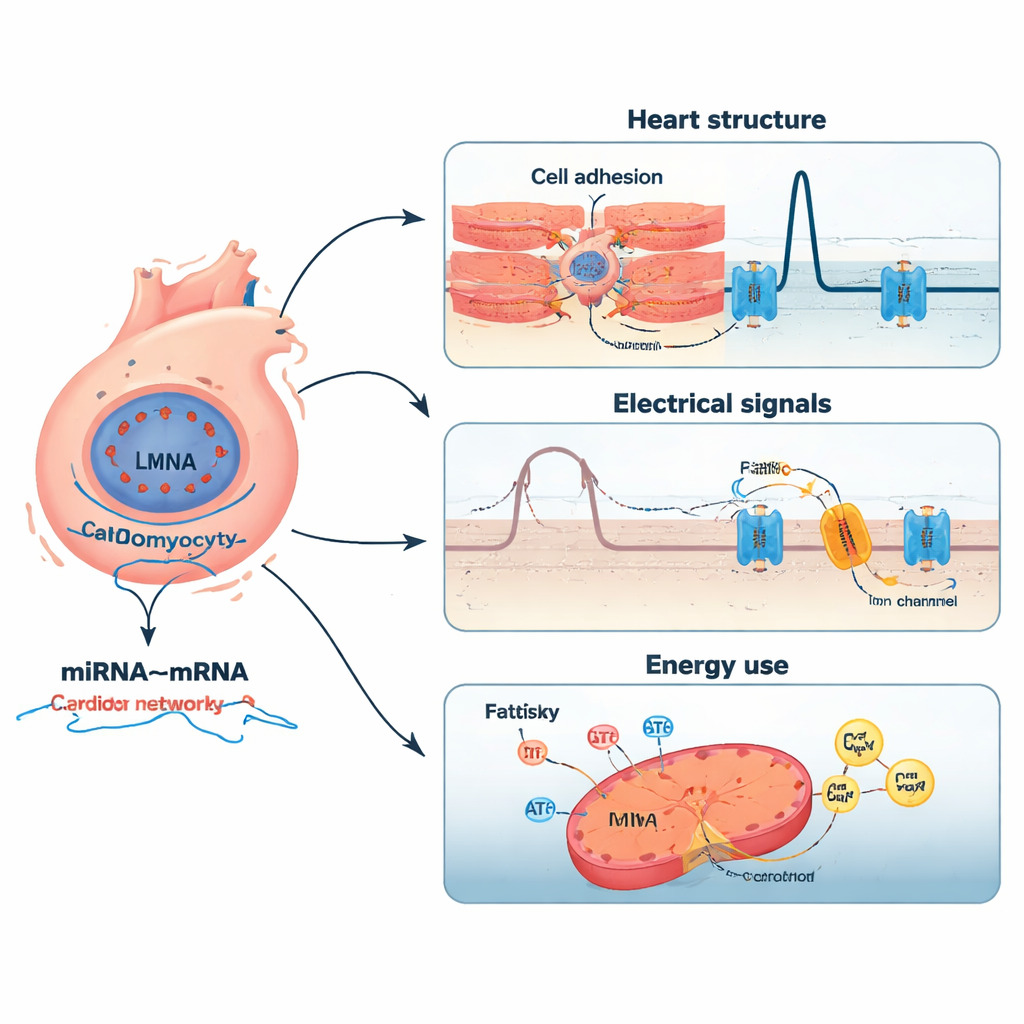
רשתות של מתגי-זעירים ויעדיהם
המחקר התקדם בכך שלזג miRNA עם מטרות ה-mRNA הסבירות שלהם. באמצעות ניתוחי קורלציה ובדיקות חוצה מול מאגרי מידע גדולים של אינטראקציות שנבדקו ניסויית, המחברים הרכיבו רשת אמינה גבוהה של 2,197 זוגות miRNA–mRNA הכוללת 12 miRNA מרכזיים. כמה miRNA היו פעילים יותר ונראו מדכאים גנים קריטיים להתפתחות הלב, לטיפול בסידן ולתגובות ללחץ חמצוני. אחרים היו פחות פעילים, ובכך שחררו מעצורים על גנים המעורבים בהדבקות בין-תאית, בדלקת ובשיקום תשתית המבנה של הלב. לדוגמה, miRNA אחד (miR-183-5p) נקשר לקולטן במסלול איתות Wnt, המשפיע על תקשורת בין-תאית, בעוד אחר (miR-3473a) התחבר לתעלת שחרור סידן מרכזית בקצב פעימת הלב. יחד, רשתות אלה משרטטות כיצד שינויים עדינים בוויסות של RNA זעירים יכולים להעצים את השפעת המוטציה ב-LMNA.
ממפות מולקולריות לעבר טיפולים עתידיים
בעבור לא-מומחים, המסקנה היא שהמחקר מציע מפה מפורטת של האופן שבו מוטציה ב-LMNA משנעת את החיווט הפנימי של הלב ברמת בקרה על גנים. במקום "גן רע" יחיד, המחלה משקפת מפל של הודעות משוננות — רבות מהן מתוזמרות על ידי miRNA — המשפיעות על מבנה הלב, יציבות חשמלית ושימוש באנרגיה. למרות שהעבודה בוצעה בעכברים ותלויה במידה רבה באנליזה חישובית, היא מאירה זוגות miRNA–גן ספציפיים כמועמדים מבטיחים לסמנים בדם או לטיפולים ממוקדים בעתיד. בטווח הארוך, כיוון ויטול של מתגי RNA קטנים אלה עשוי לסייע לרופאים לזהות טוב יותר מי בסיכון הגבוה ביותר, לנטר את התקדמות המחלה בדיוק רב יותר ולעצב טיפולים מותאמים אישית למשפחות הנפגעות מקרדיומיופתיה הקשורה ל-LMNA.
ציטוט: Córdoba-Caballero, J., Martínez, F.B., Campuzano, O. et al. An integrative approach to identify novel miRNA-mRNA interaction networks in LMNA-cardiomyopathy. Sci Rep 16, 6110 (2026). https://doi.org/10.1038/s41598-026-36439-9
מילות מפתח: קרדיומיופתיה מורחבת, גן LMNA, microRNA, ויסות גנים, כשל לב