Clear Sky Science · he
מודלים QSAR במחשב ובדיקת MTT במעבדה: אימות ניסיוני של מוליכים חדשים ל-uPAR לסרטן השד משולש-השלילה וסרטן העור
מדוע המחקר הזה חשוב
סרטן כמו סרטן השד משולש‑השלילה וסוגים מסוימים של סרטן העור קשים במיוחד לטיפול כי הם מתפשטים במהירות ולעתים קרובות עמידים לטיפולים סטנדרטיים. מחקר זה בוחן מטרה מבטיחה על פני התא — uPAR — ומדגים כיצד שילוב של עיצוב תרופתי במחשב וניסויים במעבדה יכול לחשוף מועמדים חדשים לתרופות שעשויים להאט או לעצור את התפשטות הגידולים האגרסיביים האלה.
פתח שעוזר לסרטן להתפשט
כדי שגוש סרטן יהפוך לממאיר באמת, תאים צריכים להשתחרר ממקומם המקורי, לחדור רקמות סביבתיות, להיכנס למחזור הדם ולהתיישב באיברים מרוחקים. uPAR הוא סייע מרכזי בתהליך זה. הוא יושב על פני התא הסרטני ופועל עם חלבונים שותפים להפעלת אנזימים הממיסים את המבנה התמך שסביבם, מה שמקל על התאים לנוע ולחדור. רמות uPAR גבוהות במיוחד נרשמות בתאי סרטן השד משולש‑השלילה ובחלק מסוגי סרטן העור, וקיומו מקושר לצמיחה מהירה יותר, לחדירות מוגברת ולתוצאות קליניות גרועות יותר. לכן uPAR מהווה מטרה אטרקטיבית — אך עד כה לא מנוצלת די הצורך — לפיתוח תרופות נגד סרטן.
כריית נתונים כימיים גדולים בעזרת אלגוריתמים חכמים
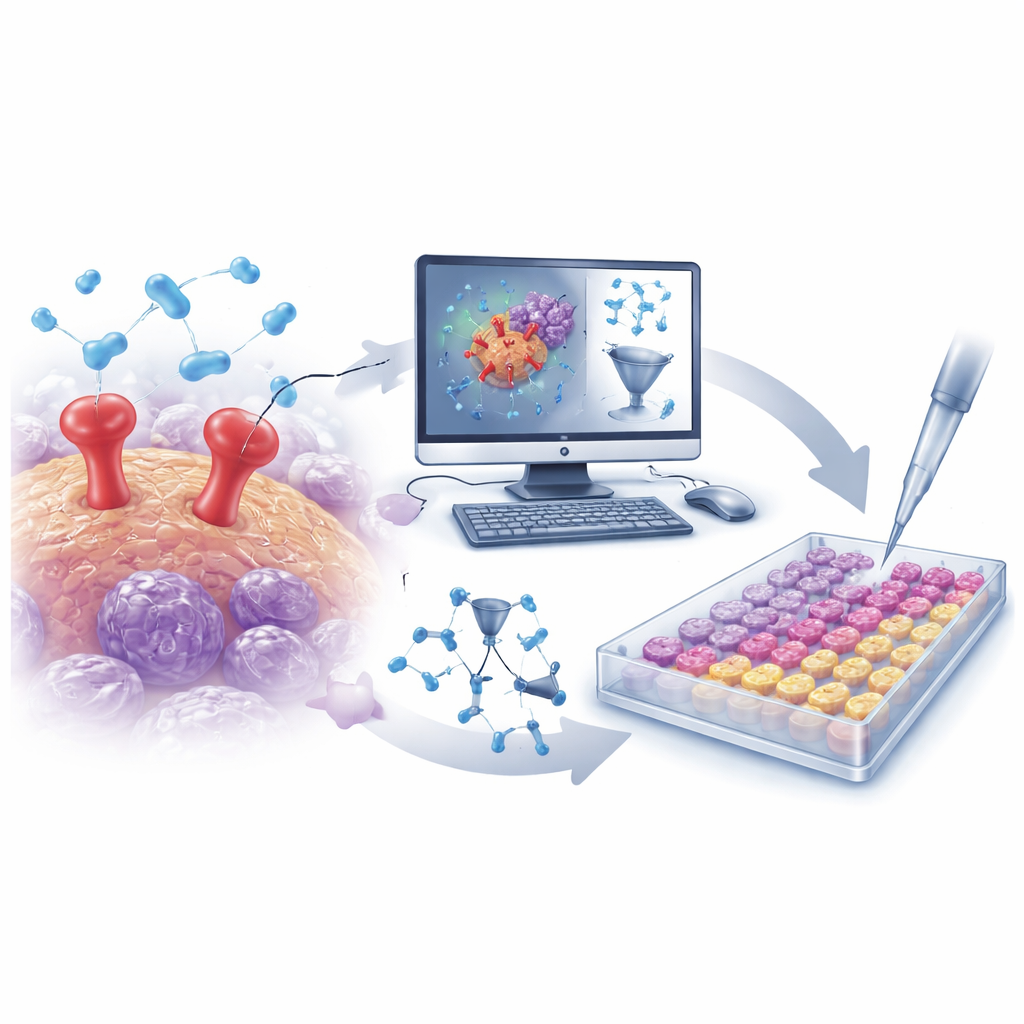
החוקרים התחילו באיסוף מאגר גדול של יותר מ‑500 מולקולות ידועות כחוסמות uPAR מתוך בסיס נתונים ציבורי. מבנה כל מולקולה תורגם לאלפי תיאורים מספריים המתארים מאפיינים כמו גודל, צורה, התפלגות מטען וגמישות. בעזרת נתונים אלה בנויה מודל יחס מבנה‑פעילות כמותי (QSAR) — כלי מתמטי שלומד אילו תכונות מבניות נוטות להפוך מולקולה למעכב חזק יותר של uPAR. לאחר ולידציה זהירה כדי למנוע התאמה-יתר, המודל הראה יכולת חיזוי גבוהה על תרכובות שלא נראו קודם, והדגיש מספר תכונות מפתח שהגבירו או החלישו את החסימה של uPAR. התובנות האלה הנחו את החיפוש אחר מולקולות חדשות ומתוכננות טוב יותר.
ממסכים וירטואליים ללשפופיות אמיתיות
מצוידים במודל QSAR מאומן, הצוות ביצע סריקה וירטואלית של ספרייה ממוקדת של כ‑30,000 מולקולות המכוונות בפרוטאזות. המודל צמצם במהירות את מאגר הענק הזה לקבוצת מועמדים קטנה של מעכבי uPAR סבירים. במקביל בוצעו סימולציות דוקינג במחשב כדי לבדוק עד כמה כל מועמד מתאים לאתר הקשירה של uPAR, וסימולציות דינמיקה מולקולרית בחנו האם קומפלקסים אלו יישארו יציבים לאורך זמן. מתוך הקמפיין המשולב הזה בלטו שתי מולקולות: D685‑0061, שסווגה על ידי מודל ה‑QSAR כחזקה במיוחד, ו‑C878‑1660, שזכתה לציון גבוה בדוקינג ובסימולציות כזו שיוצרת אינטראקציות יציבות במיוחד עם uPAR.
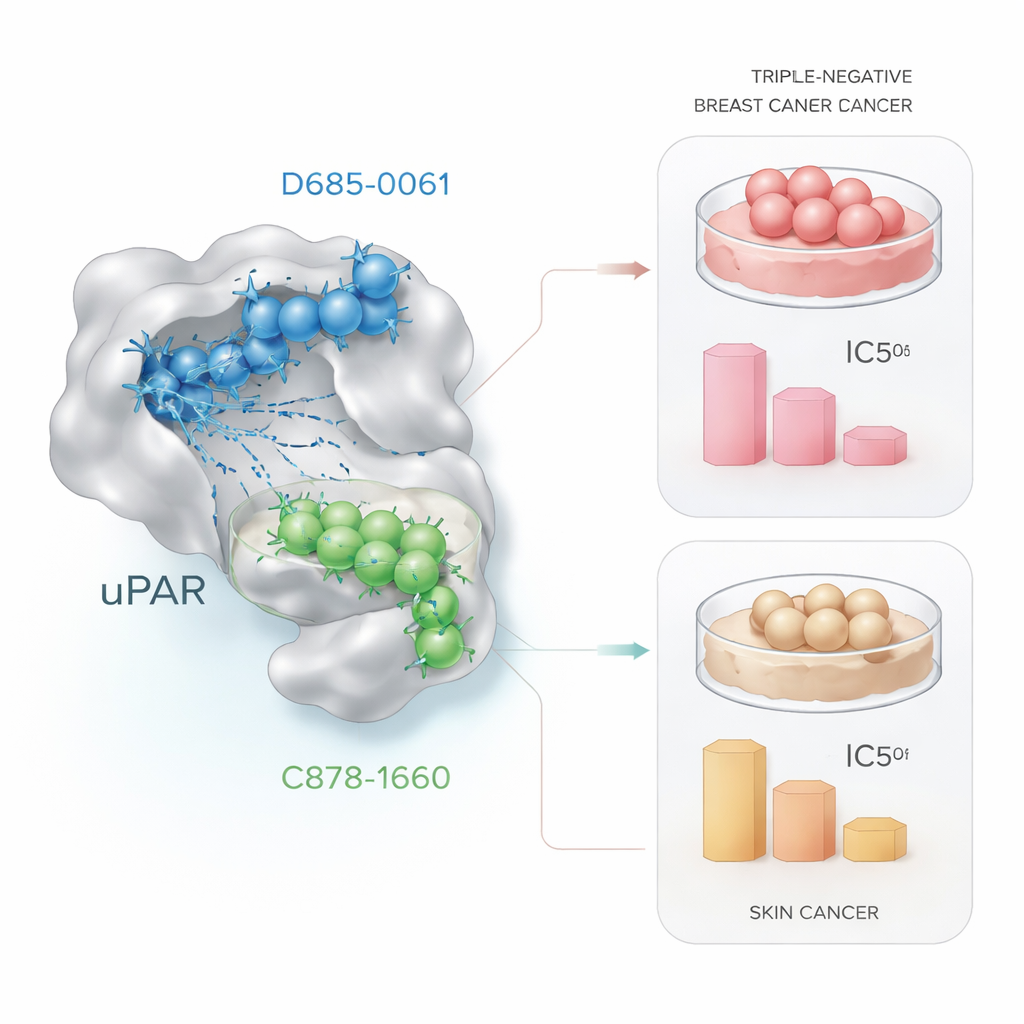
מבחן המועמדים בתאי סרטן
הבטחה חישובית משמעותית רק אם היא מתורגמת לאפקטים ביולוגיים אמיתיים. כדי לבדוק זאת חשפו החוקרים תאים סרטניים חיים למנות עולהות משתי המולקולות המובילות ומדדו הישרדות תאים בעזרת שיטת מעבדה סטנדרטית שנקראת בדיקת MTT. בתאי סרטן השד משולש‑השלילה (MDA‑MB‑231) D685‑0061 הרג תאים ביעילות רבה יותר, כשהרדיוס לחצי-חיים של הישרדות (IC50) היה סביב 21 מיקרומול, בעוד ש‑C878‑1660 דרש בערך פי ארבעה מכמות זו. תחת המיקרוסקופ, תאים שטופלו ב‑D685‑0061 הראו סימנים ברורים של מוות תאי מתוכנת, כגון התעגלות, ניתוק מהמשטח והתפוררות לחלקים. לעומת זאת, בתאי סרטן העור (A431) C878‑1660 היה הקטלני יותר, והשיג 50% מוות תאי בסביבות 19 מיקרומול לעומת כ‑28 מיקרומול ל‑D685‑0061, גם כאן עם נזקים תלויי מינון שנראו לעין.
מה המשמעות לעתיד טיפולי הסרטן
העבודה הזאת אינה מספקת תרופה חדשה באופן מיידי, אבל היא מספקת שתי נקודות התחלה מבטיחות וחשוב לא פחות — מתווה חזק לכימות ולגילוי נוספים. באמצעות חיבור בין דוגמנות גדלי‑נתונים, סימולציות תלת‑ממדיות וניסויים תאיים קפדניים, המחקר מראה שניתן לכוון בצורה סלקטיבית ל‑uPAR באמצעות מולקולות קטנות שפוגעות בתאי סרטן אגרסיביים של השד והעור. D685‑0061 ו‑C878‑1660 משמשות כעת כתרכובות מובילות שכימאים יכולים לחדד כדי להגדיל יעילות, לשפר בטיחות ולשפר פרמטרים של תנועה בגוף. בטווח הארוך, תרופות שיפותחו על פי גישה זו עשויות לסייע לחסום את התפשטות הסרטן המונעת על‑ידי uPAR, ולהפוך חלק מהגידולים המסוכנים של היום למחלות ניתנות לניהול טוב יותר.
ציטוט: Badukle, H., Jawarkar, R.D., Shah, U. et al. From in-silico QSAR modeling to in-vitro MTT assay: experimental validation of novel uPAR leads for triple-negative breast cancer (TNBC) and skin cancer. Sci Rep 16, 5786 (2026). https://doi.org/10.1038/s41598-026-36406-4
מילות מפתח: מעכבי uPAR, סרטן השד משולש‑השלילה, סרטן העור, עיצוב תרופתי בעזרת מחשב, בדיקת עמידות תאים MTT