Clear Sky Science · he
מסגרת למידה עמוקה משולבת אינטראקטיבית עם כוונון מומחה לדימות מדויק של תת‑אזורי האסטריאום
למה מיפוי של אזורים קטנטנים במוח חשוב
האסטריאום, מבנה קטן העמוק במוח, ממלא תפקיד מרכזי בתנועה ובמוטיבציה ונפגע רבות בהפרעות כמו מחלת פרקינסון. רופאים משתמשים לעיתים קרובות בסריקות PET ו‑MRI כדי למדוד שינויים כימיים באזור זה, אך האסטריאום מחולק לתת‑אזורים רבים וקטנים שקשה לראות ולתכנן אותם במדויק. מאמר זה מציג שיטה ממוחשבת מסייעת חדשה, בשם StriaSeg‑iARM, שעוזרת למומחים לצייר גבולות אלה בצורה מדויקת ויעילה יותר, גם אצל אנשים שמוחם השתנה בעקבות הזדקנות או מחלה.
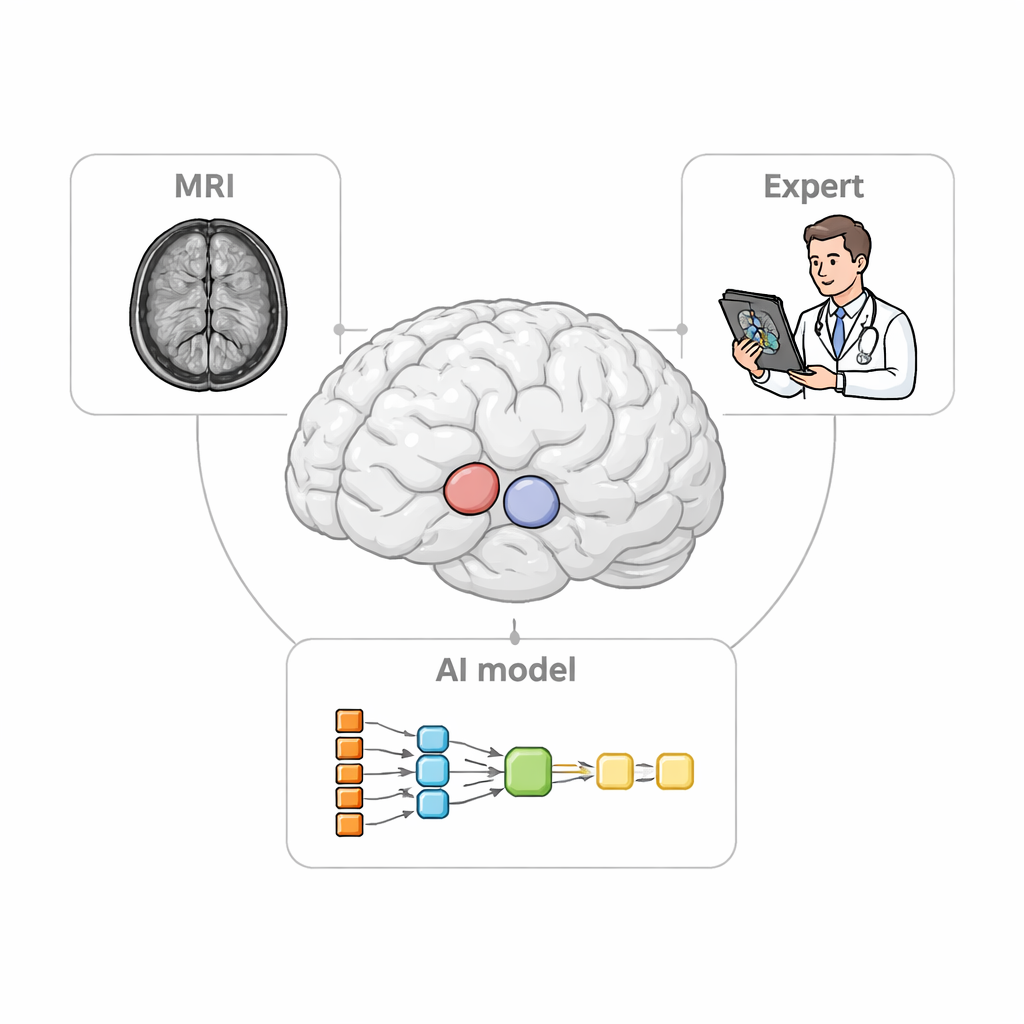
הבעיה הקלינית שמשתקפת לעין
כשנוירולוגים מעריכים מצבים כמו מחלת פרקינסון, הם מסתמכים על סריקות PET כדי לעקוב כיצד איתותים הקשורים לדופמין משתנים בחלקים שונים של האסטריאום. כדי לעשות זאת נכון, הם חייבים תחילה להגדיר אזורי עניין תלת־ממדיים קטנים על גבי ה‑MRI, המשמשים ככוסות מדידה לנתוני ה‑PET. שרטוט ידני של אזורים אלה הוא עבודה איטית ומייגעת ועלול להשתנות בין מומחה למומחה. תוכנות קיימות יכולות לאתר באופן אוטומטי רק את המבנים הגדולים יותר ולעיתים מתקשות בחולים שמוחם מצטמק או מעוות — מצב שכיח במחלות נוירודגנרטיביות מתקדמות. ליקויים אלה יכולים לטשטש את דפוס הנזק האמיתי ולהחליש את יכולת הדימות ככלי אבחוני.
עוזר חכם בשני שלבים
החוקרים תיכננו את StriaSeg‑iARM כמערכת למידה עמוקה בת שני שלבים הפועלת ישירות במרחב המוחי של כל מטופל במקום לכפות את הסריקה לתבנית סטנדרטית. בשלב הראשון התוכנית מוצאת את כלל האסטריאום ב‑MRI תלת־ממדי. בשלב השני היא מחלקת מבנה זה ל‑12 תת‑אזורים אנטומיים מכל צדדי המוח. בין שני השלבים טמונה החידוש המרכזי: שלב אינטראקטיבי שבו מומחה יכול במהירות לבדוק ואם צריך לתקן את הקו הגס שנוצר בשלב הראשון לפני שמריצים את חלוקת המשנה המדויקת. גישה זו משלבת את המהירות של האוטומציה עם מקרת־שיקול דעת של צופה אנושי מנוסה.
אימון ובדיקה במוחות מהעולם האמיתי
כדי ללמד את המערכת מה לחפש, הצוות אסף מאות סריקות MRI ממספר בתי חולים וסוגי סורקים, ויצר שרטוטים ידניים מדוקדקים של 12 תת‑האזורי האסטריאום. לאחר מכן הם בדקו את המודל בשני מאגרי נתונים חיצוניים שכללו גם MRI וגם סריקות PET הקשורות לדופמין: אחד ממטופלים עם פרקינסון בשלבים יחסית מוקדמים ומתנדבים בריאים, והשני מקבוצה קלינית מבוגרת יותר וסובלת מהצטמקות מוח משמעותית ואבחנות מעורבות. במקרים המאתגרים הללו StriaSeg‑iARM התאים בעקביות לשרטוטים הידניים של המומחים טוב יותר משיטות מבוססות אטלס מסורתיות וממודל למידה עמוקה חד‑שלבי פשוט יותר, עם חפיפה גבוהה יותר, גבולות מדויקים יותר ומדידות נפח יציבות.
מדידות חדות יותר לסריקות דימות כימי מוחי
מכיוון שהמטרה הסופית היא לכמת אותות PET, המחברים בדקו גם כיצד שיטות סגמנטציה שונות משפיעות על קריאות ה‑PET. בעזרת מדד סטנדרטי של קשירת טרייסר בכל תת‑אזור השוו התוצאות האוטומטיות עם אלה המבוססות על שרטוטים ידניים. שיטת האטלס נטתה להמעיט בקשירה, במיוחד בחולים עם שינויים חמורים יותר, בעוד שהמודל הבסיסי של הלמידה העמוקה עדיין הציג הטיה ניכרת בחלק מהאזורים. לעומת זאת, המודלים המדרגיים — ובפרט כאשר השתמשו בשלב התיקון האינטראקטיבי — ייצרו ערכי PET שעקבו מקרוב אחרי הוועד המומחה, עם הטיה ופיזור מינימליים. הצוות הראה בנוסף כי ציון אי־וודאות פשוט מהשלב הראשון יכול לסמן כ‑25% מהמקרים המאתגרים ביותר שבהם כוונון מומחה אכן נדרש, תוך שמירה על היתר אוטומטיים לחלוטין.
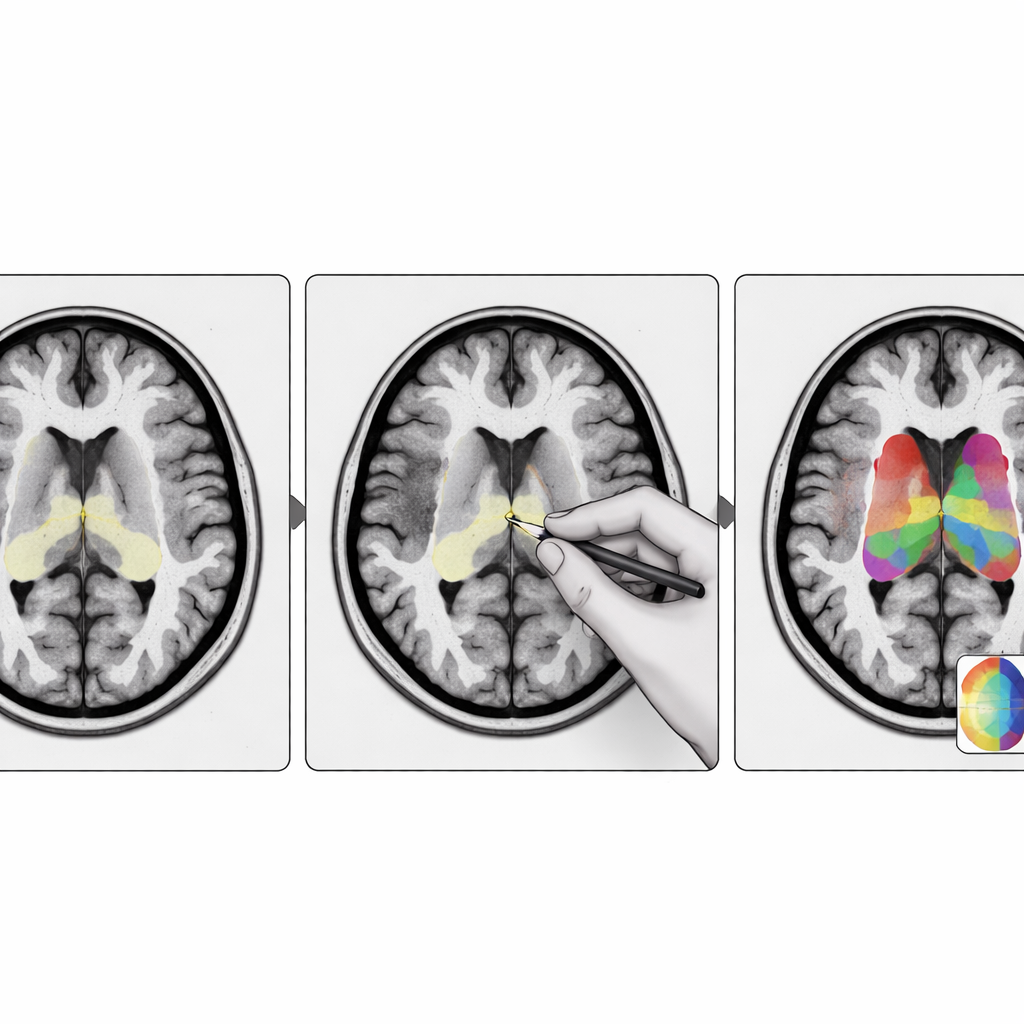
מה זה אומר לחולים ולרופאים
ללא‑מומחים, המסר המרכזי הוא שמפות דיגיטליות משופרות של אזורים מוחיים קטנים יכולות להפוך סריקות כימיות של המוח לאמינות יותר. StriaSeg‑iARM מספקת מסגרת גמישה שבה מודל למידה עמוקה עושה את רוב העבודה, אך מומחים עדיין יכולים להתערב ולתקן מקרים בעיתיים ללא צורך באימון מחודש של המערכת. השילוב הזה של אוטומציה ופיקוח מומחה משפר את דיוק המדידות המשמשות לאבחון ומעקב של הפרעות כמו מחלת פרקינסון, וניתן להתאימו לאיברים ומחלות אחרים שבהם מבנים קטנים וקשים לזיהוי מחזיקים רמזים חשובים.
ציטוט: Kim, J., Kim, D., Kim, S. et al. An interactive cascaded deep learning framework with expert refinement for accurate striatal subregion segmentation. Sci Rep 16, 6550 (2026). https://doi.org/10.1038/s41598-026-36399-0
מילות מפתח: דימות של מחלת פרקינסון, סגמנטציה של האסטריאום, למידה עמוקה ברדיולוגיה, PET ו‑MRI של המוח, סמנים ביולוגיים של מחלות נוירודגנרטיביות