Clear Sky Science · he
העלאת ביטוי MGMT מתווכת עמידות לטמוזולומיד שמוקנית על ידי תלות ב‑USP5
מדוע חלק מהגידולים במוח מפסיקים להגיב לתרופה מרכזית
לאנשים עם הסרטן האגרסיבי של המוח, גליובלסטומה, אחת התרופות העיקריות שעליהן רופאים סומכים היא טמוזולומיד. בהתחלה הכימותרפיה הזאת יכולה להאט את המחלה, אך הגידולים לעיתים לומדים להתעלם ממנה. המחקר בוחן שאלה פרקטית עם השלכות של חיים או מוות: מה בדיוק מאפשר לתאים הסרטניים להימלט מהתרופה, והאם ניתן למצוא נקודות תורפה חדשות להילחם בהן כדי שהטיפול יתחיל שוב להשפיע?
תרופה שעוזרת בתחילה, ואז מאבדת השפעה
טמוזולומיד פועל על ידי פגיעה ב‑DNA של תאים שמתחלקים במהירות, וכופה עליהם למות. עם זאת, רבות מהגליובלסטומות מייצרות חלבון תיקון בשם MGMT שיכול לבטל את הנזק הזה. מטופלים שהגידול שלהם מדליק את MGMT נוטים להחמיר מכיוון שהשפעת התרופה מבוטלת. רופאים יכולים לחזות במידה מסוימת את התגובה על‑ידי בדיקה האם גן MGMT מושתק כימית (מתילציה) או לא, אך זה לא מסביר במלואו מדוע מתפתחת עמידות או איך רמות MGMT נשמרות גבוהות בתוך תאי הגידול לאורך זמן.
עוזרים נסתרים שמגנים על חלבון התיקון
המחברים בחנו שכבת בקרה נוספת: ה"צוותי ניקיון" המולקולריים שמחליטים אילו חלבונים יושמדו ואילו יינצלו. תאים מסמנים בדרך כלל חלבונים בלויים לפירוק, בעוד שקבוצת אנזימים הנקראת אנזימי דה‑יוביקוויטינציה (DUBs) יכולה להציל חלבונים מגורל זה. באמצעות כרייה של מאגרי נתונים ציבוריים גדולים על סרטן ובחינת קווי תאים של גליובלסטומה עמידים שנגידו במעבדה, הצוות התמקד בשני אנזימים כאלה, USP5 ו‑USP8. במדגמי גידולים ממאות מטופלים, רמות גבוהות יותר של USP5 נטו להופיע יחד עם רמות גבוהות יותר של MGMT, ומטופלים שלגידוליהם היו שני הגנים מופעלים ברמה גבוהה בדרך כלל מתו מוקדם יותר.
בניית עמידות במעבדה
כדי לחקות את מה שקורה בחולים, החוקרים חשפו לאט שתי שורות תאים נפוצות של גליובלסטומה למינונים עולה של טמוזולומיד עד שהתאים הפכו לעמידים. בתאים המקשים האלה עלו כמה DUBs, אך USP5, USP8, USP10 וחלבון התיקון MGMT הועלו במיוחד. כאשר הצוות השתמש במולקולות RNA קטנות להשתקה של USP5 או USP8, התאים העמידים הפכו פתאום לפגיעים: הם הפעילו תוכניות הרס עצמי, כולל אפופטוזה וצורה של עיכול עצמי מונע־לחץ שמכונה אוטופאגיה. במקביל, רמות MGMT ירדו בכוח, וחלבון נוסף המקושר לעמידות, USP10, ירד גם הוא, מה שמרמז שהאנזימים האלה תופסים מיקום בראש רשת הישרדות.
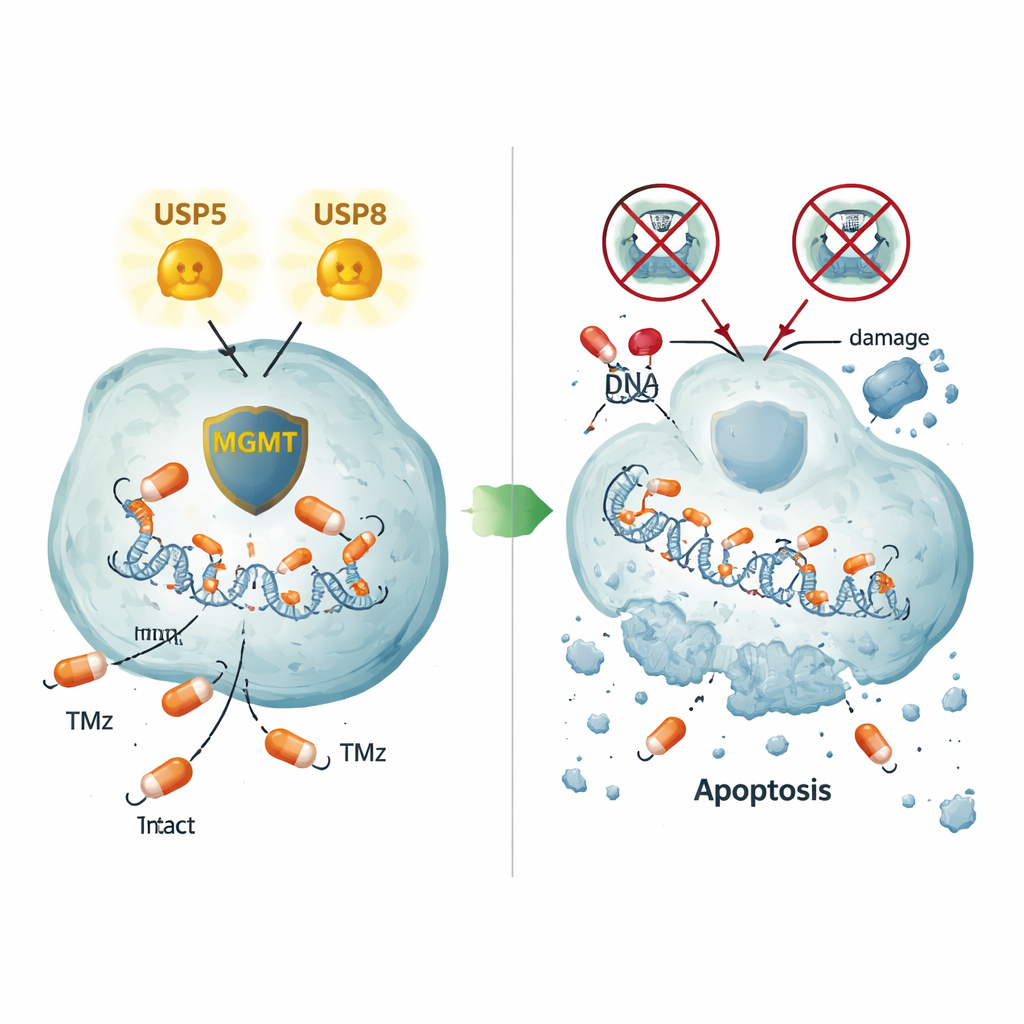
שתי דרכים שונות לשמור על MGMT בחיים
הדמיה מדוקדקת של תאי גידול ורקמת גידול אנושית הראתה כי USP5 ו‑MGMT לעתים יושבים יחד באותן אזורים של התא, במיוחד בציטופלסמה. חסימת USP5 לא רק הורידה את MGMT אלא גם גרמה ל־MGMT להישבר על‑ידי מכונת פירוק החלבונים של התא, תהליך שניתן היה להפוך עם התרופה בורטזומיב, שחוסמת את הפרוטאוזום. ייצור יתר של USP5 בתאים שאינם מבטאים בדרך כלל MGMT הספיק להעלות את רמות חלבון MGMT, אפילו בקו תאי שאינו מוחי, ובכך אישר השפעה מייצבת ישירה. USP8 התגלה כפעיל באופן שונה: השתקתו גם היא הורידה את MGMT, אך בלי לשנות את USP5 עצמו, וחושפת מסלול שני, בלתי תלוי ב‑USP5, שעוזר לשמור על MGMT. אפילו בקו תאים עמיד שלא ייצר כלל MGMT, כיבוי USP5 או USP8 עדיין השיב מוות תאי נרחב, מה שמצביע על מסלולי עמידות נוספים הנשלטים על‑ידי אנזימים אלה.
קישורים למערכת החיסון ורעיונות טיפוליים חדשים
מעבר לעמידות לתרופות, המחקר קושר את USP5 לאופן שבו גליובלסטומה מתקשרת עם מערכת החיסון. ניתוח נתוני גנום הציע ששינויים ברמות USP5 ובמספר העתקים של הגן משנים את האיזון של סוגים שונים של תאי חיסון סביב הגידול, כולל תאי T קטלניים ותאי T רגולטוריים. עבודות קודמות גם הראו כי USP5 יכול לייצב את PD‑L1, חלבון שהגידולים משתמשים בו כדי להשתיק תאי T תוקפים. אם לוקחים את הכול ביחד, הממצאים מציעים ש‑USP5 עשוי לסייע לגידולים הן לשרוד כימותרפיה והן להתחמק ממתקפת מערכת החיסון, מה שהופך אותו למטרה תרופתית אטרקטיבית במיוחד.
מה זה אומר לטיפול עתידי בסרטן מוח
במילים פשוטות, עבודה זו מזהה את USP5 ו‑USP8 כשומרי ראש מרכזיים שמגינים על חלבון התיקון MGMT ועוזרים לתאי גליובלסטומה לעמוד בעמידות לטמוזולומיד. על‑ידי פירוק שומרי הראש האלה, המחברים הצליחו להרוג תאים עמידים לתרופות במעבדה ולהוריד רמות MGMT, אפילו במקרים מסוימים שבהם עמידות מבוססת MGMT לא הייתה הבעיה היחידה. זה מייצר תקווה שתרופות עתידיות המכוונות ל‑USP5 או ל‑USP8, ייתכן בשילוב עם כימותרפיה קיימת ותרופות מבוססות חיסון, יוכלו להחזיר את הרגישות של גידולים עקשניים ולתת למטופלים זמן נוסף.
ציטוט: Bhardwaj, S., Sanjay, Sharma, D. et al. MGMT upregulation mediates Temozolomide resistance conferred USP5 dependency. Sci Rep 16, 6118 (2026). https://doi.org/10.1038/s41598-026-36379-4
מילות מפתח: גליובלסטומה, עמידות לטמוזולומיד, MGMT, USP5, אנזימי דה‑יוביקוויטינציה