Clear Sky Science · he
פיקוח גנומי ארצי על השתמרויות בדם של Klebsiella pneumoniae עמידות לקרבפנמים ולקוליסין בתאילנד (2020–2024)
עלייה בזיהומים קטלניים בדם
בתי חולים ברחבי העולם מתמודדים עם מגמה מדאיגה: חיידקים נפוצים שבעבר נכנעו לאנטיביוטיקות החזקות שלנו הופכים בקושי ניתנים לטיפול. המחקר הזה מתמקד ב‑Klebsiella pneumoniae, מיקרואורגניזם היכול לחדור לזרם הדם ולגרום לזיהומים מסכני חיים, ועוקב כיצד הוא השתנה ברחבי תאילנד כדי לעמוד בעמידות אפילו בפני תרופות קו אחרון. הבנה היכן הסופרבאגים האלה מתפשטים ואיך הם מתחמקים מטיפולים חיונית להגנה על מטופלים, להנחיית החלטות רופאים ולעיצוב מדיניות בריאות הציבור.
מעקב אחרי סופרבאג תזרימי ברחבי אומה
החוקרים ניתחו 227 דגימות של Klebsiella pneumoniae שנלקחו מדם של חולים בבתי חולים ברחבי תאילנד בין 2020 ל‑2024. דגימות אלה הגיעו מרשת פיקוח ארצית שאוספת באופן שגרתי נתונים על זיהומים עמידים לתרופות. בדיקות מעבדה הראו שמעבר ל‑93% מהבודדים מהדם היו עמידים לקרבפנמים, קבוצה חזקה של אנטיביוטיקות שמשתמשים בה כאשר תרופות אחרות נכשלות. בדאגה רבה, כמעט שליש מהזנים העמידים לקרבפנמים היו גם עמידים לקוליסין, אחת מאפשרויות הקו האחרון שאליהן פונים רופאים כשאין כבר מה לעשות. בשילוב בדיקות תרופתיות סטנדרטיות עם רצף גנומי מלא, הצוות יכול היה לראות לא רק אילו תרופות נכשלו, אלא גם אילו תחבולות גנטיות השתמשו החיידקים כדי לשרוד.
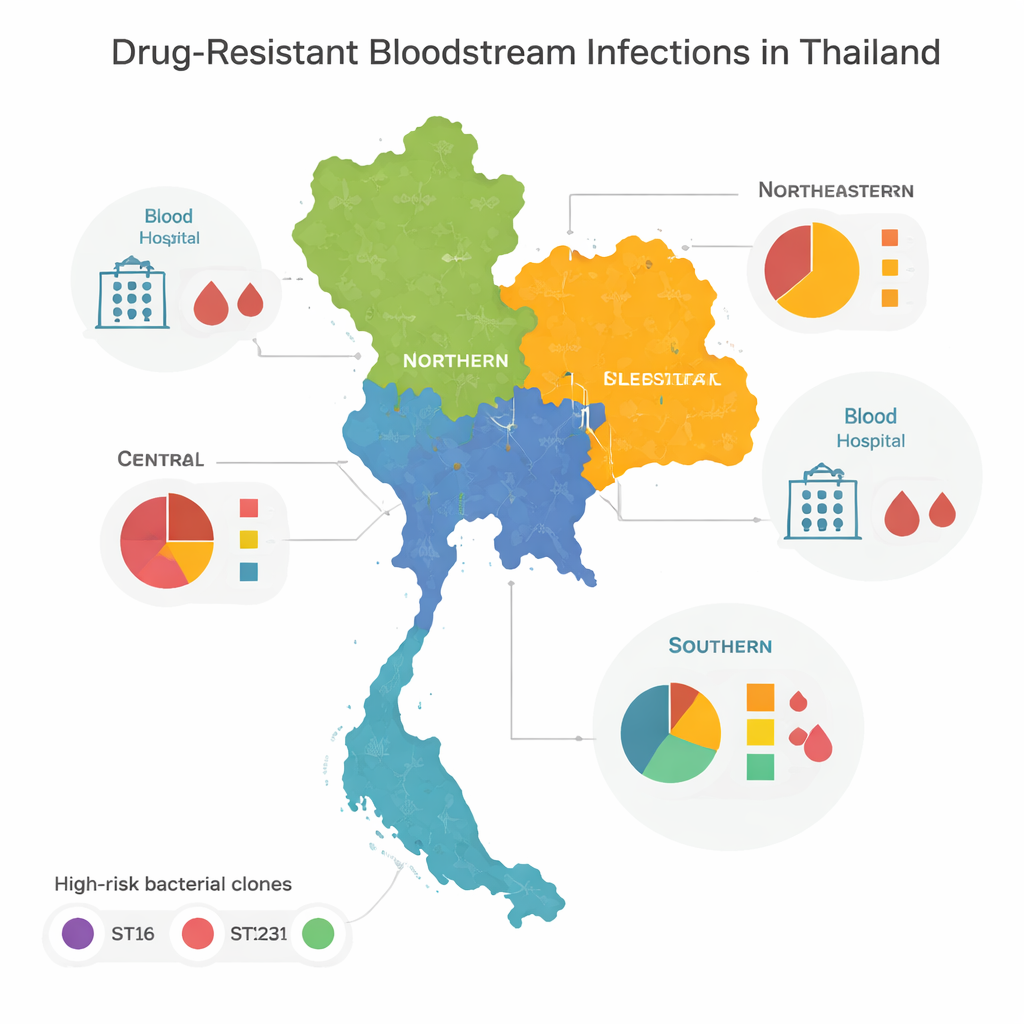
שיבוטים בסיכון גבוה ודפוסי אזור
כשהצוות השווה בין הגנומים, נמצא שרוב החיידקים העמידים השתייכו לכמה משפחות "בסיכון גבוה" או שיבוטים, המוכרים בעולם כולו כגורמים להתפרצויות בבתי חולים. שלושה מהם — ST16, ST147 ו‑ST231 — שלטו במיוחד במרכז, בצפון ובצפון‑מזרח תאילנד. שיבוטים אלה התפשטו באופן נרחב בין אזורים, מה שמרמז על תנועה תדירה של חולים, צוות או חיידקים בין בתי חולים. הדרום של המדינה נראה שונה: במקום שליטה של כמה סוגים בודדים, הופיעה שם שונות גדולה של סוגי שושלות חיידקיות, רבות מהן נצפו פעם אחת בלבד. המגוון הזה מרמז על תמהיל מורכב של התפרצויות מקומיות, מקורות סביבתיים ותנועה חוצת־גבולות במקום שיבוט אחד או שניים שמתפשטים בשליטה.
איך החיידקים עוקפים אנטיביוטיקות
המחקר חשף כיצד החיידקים משכפלים מנגנוני עמידות מרובים. רבים מזני ST16 ו‑ST231 נשאו גנים הידועים כ‑blaNDM ו‑blaOXA, המייצרים אנזימים שמפרקים אנטיביוטיקות קרבפנם לפני שהן יכולות להשפיע. אצל חלקם היו גם שינויים בממברנה החיצונית שמצמצמים כניסת תרופות, ובשילוב נוצרה עמידות ברמה מאוד גבוהה. זני ST231 נשאו לעיתים קרובות גם גן נוסף, rmtF1, שמחסום קבוצה חשובה של תרופות שנקראות אמינוגליקוזידים, וצמצם עוד יותר את אפשרויות הטיפול. ST147 בלט בגמישות הגנטית שלו: הוא שולב וערבב גני עמידות ופלאסמידים שונים — טבעות DNA ניידות — מה שהופך אותו לצומת פוטנציאלי להפצת תכונות עמידות לחיידקים אחרים.
כשלי קו‑אחרון וסכנות חבויות
הממצא הכי מעורר דאגה עסק בעמידות לקוליסין, התרופה שהרופאים שומרים למקרים נואשים. כמה משפחות חיידקיות נדירות נשאו גני mcr, שיכולים לעבור בין מינים על גבי פלאסמידים ולגרום ישירות לעמידות לקוליסין. אחרות, במיוחד בתוך השיבוט ST16, היו עמידות לקוליסין אף על פי שלא זוהו בהן גנים או מוטציות ידועים לעמידות. זה מצביע על כך שמדענים עדיין לא מיפו את כל הדרכים שבהן חיידקים יכולים לנטרל את תרופת הקו‑האחרון הזו. הצוות גם זיהה זנים היפרוירולנטיים — חיידקים שמסוגלים לגרום למחלה קשה במיוחד — כולל שושלת ששילבה וירולנטיות גבוהה עם עמידות לכל הקרבפנמים שנבדקו, תערובת מסוכנת במיוחד.
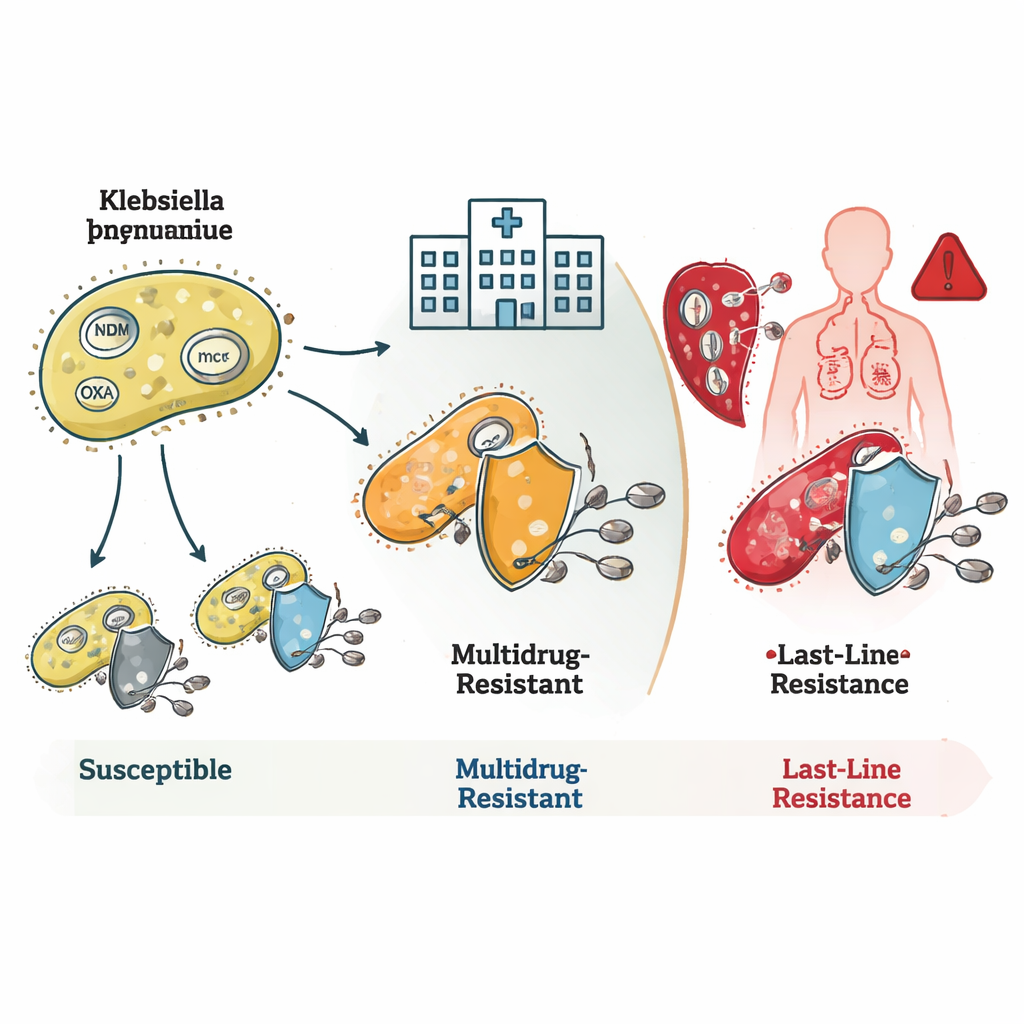
למה פיקוח גנומי חשוב
כדי להבין כיצד שינויים גנטיים התרגמו לכישלון תרפי במציאות, החוקרים השתמשו במודלים סטטיסטיים כדי לקשר גנים ספציפיים לעמידות כפי שהודגמה בבדיקות מעבדה. גנים כמו blaNDM‑1 וקרוביהם הראו קשרים חזקים מאוד עם עמידות לקרבפנמים, ואישרו את תפקידם המרכזי בגרימת כישלון טיפול. עם זאת, לגבי קוליסין — רוב החיידקים העמידים לא הראו סמנים מוכרים לעמידות, מה שמצביע על מנגנונים חבויים שעדיין יש לגלות. המחברים טוענים ששימוש שגרתי בריצוף גנומי מלא במסגרת פיקוח בתי חולים יכול לפעול כרדאר אזהרה מוקדמת: לאתר שיבוטים בסיכון עולה, לעקוב אחרי תנועתם בין אזורים וגבולות, ולהנחות תגובות מהירות בשליטה בזיהומים.
מה משמעות הדבר למטופלים ולמדיניות
בעבור קורא שאינו מומחה, המסר חמור אך ברור: חלק מזיהומי הזרם הדם בתאילנד נגרמים כיום על ידי חיידקים העמידים כמעט לכל התרופות שהרופאים יכולים להציע, וכמה משפחות מסוכנות של מיקרואורגניזמים אלה מתפשטות במידה נרחבת. יחד עם זאת, המחקר מראה שעם הכלים הנכונים — דגימה ארצית, ניתוח גנטי ושיתוף מהיר של נתונים — מערכות בריאות יכולות לזהות איומים אלה מראש ולהתאים את עצמן. הרחבת הפיקוח הגנומי, פיתוח בדיקות מולקולריות מהירות והקשחת כללי בקרת זיהומים עשויים לסייע להאט את התקדמות הסופרבאגים האלה ולרכוש זמן לפיתוח טיפולים וחיסונים חדשים.
ציטוט: Krobanan, K., Kamjumphol, W., Leethongdee, P. et al. Nationwide genomic surveillance of carbapenem- and colistin-resistant Klebsiella pneumoniae bloodstream isolates in Thailand (2020–2024). Sci Rep 16, 5853 (2026). https://doi.org/10.1038/s41598-026-36228-4
מילות מפתח: עמידות נגד מיקרוביאלית, Klebsiella pneumoniae, זיהום בזרם הדם, פיקוח גנומי, מערכת הבריאות בתאילנד