Clear Sky Science · he
קרינת γ גורמת לשינויים תת‑תאיים אזוריים בסמנים של טרשת נפוצה של תאים מוטוריים ודמנציה פרונטו‑טמפורלית במוח חזירים
מדוע מינונים קטנים של קרינה ומוחות חזירים חשובים
רובנו נוטים לחשוב על קרינה כמשהו מזיק, במיוחד למוח. עם זאת, עולמנו מלא ברמות נמוכות של קרינה שמקורן בסריקות רפואיות, בטיסות ובסביבה. בו‑זמנית, המדענים עדיין מנסים להבין מה גורם לטרשת נפוצה של תאים מוטוריים (ALS), המחלה הממית שהשיתקה את שחקן הבייסבול לו גריג, ולבני דודה הקרובה, הדמנציה הפרונטו‑טמפורלית (FTD), שמתקיפה התנהגות ואישיות. המחקר הזה שואל שאלה מפתיעה ומעט תקווה: האם מנה אחת צנועה של קרינת גמא עשויה לשנות בעדינות את הכימיה המוחית בדרכים שאינן בהכרח מזיקות — ואולי אף מגנות — מפני השינויים המולקולריים הקשורים ל‑ALS ו‑FTD?
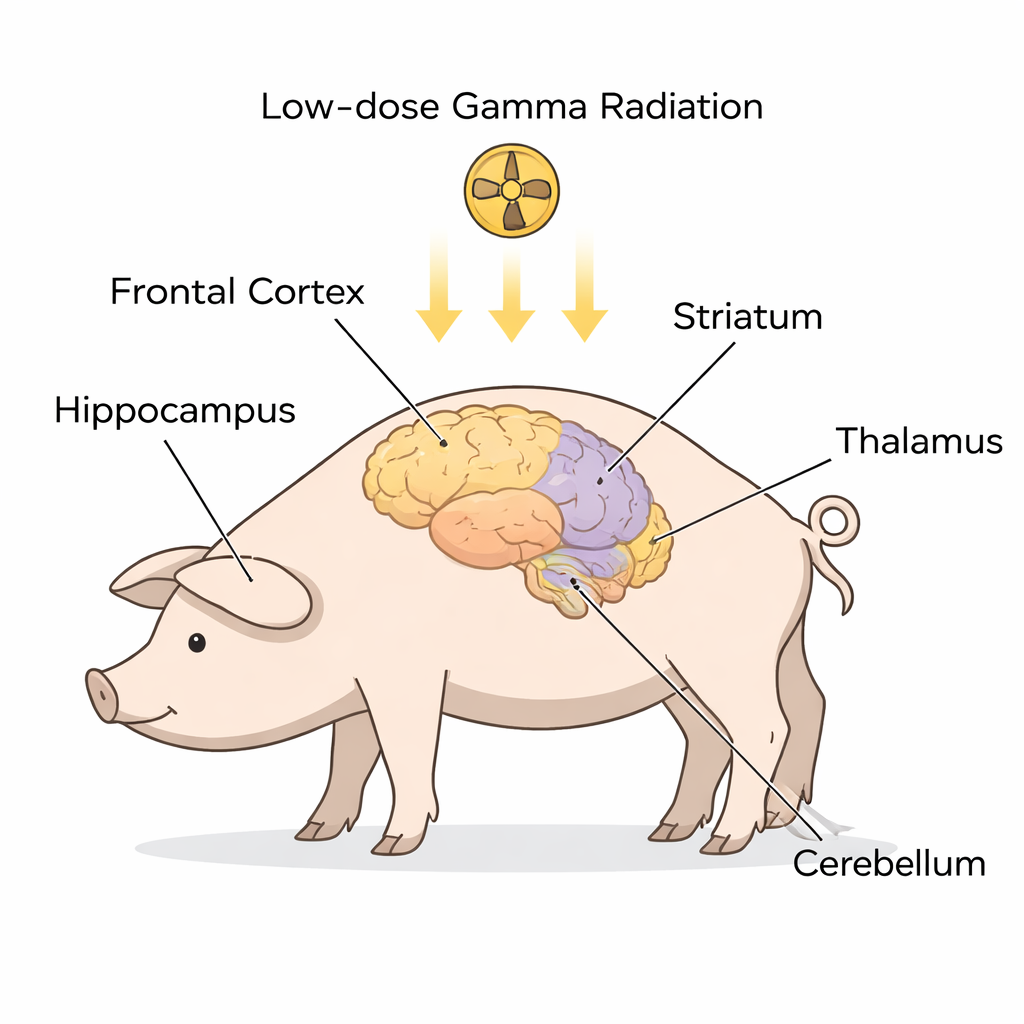
מבט מקרוב על סימנים מצביעים ל‑ALS במוח
במקום לבדוק מטופלים שכבר חלו ב‑ALS, החוקרים עבדו עם מיניפיגים מסוג גוטינגן בריאים, שמוחותיהם דומים מבחינה אנטומית לשלנו. תשעה בעלי חיים קיבלו חשיפה גוף‑שלמה חד‑פעמית של קרינת גמא במינון נמוך, בעוד ששישה הועברו להרדמה אך לא הושמו תחת קרינה ושימשו קבוצת ביקורת. כשבוע לאחר מכן פשטו המדענים חמישה אזורים מוחיים מרכזיים שלרוב מעורבים ב‑ALS ו‑FTD — קליפת המוח הפרונטלית, היפוקמפוס, סטריאטום, תלאמוס/היפותלמוס והמוחון. בכל אזור הם הפרידו את תכני התא לשני תאים מרכזיים: הציטופלזמה (נוזל התא) והגרעין (המחלקה שמכילה את ה‑DNA). באמצעות טכניקה שנקראת ווסטרן בלוט מדדו את רמות כמה חלבונים שקשורים חזק ל‑ALS ול‑ALS‑FTD, כולל SOD1, FUS, C9orf72, STMN2, ubiquitin, TDP‑43 וצורתו המותמרת — TDP‑43 מזורחן.
הקרינה משאירה חלק מהסמנים ללא שינוי — ואחרים משתנים
ממצא המנחם היה שרמות כוללות של SOD1, חלבון שלשינואותיו גורמות לחלק ממצבי ה‑ALS התורשתיים, לא השתנו באף אזור אחרי הקרינה. באותו אופן, הצורות המרכזיות של TDP‑43 — החלבון שמצטבר בתאי המוח בחולי ALS — נשארו יציבות גם בגרעין וגם בציטופלזמה בכל האזורים. אך לא הכול היה סטטי. הצוות הבחין בשינויים ספציפיים לאזור ולמחלקת התא בכמה חלבונים אחרים. לדוגמה, FUS, חלבון שבדרך‑כלל חי בגרעין אך יכול להתנהג באופן לקוי ולצבור ב‑ALS, ירד בציטופלזמת התלאמוס/היפותלמוס לאחר הקרינה, בעוד שרמותיו בגרעין עלו בקליפת המוח הפרונטלית וירדו בהיפוקמפוס. החלבון המקושר ל‑ALS, C9orf72, לא השתנה בנוזל התא אך הציג ירידה בגרעיני ההיפוקמפוס. גם STMN2, חלבון חשוב לשמירה על סיבי העצב, ירד בגרעיני ההיפוקמפוס, דבר שמעיד על תגובה מקושרת בין שני המולקולות באזור זה הקשור לזיכרון.
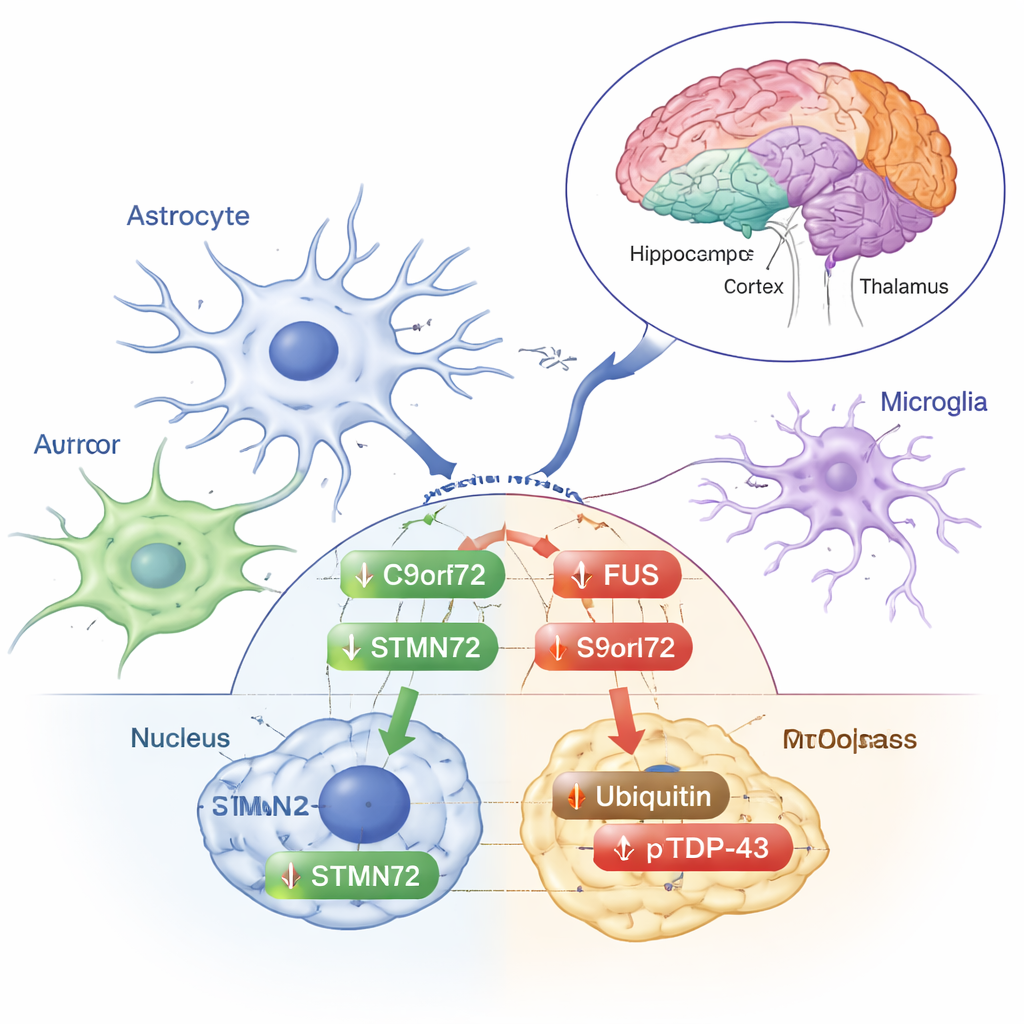
אותות של מתח או הגנה מוקדמת?
שינויים אחרים נראו יותר כמו תגובות מתח קלאסיות. ubiquitin — התג הקטן שהתא משתמש בו כדי לסמן חלבונים פגומים לניקוי — עלה בחלק הציטופלזמטי של קליפת המוח הפרונטלית. הצורה המזורחנת של TDP‑43, שלעיתים מצטברת בפקדות בלתי תקינות ב‑ALS וב‑FTD, עלתה בציטופלזמה של קליפת המוח הפרונטלית, סטריאטום ותלאמוס/היפותלמוס, אף על פי שרמות ה‑TDP‑43 הכוללות לא השתנו. שינויים אלה מצביעים על כך שקרינה במינון נמוך מעוררת במקצת את מנגנוני הטיפול בחלבונים של המוח מבלי להוביל לתבניות המלאות של קיפול לקוי והצטברות המאפיינות מחלה. המחברים מדגישים שהתגובות האלה משתנות לפי אזור מוחי ובהתאם למקום שבו החלבון נמצא בתוך התא או מחוצה לו, מה שמבליט עד כמה תגובת המוח למתח היא מדויקת ומותאמת.
מה זה עשוי להעיד לגבי הסיכון ל‑ALS — ואפשרויות תועלת
האם זה אומר שקרינה במינון נמוך גורמת ל‑ALS? הנתונים נוטים לשלול תשובה חד‑משמעית בחיוב. החוקרים לא ראו את ההזזה האופיינית או הצטברות של חלבוני ה‑ALS המרכזיים, ורבים מהשינויים מצביעים על ויסות משתנה במקום על פגיעה גמורה. באופן מעניין, התוצאות משתלבות עם עבודות קודמות של אותה קבוצה וקבוצות אחרות שמציעות שלפעמים כמויות קטנות של קרינה יכולות לעורר “הורמזיס” — תופעה שבה מתח מתון מפעיל מסלולי תיקון ומפחית חלבונים מזיקים, כמו אלה שקשורים לאלצהיימר או לפרקינסון במודלים של בעלי חיים. המחקר הנוכחי מרמז שלפחות בטווח הקצר, מנה אחת נמוכה של קרינת גמא משנה סמני ALS בדרכים שעשויות להיות אדפטיביות במקום הרסניות.
שאלות גדולות ותקווה זהירה
לעורכי קריאה כלליים, המסקנה המרכזית היא שהקשר בין קרינה לבריאות המוח מורכב יותר מאשר “כל הקרינה מזיקה”. במודל חיה גדול זה, חשיפה לקרינת גמא במינון נמוך יצרה שינויים עדינים ותלויי‑אזור בחלבונים המקושרים ל‑ALS ו‑FTD, מבלי לשחזר את דפוסי הנזק שנצפים במוחות חולים. שינויים אלה עשויים לשקף את ניסיון המוח להתמודד עם המתח ולתקן אותו, ובמקרים מסוימים אף להועיל. עם זאת, המחקר בחן רק חודש לאחר חשיפה יחידה, ורק במוח (ולא בחוט השדרה, שבו ה‑ALS פוגע בעוצמה הגדולה ביותר). נדרשים מחקרים ארוכי‑טווח ובחינות במתן חוזר לפני ששוקלים לתרגם ממצאים אלה לבני אדם. עם זאת, העבודה פותחת חלון חדש על האופן שבו קרינה ברמות יומיומיות מתקשרת למולקולות שעומדות בבסיס מחלות ניווניות הרסניות — ומעלה את האפשרות שבעתיד, בתנאים מבוקרים, מנות קטנות עשויות לשמש לעידוד מנגנוני ההגנה של המוח.
ציטוט: Iacono, D., Murphy, E.K., Perl, D.P. et al. γ-Radiation induces region-specific subcellular alterations of amyotrophic lateral sclerosis and frontotemporal dementia markers in swine brain. Sci Rep 16, 5627 (2026). https://doi.org/10.1038/s41598-026-36208-8
מילות מפתח: טרשת נפוצה של תאים מוטוריים, דמנציה פרונטו‑טמפורלית, קרינה במינון נמוך, חלבוני מוח, מודל מיניפיג