Clear Sky Science · he
מיקומי R5 ו‑R7 על שלדי הפלואורוקווינולונים מניעים פירוק של סיבי F‑actin
להפוך אנטיביוטיקות לעוזרות של המוח
מחלות מוח נפוצות רבות, מאלצהיימר ועד פרקינסון, חולקות עבריין חבוי: מוטות מבניים זעירים בתוך תאי העצב שמתקשים ונוקשים עם הזמן. מוטות אלה עשויים מחלבון בשם אקטין, שבמצב תקין מהווה חלק גמיש מהשלד הפנימי של התא. המחקר חוקר אפשרות מפתיעה — שמחלקה מוכרת של אנטיביוטיקות, הפלואורוקווינולונים, יכולה לעבור עיצוב מחדש כדי לפרק בעדינות את הצבירי אקטין המזיקים האלה ואולי לעזור להגן על המוח.
כששלד תא מתקלקל
תאי מוח בריאים מעצבים ללא הרף את השלד הפנימי שלהם כדי ליצור ולשנות חיבורים. סיבי אקטין הם מרכזיים בתהליך זה, נוצרים ומתמוססים לפי הצורך. תחת לחץ, עם זאת, אקטין עלול להיתקע בצברי מוטות עקשניים החוסמים את התא, מפריעים להובלת מטען חיוני ומעודדים הצטברות של חלבונים הקשורים למחלה כמו עמילואיד וטאאו. עם השנים צברים אלה עלולים להתפתח למבנים צפופים הידועים כגופי הירנו (Hirano bodies), הנצפים לעתים קרובות במוחות של אנשים עם מצבים ניווניים שונים. משום שתרופות מטרות־אקטין ידועות לעתים קרובות כעת לצרוך יתר על המידה, החוקרים מעוניינים למצוא מולקולות קטנות בטוחות יותר שיכולות להחליש צברים אלה מבלי לפגוע בתאים.
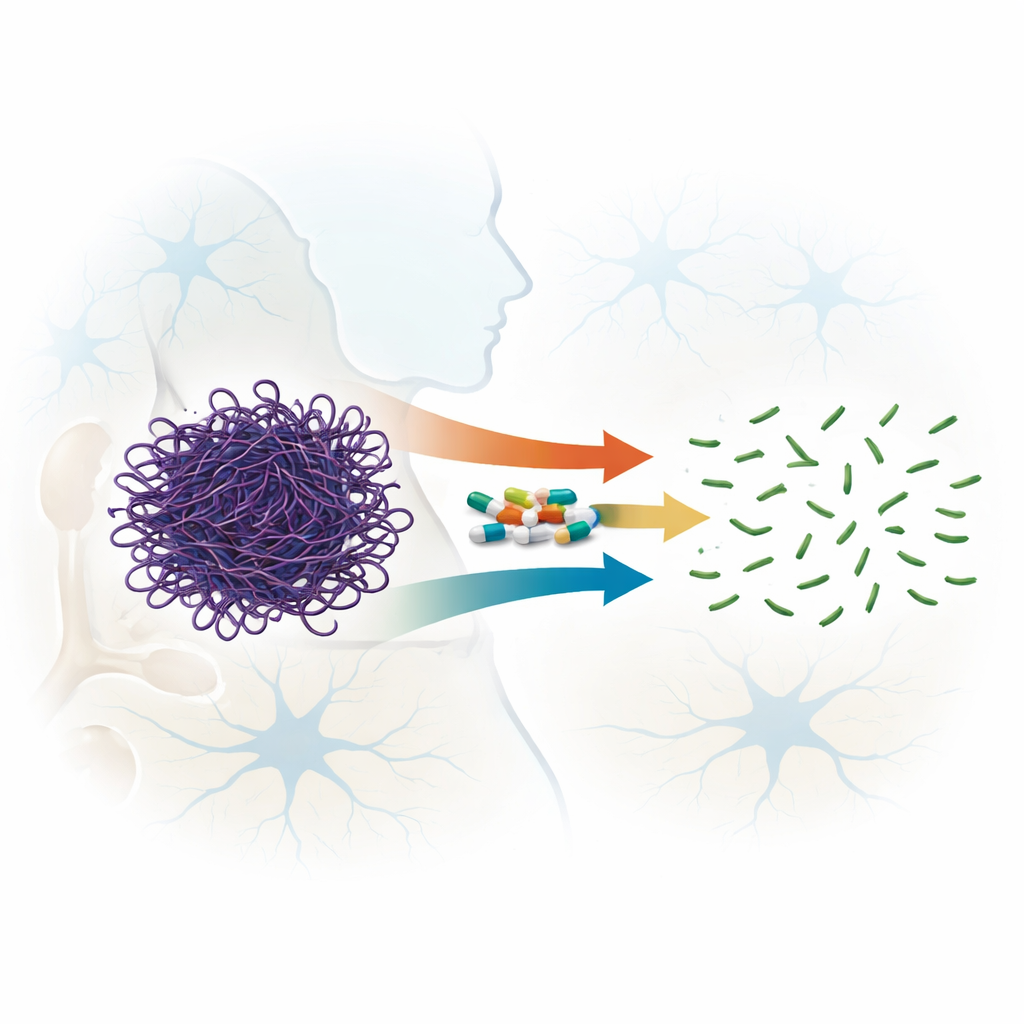
כישרון בלתי צפוי של תרופות מוכרות
פלואורוקווינולונים הן אנטיביוטיקות רחבות טווח המשמשות ברחבי העולם לטיפול בזיהומים, וחלק מהחברים החדשים במשפחה זו חודרים את מחסום דם‑מוח. רמזים מוקדמים הצביעו על כך שפלואורוקווינולונים מסוימים עלולים לייצב פחות את סיבי האקטין. בעבודה זו השוו המחברים באופן שיטתי שבע תרכובות קרובות, המשתרעות על פני ארבעה דורות של המשפחה, כדי לבדוק עד כמה הן מפרקות סיבי אקטין שנוצרו מראש ולא רק מונעות את היווצרותם. באמצעות מדידות פיזור אור, מיקרוסקופ אלקטרונים וסינון בגל, הם הראו שכל התרופות שנבדקו יכולות להפריע לסיבי האקטין, אך בעוצמות שונות מאוד. שתי תרופות, ספרפלקסין (דור שלישי) ומוקסיפלוקסצין (דור רביעי), בלטו בכך שהן קוטעות במהירות ובאופן בלתי הפיך סיבים ארוכים לחתיכות קטנות בהרבה, אפילו ביחסי תרופה‑ל‑חלבון יחסית נמוכים.
לראות את הסיבים מתמוטטים
דימות ברזולוציה גבוהה ובדיקות ביופיזיקליות חשפו כיצד הסיבים משתנים תחת טיפול תרופתי. מיקרוסקופ אלקטרונים הראה שאקטין שלא טופל יוצר גידים ארוכים ורציפים, בעוד שפלואורוקווינולונים יעילים ממירים אותם לרסיסים קצרים ומפוזרים. חברים בעלי עוצמה נמוכה יותר ייצרו סיבים כפופים ומעוקלים אך לא שברו אותם לחלוטין. מדידות יציבות מבוססות חום אישרו את השיבוש הפיזי הזה: לאחר הטיפול, האקטין התנהג יותר כמו צורתו החופשית, הלא מורכבת, עם טמפרטורת התכה נמוכה יותר, אך המבנה הבסיסי של היחידות נותר כמעט ללא שינוי. זה מצביע על כך שהתרופות אינן מקפלות או מפגועות באקטין עצמו — הן בעיקר מפרידות את האופן שבו היחידות נדבקות זו לזו בסיבים.
להתמקד באחיזה המולקולרית
כדי להבין מדוע חלק מהפלואורוקווינולונים יעילים יותר מאחרים, הצוות שילב ניסויי תהודה מגנטית גרעינית מתקדמת עם סימולציות מחשב של אינטראקציות תרופה‑חלבון. הם מצאו שכל התרכובות נשענות על "גרעין" טבעתי משותף ליצירת מגע עם האקטין, במיוחד בשני מקומות על אותו גרעין שנוגעים בסיב שוב ושוב. עם זאת, קבוצות כימיות נוספות המחוברות באתרים ספציפיים — הקרויות R5 ו‑R7 — משפיעות בעוצמה על כמה בחוזקה ובאיפה כל מולקולה נקשרת. במפרקות היעילות ביותר, עמדות אלה נושאות קבוצה אמינית ומערכות טבעת גדולות שחודרות לכיס קטן בממשק בין גדילי אקטין שכנים. שם הן מפריעות למגעים מייצבים מרכזיים, כולל גשר מלוח חשוב שלרוב מסייע לאחיזת הסיבים יחד.
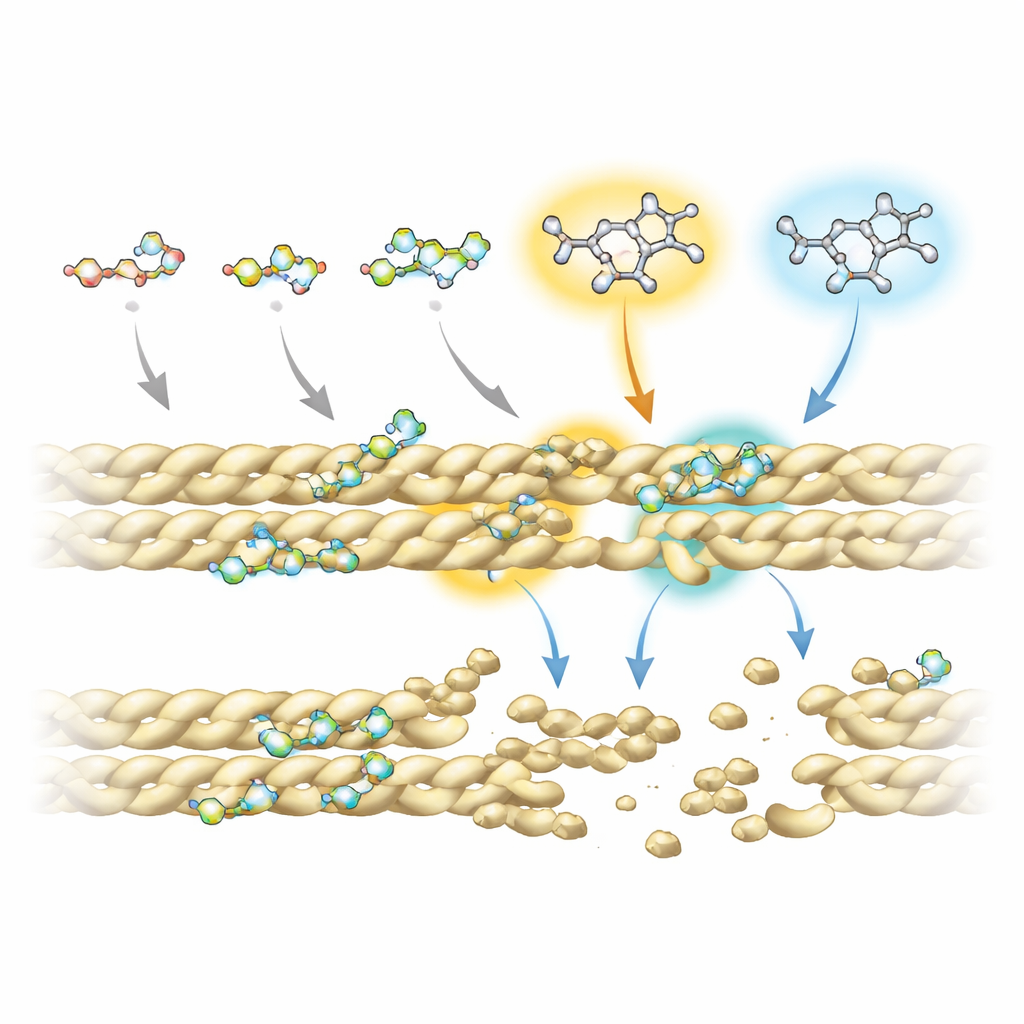
מתאי שמרים עד טיפולים עתידיים
החוקרים גם בדקו את התרופות בזן שמרים המצטבר בו באופן טבעי צברי אקטין, המדמה היבטים של תאים חולים. תחת המיקרוסקופ, שמרים שלא טופלו הראו גושי אקטין גדולים ובהירים, בעוד שהתאים שנחשפו לפלואורוקווינולונים — במיוחד ספרפלקסין, מוקסיפלוקסצין, ובמינונים גבוהים יותר נלידיקסיק אסיד — הציגו דפוסים מפוזרים ונקודתיים הרבה יותר, מה שמעיד על כך שהצברים נשברו. חשוב מכך, פעולת התרופות נראתה יחסית עדינה: הן החלישו את אריזת הסיבים ללא עיוות גס של הצורה הבסיסית של האקטין, והקשר שלהן היה חלש יותר מזה של רעלים קלאסיים של אקטין, מה שעשוי להפחית את הסיכון לתופעות לוואי קשות.
לעצב תרופות חכמות יותר המכוונות לאקטין
בסך הכל, המחקר מראה ששינויים זעירים באנטיביוטיקות מוכרות יכולים לשנות באופן דרמטי את האופן שבו הן מתקשרות עם השלד הפנימי של התא. על ידי זיהוי מיקומי R5 ו‑R7 כ"כפתורי שליטה" מרכזיים הן לפירוק האקטין והן לחציית מחסום דם‑המוח, המחברים מספקים מתווה ליצירת מולקולות חדשות בהשראת פלואורוקווינולון שמפרקות באופן סלקטיבי צברי אקטין מזיקים. ממצאים אלה הם הוכחה עקרונית מוקדמת במעבדה, אך הם מעוררים אפשרות שמוצרים עתידיים נגזרים מאנטיביוטיקות מוכרות יוכלו לעזור לנקות שלד רעיל בתאי עצב ולעכב או למנוע צורות מסוימות של ניווון עצבי.
ציטוט: Gupta, R.J., Nair, H., Sarhadi, T.R. et al. R5 and R7 positions on fluoroquinolone scaffolds drive F-actin filament disruption. Sci Rep 16, 9517 (2026). https://doi.org/10.1038/s41598-026-36089-x
מילות מפתח: אגgregטים של אקטין, אנטיביוטיקות פלואורוקווינולון, מחלות ניווניות של המוח, מיחזור תרופות, שלד תאיים