Clear Sky Science · he
למידה עצמית מונחית על גרפים חוזה אסוציאציות בין RNA שאינו מקודד למחלות
מדוע ה‑RNA הנסתר חשוב לבריאותנו
רבים מאיתנו למדו שתפקידו העיקרי של ה‑RNA הוא לסייע בבניית חלבונים. אך בעשור האחרון גילו מדענים כמות עצומה של מולקולות "RNA שאינן מקודדות" שמעולם לא הופכות לחלבונים ובכל זאת מסייעות לווסת את פעילות התאים שלנו. כיום ידוע שרבים מהמולקולות האלה יכולים לקדם או לדכא סרטן ומחלות מורכבות אחרות. זיהוי אילו RNAs שאינם מקודדים קשורים לאילו מחלות עשוי לחשוף דרכים חדשות לאבחון מוקדם או לעיצוב טיפולים מדויקים יותר — אך בדיקה ניסויית של כל האפשרויות תהיה איטית מדי. המחקר הזה מציג שיטה חזקה מבוססת מחשב שיכולה לסרוק רשתות ביולוגיות עצומות ולהציע בצורה מהימנה את הקשרים RNA–מחלה המבטיחים ביותר לבדיקה ניסויית.
מ״זבל״ לשחקנים מרכזיים בתא
שנים רבות זלזלו ב‑RNA שאינו מקודד כיתרה שנשארת לאחר פעילות הגן. היום אנו יודעים שמשפחות כגון מיקרו‑RNA, RNA ארוכים שאינם מקודדים ו‑circRNA מעורבות בתיאום של תהליכים חיוניים — מאריזת ה‑DNA ועד הדלקת או הכיבוי של גנים והעברת אותות בתוך התא. מכיוון שהן עומדות בנקודות בקרה רבות, גם שינויים קטנים ב‑RNA אלה עלולים להטות את המאזן לכיוון סרטן או מחלה אחרת. קלינאים כבר החלו לראות בהן סמנים ביולוגיים אפשריים וביעדי תרופה. האתגר הוא בקנה המידה: יש אלפי RNAs שונים ומאות מחלות, וניסויים מסורתיים לבחינת כל קישור אפשרי יקרים וגוזלים זמן. כאן נכנסת לתמונה חיזוי חישובי, שנותן דרך לצמצם את מרחב החיפוש.
איך קוראים רשת ביולוגית
שיטות ממוחשבות קודמות ניסו לחזות קישורי RNA–מחלה על ידי פירוק טבלאות נתונים גדולות לחלקים פשוטים או על ידי אימון מודלים של למידת מכונה על דוגמאות ידועות. גישות אלה סייעו, אך לעתים קרובות התעלמו מהאופן שבו RNAs ומחלות משוזרות לתוך רשתות. "רשתות עצביות גרפיות" מודרניות מטפלות ב‑RNA ומחלות כנקודות המחוברות בקווים, בדומה לרשת חברתית. הן יכולות ללמוד דפוסים של מי מקושר למי. עם זאת, רוב השיטות הגרפיות האלה זקוקות להרבה דוגמאות אימון אמינות ולמאפיינים קלט מעוצבים בקפידה. זה הופך אותן לרגישות לנתונים חסרים, למדידות רועשות ולהתאמת יתר — הופעה טובה על נתונים ידועים אך כישלון בחיזוי אסוציאציות חדשות.
ללמוד מהנתונים עצמם
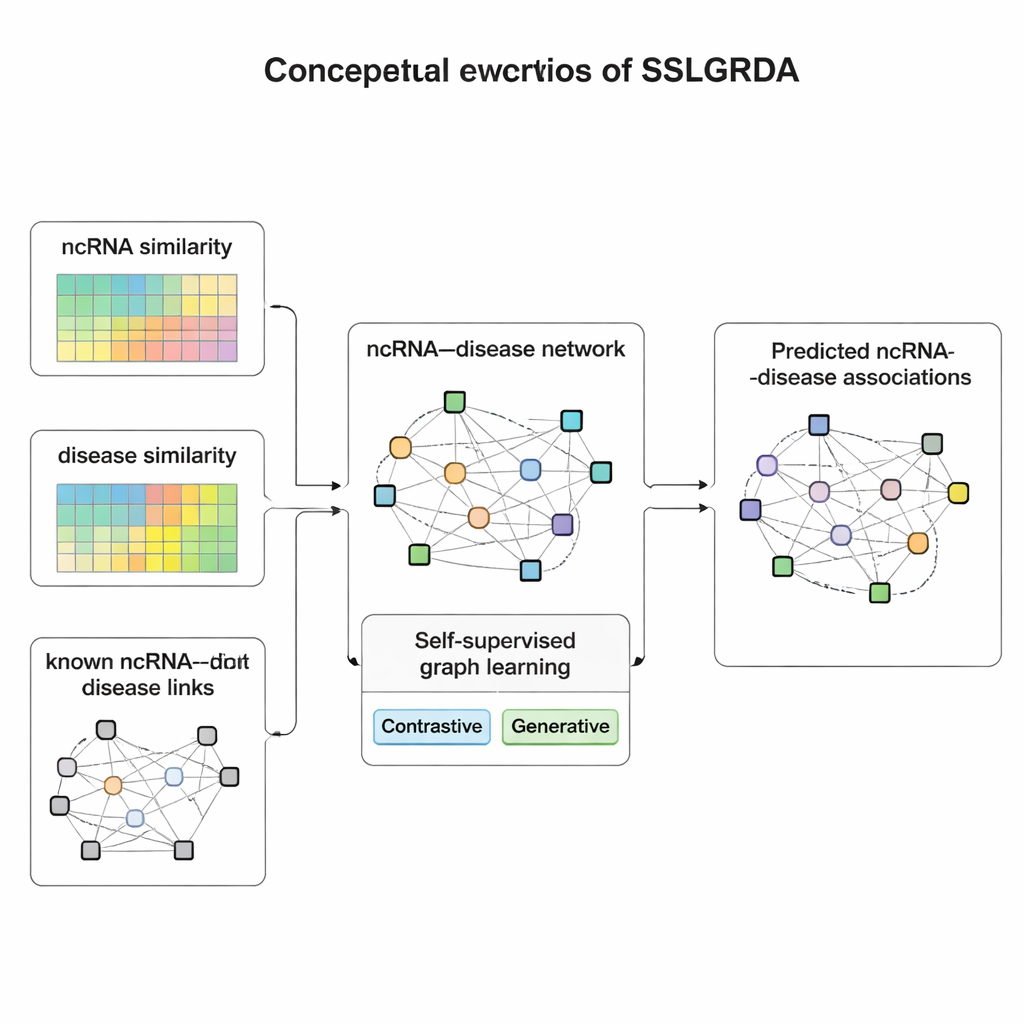
המחברים מציגים את SSLGRDA, מסגרת חדשה שמלמדת מודל גרפי לזהות דפוסים שימושיים בלי להסתמך רבות על נתוני אימון מתויגים. הרעיון המרכזי הוא "למידה עצמית מונחית": במקום להגיד למודל איזה RNA קשור לאיזו מחלה, המודל ממציא משימות תרגול משלו המבוססות רק על מבנה ותכונות הרשת. החוקרים בונים שני סוגי גרפים. אחד שומר על RNA ומחלות כסוגי צמתים נפרדים המחוברים בקישורים ידועים. השני מאחד אותם לרשת הומוגנית גדולה שכוללת גם מידע דמיון — כמה דומים שני RNAs או שתי מחלות — כך שגם פריטים בעלי חיבורים דלילים מקבלים שכנים תומכים. על גבי הגרפים האלה SSLGRDA משתמש בשני סגנונות אימון עצמי. אסטרטגיות ניגודיות מבקשות מהמודל לזהות ש"מבטים" שונים של אותו צומת (למשל, הקשרים שלו לעומת התכונות שלו) אמורים להניב ייצוגים פנימיים דומים, בעוד שמפרידים באופן ברור צמתים לא קשורים. אסטרטגיות גנרטיביות מסתירות כוונתית חלק מתכונות הקלט ומאתגרות את המודל לשחזרן, וכך מעודדות אותו לתפוס מבנה עמוק יותר במקום לשנן רעש.
בדיקת השיטה
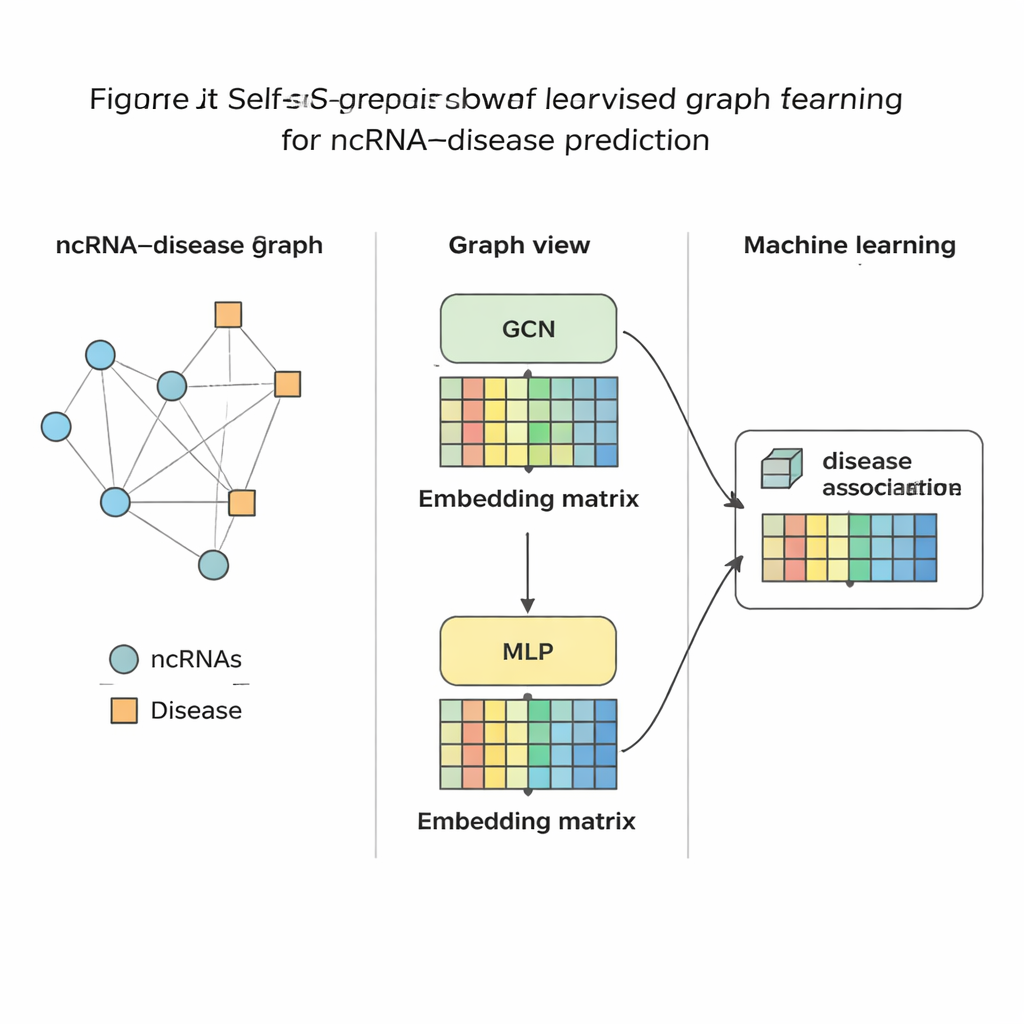
לאחר ש‑SSLGRDA זיקק כל RNA וכל מחלה לטביעת אצבע מספרית קומפקטית, מאמן סטנדרטי של למידת מכונה משמש כדי לשפוט האם קישור ביניהם סביר. המחברים העריכו גישה זו על תשעה מערכי נתונים שונים המכסים שלושה סוגי RNA עיקריים ומאות מחלות. באופן עקבי, הווריאנטים הבנויים על למידה עצמית ניגודית על הגרף המאוחד (ההומוגני) הציגו את התוצאות הטובות ביותר, והתעלו על מגוון כלים קיימים, כולל בסיסים גרפיים חזקים. השיטה לא רק השיגה דיוק גבוה יותר במבחנים גלובליים, אלא גם דירגה את השותפים הנכונים במקומות גבוהים כשממוקדים ב‑RNA או במחלה בודדת — דבר מכריע לשימוש מעשי שבו ביולוג עשוי להתחיל מסרטן יחיד ולשאול אילו RNAs כדאי לחקור. הם הראו עוד שהרעיונות הללו מועברים היטב לרשתות ביומדיקליות אחרות, כגון קשרים בין מיקרובים למחלות או לתרופות.
מחיזויים לטיפולים אפשריים
על מנת להדגים ערך מעשי, הצוות השתמש ב‑SSLGRDA כדי לחפש RNAs שאינם מקודדים חדשים המעורבים בסרטן השד, סרטן המעי ומצבים נוספים. רבות מההצעות שנמצאו במקומות גבוהים אושרו לאחר מכן בבסיסי נתונים או בדוחות מדעיים עצמאיים, מה שתומך ביכולת המודל לזהות דפוסים בעלי משמעות ביולוגית. עבור הלא‑מומחים, המסקנה היא שעבודה זו מספקת דרך חכמה יותר לכורים את הסבך המתמשך של נתונים ביולוגיים כדי למצוא רמזים נסתרים למחלות. על ידי למידה אוטומטית כיצד RNAs ומחלות מתקבצים ומתקשרים, שיטות גרפיות של למידה עצמית מונחית כמו SSLGRDA יכולות להנחות חוקרים מעבדתיים לעבר היעדים המבטיחים ביותר, ובכך להאיץ את הדרך מנתונים גולמיים לאבחונים וטיפולים משופרים.
ציטוט: Wu, Q., Tang, S. Self-supervised learning on graphs predicts non-coding RNA and disease associations. Sci Rep 16, 5231 (2026). https://doi.org/10.1038/s41598-026-36030-2
מילות מפתח: RNA שאינו מקודד, אסוציאציה למחלות, רשתות עצביות גרפיות, למידה עצמית מונחית, ביולוגיה חישובית