Clear Sky Science · he
חלבון KIN17 מקל על תחילת והתקדמות גידולי הכליה דרך מסלול PI3K‑AKT‑mTOR
למה המחקר הזה על סרטן הכליה חשוב
סרטן הכליה מאובחן בתדירות גבוהה יותר, אך עבור רבים מהחולים המחלה נשארת קשה לשליטה ברגע שהיא מתפשטת. המחקר בוחן את הדברים במיקרוסקופ — עד לרמת המולקולות הבודדות בתוך תאי הגידול — כדי להבין מה מניע את הגדילה והפלישה של גידולים כלייתיים והאם תרופה ניסיונית יכולה להאט את התהליך. הממצאים מצביעים על חלבון פחות מוכר, KIN17, כגורם מפריע חדש בסרטן הכליה ומציעים דרך לפגוע בו בעקיפין באמצעות טיפול טבלייתי.
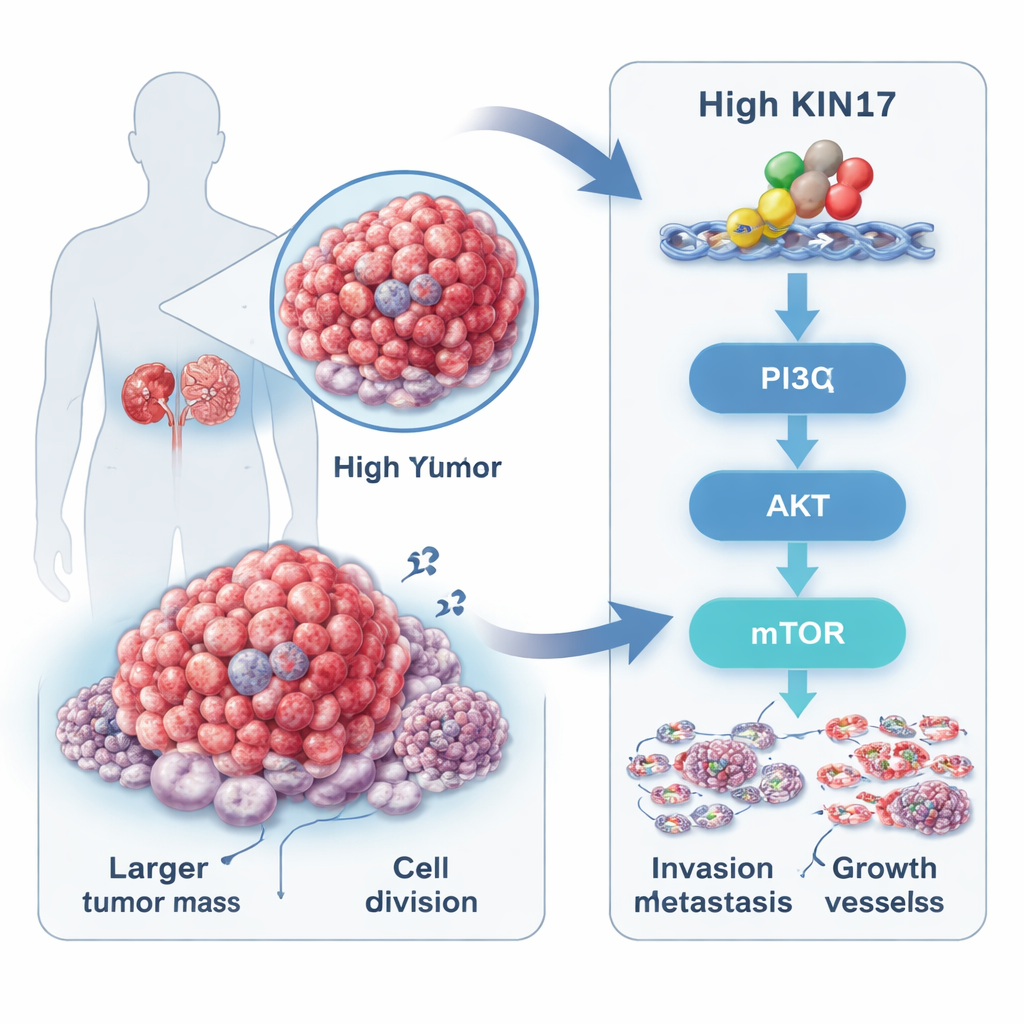
מניע חבוי בתוך גידולי הכליה
סרטן תא כלייתי, הצורה הנפוצה ביותר של סרטן הכליה, לעתים קרובות מתחיל ללא תסמינים ונמצא במקרים רבים בשלב מאוחר. החוקרים התרכזו בחלבון בשם KIN17, שידוע מזה זמן בתפקידיו בהגנה על DNA ובהעתקה שלו, אך רק לאחרונה נקשר גם לסוגי סרטן שונים. בניתוח מאגרי נתונים ציבוריים ובדגימות גידול מ‑88 חולים נמצא שרמות KIN17 גבוהות בהרבה בגידולים הכלייתיים לעומת רקמה סמוכה שאינה סרטנית. אצל חולים שהגידול שלהם כילל יותר KIN17 נצפו יותר גידולים גדולים, מחלה בדרגה גבוהה יותר, שלב מתקדם יותר ופיזור מרוחק יותר — והם חיו פחות זמן בהשוואה לאלה עם רמות נמוכות של KIN17. התבנית הזו רמזה ש‑KIN17 אינו סתם עד כדי סתירה, אלא קשור באופן הדוק לאגרסיביות הגידול.
בחינת KIN17 בתאי סרטן
כדי לגלות מה עושה KIN17 בתוך תאי סרטן כלייתיים, הצוות מהנדס שורות תאים מעבדתיות כדי להנמיך או להעלות את ביטוי KIN17. כאשר הקטינו את KIN17, התאים גדלו לאט יותר, יצרו פחות מושבות והיו פחות מסוגלים לנוע ולפלוש דרך ממברנות מלאכותיות. יותר מתאים אלה תקועים בשלב המנוחה של מחזור התא והידרדרו למוות, עם רמות גבוהות יותר של מוות מתוכנת. כאשר KIN17 בוצע עודף, קרה ההפך: התאים התרבו מהר יותר, שכפלו את ה‑DNA ביתר קלות, סגרו פערים בדומה לשריטות בשכבות תאים מהר יותר ופלשו באגרסיביות רבה יותר. ניסויים אלה הראו כי KIN17 מתנהג כדוושת הגז לצמיחה ולהתפשטות של תאי סרטן הכליה.
מסלול גדילה שנלכד בעשייה
החוקרים שאלו כעת כיצד KIN17 מפעיל את הכוח הזה. בדיקות פעילות גנים ובדיקות חלבון הצביעו על רשת ידועה של גדילה והישרדות בתאים, הקרויה מסלול PI3K–AKT–mTOR. מסלול זה משווה לעתים קרובות לצומת מרכזית שמנחה תאים מתי לגדול, להתחלק ולהימנע ממוות. בתאי סרטן כלייתיים עם רמות גבוהות של KIN17 נצפו אותות "הדלק" גבוהים יותר — תגיות כימיות הנקראות פוספטים — על רכיבים מרכזיים של המסלול, אף על פי שכמותם הכוללת של חלבונים אלה לא השתנתה. כאשר הורידו את KIN17, תגיות ההפעלה ירדו, ומולקולות הקשורות לתנועה ולפלישה של תאים השתנו גם הן. בניסויים בעכברים, גידולים שנבנו מתאים עשירים ב‑KIN17 גדלו גדולים ומהר יותר, וצביעה רקמתית הראתה שמסלול הגדילה הזה הופעל בעוצמה באותם גידולים.
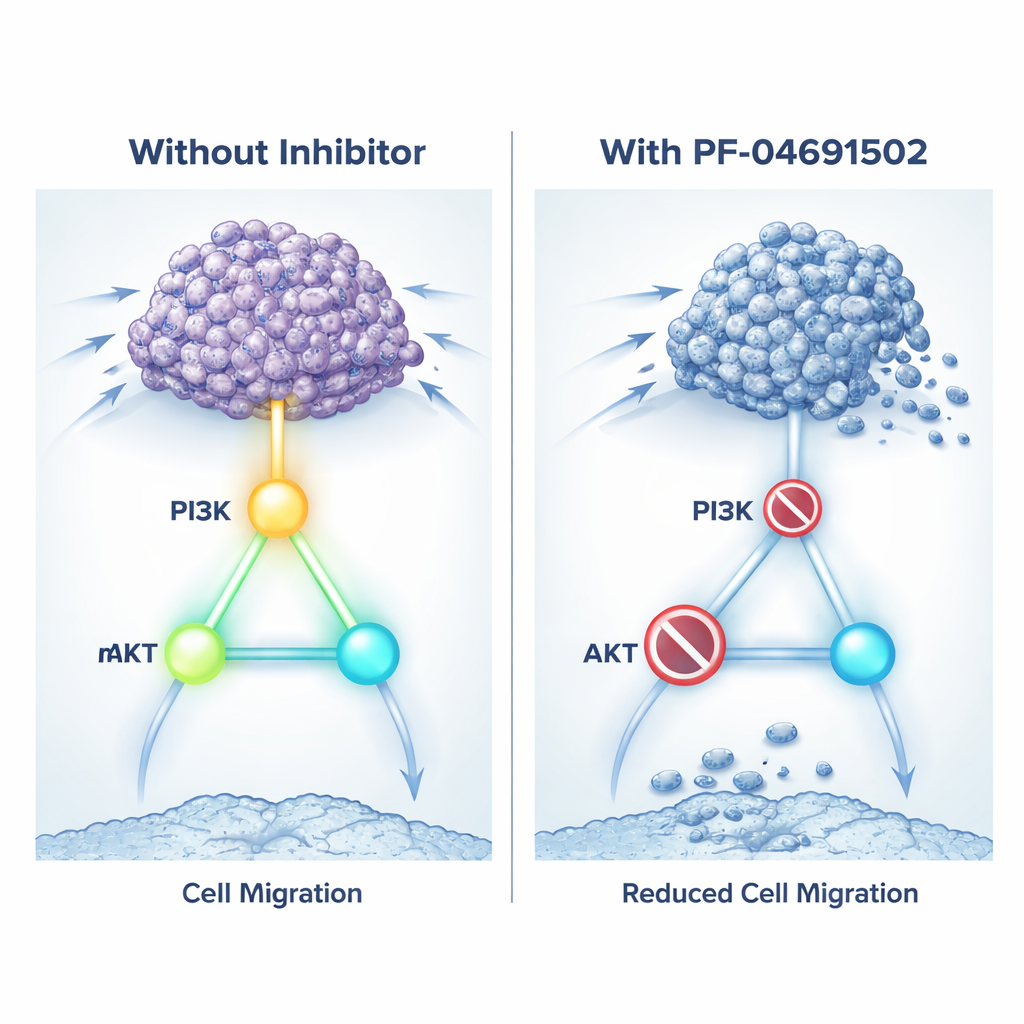
החלשת האות בעזרת תרופה דו‑מטרתית
מאחר שבלימת KIN17 ישירות אינה אפשרית עדיין באמצעות תרופות קיימות, הצוות ניסה טקטיקה שונה: לכבות את מסלול הגדילה שהוא נראה שולט בו. הם השתמשו ב‑PF‑04691502, תרופה ניסיונית החוסמת הן את PI3K והן את mTOR, שני מיתגים מרכזיים במסלול. במאכלות, טיפול בתאי סרטן כלייתיים עם ביטוי גבוה של KIN17 בעזרת המעכב הזה האט את צמיחתם, הפחית את יכולתם לנוע וליצור מושבות ודחף יותר תאים למוות. התרופה גם הורידה את תגיות ההפעלה על PI3K, AKT ו‑mTOR והורידה רמות של חלבונים הקשורים לפלישה. בעכברים נשאים גידולים כלייתיים, מינונים יומיים של PF‑04691502 הקטינו גידולים שמיצרו KIN17 במידה גבוהה והפחיתו סימנים להתחלקות תאים תוך עלייה באותות של מוות תאי. במהות, התרופה הצליחה להרגיע את ההשפעות המזיקות של KIN17 על ידי השתקת נתיב הגדילה שהוא מעדיף.
מה זה עשוי לשנות עבור חולים
עבור אנשים המתמודדים עם סרטן הכליה, הממצאים מציעים שתי רעיונות מעודדים. ראשית, מדידת KIN17 בדגימות גידול עשויה לעזור לרופאים להעריך עד כמה סרטן אגרסיבי ועד כמה צפוי להתפשט. שנית, גידולים התלויים מאוד ב‑KIN17 עשויים להיות פגיעים במיוחד לתרופות הפוגעות במסלול PI3K–AKT–mTOR, כמו PF‑04691502 או מעכבים דו‑מטרתיים דומים שנמצאים כבר בניסויים קליניים לסוגי סרטן אחרים. אמנם עוד דרוש עבודה רבה לפני שכל טיפול חדש יגיע למקבל, המחקר משרטט שרשרת ברורה של אירועים — מ‑KIN17, דרך מסלול צמיחה מרכזי, ועד להתרחבות בלתי מבוקרת של גידול — ומראה כי שבירת השרשרת הזו יכולה להאט את סרטן הכליה במעבדה ובחיות.
ציטוט: Wen, Y., Lyu, L., Zhang, H. et al. KIN17 facilitates the initiation and progression of renal tumor progression through the PI3K-AKT-mTOR pathway. Sci Rep 16, 5721 (2026). https://doi.org/10.1038/s41598-026-35851-5
מילות מפתח: סרטן תא כלייתי, KIN17, PI3K AKT mTOR, טיפול ממוקד, PF-04691502