Clear Sky Science · he
משותף בשינויים בביטוי גנים ובמתילציה בין שני מודלים של אפילפסיה נרכשת בעכברוש
מדוע שינויים בגנים חשובים לפרכוסים
אפילפסיה משפיעה על מיליונים, ובעבור כשליש מהחולים התרופות הקיימות אינן מצליחות לשלוט לחלוטין בפרכוסים. רוב התרופות מרפות פשוט את הסופות החשמליות במוח אך אינן מונעות את התפתחות האפילפסיה מלכתחילה. במחקר זה נבדק האם סימנים כימיים מתמשכים על ה‑DNA, והאופן שבו גנים מודלקים או מושתקים, עשויים להסביר כיצד מוח בריא הופך לאפילפטי — והאם שינויים אלה משותפים בין צורות שונות של המחלה.
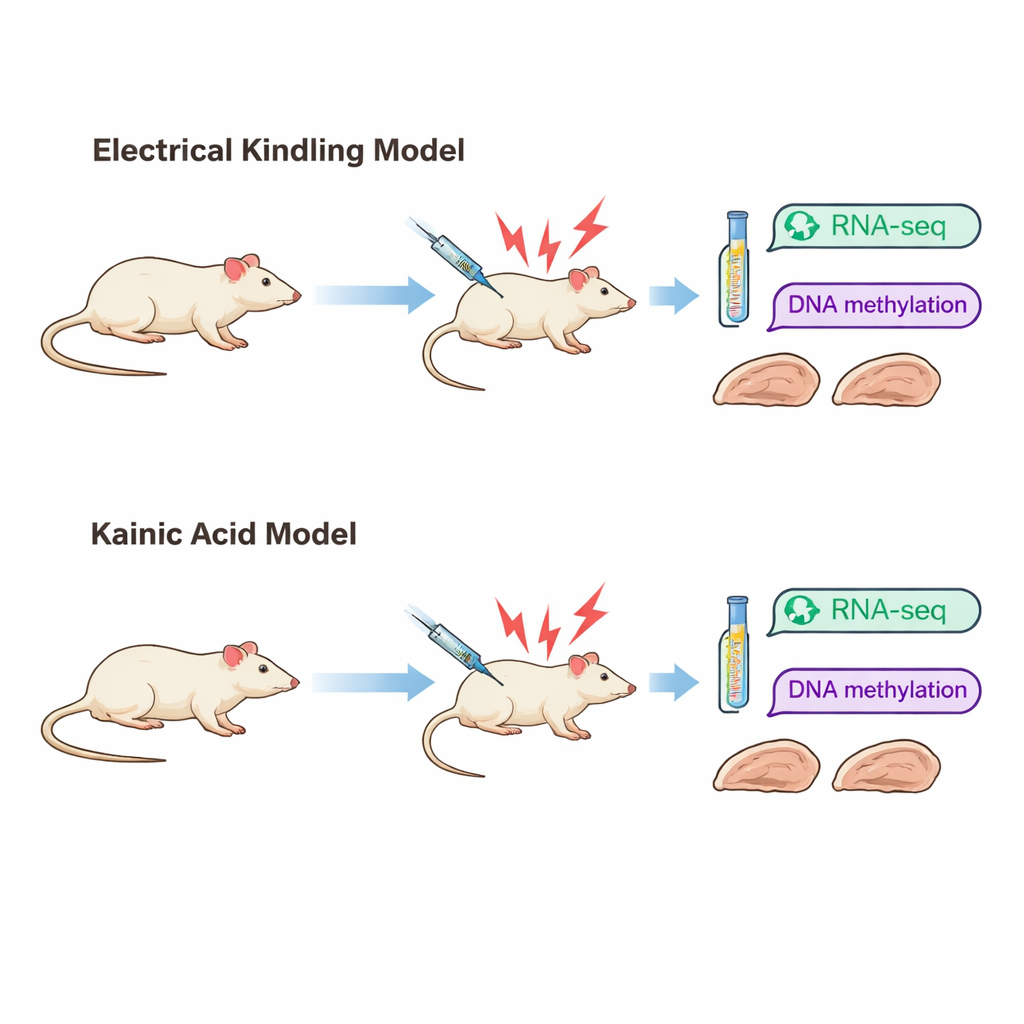
שני דרכים שונות לאותה מחלה
החוקרים התמקדו באפילפסיה של האונה הרקתית, צורה נפוצה של המחלה שלעיתים קשה לטפל בה. הם השתמשו בשני מודלים מבוססים בעכברוש שמחקים דרכים שונות להיווצרות אפילפסיה. במודל ה"קינדלינג" ניתנים פולסים חשמליים קצרים לחלק מההיפוקמפוס לאורך זמן עד שהפרכוסים הופכים קלים להנעה. במודל ה"חומצה קיינית" כימיקל גורם לפרץ פרכוסים עוצמתי, ולאחריו מופיעים פרכוסים ספונטניים בשלבים מאוחרים. אף ששני המודלים בסופו של דבר מייצרים התנהגות חיצונית דומה — פרכוסים קונבולסיביים חזקים — הנזק המוחי נראה שונה מאוד. בעכברושים מקינדלינג מבנה הרקמה נשמר ברובו, בעוד שבעכברושים שטופלו בחומצה קיינית נרשמים אובדן תאים וצלקתיות בולטת באזורים מרכזיים של ההיפוקמפוס.
קריאת הפעילות הגנטית של המוח
כדי להבין כיצד נתיבים שונים אלה לאפילפסיה משנים את המוח ברמה המולקולרית, הצוות בחן את ההיפוקמפוס לאחר שעכברושים בכל מודל חוו שלושה פרכוסים חמורים. הם מדדו אילו גנים פעילים יותר או פחות באמצעות רצף RNA, ומיפו סימני כימיה הנקראים קבוצות מתיל על ה‑DNA בעזרת שיטה הידועה כ‑reduced-representation bisulfite sequencing. שינויים בפעילות גנים משקפים כיצד תאים מגיבים ומתאימים את עצמם, בעוד שסימני מתילציה נחשבים לעתים ל"זיכרון" ארוך טווח שיכול להשפיע על הפעלת או שיתוק גנים.
שינויים בפעילות גנים עולים על סימני ה‑DNA
שני המודלים יצרו דפוסים שונים באופן בולט של פעילות גנים. במודל הקינדלינג נרשמו שינויים ביותר מעשרה פעמים במספר הגנים בהשוואה למודל החומצה הקיינית. יחד עם זאת, כאשר החוקרים חפפו את שתי הרשימות הם עדיין מצאו מעל מאה גנים שהשתנו בשני המודלים, וברובם השינוי נע בכיוון דומה. דוגמה לכך היא Mmp9, גן המקושר לאופן שבו תאי המוח משנים את הקשרים שלהם ולנזק הקשור לפרכוסים; הוא הוגבר בצורה משמעותית בשני המודלים. שינויים משותפים אלה מצביעים על תגובות גנטיות ליבתיות בעת אפילפטוגנזה, גם כאשר הגורם הראשוני והנזק הנראה לעין שונים.
הסימנים על ה‑DNA מספרים סיפור שונה
כשבדקו את מתילציית ה‑DNA התמונה השתנתה. בשני המודלים נראו רבים מהגנים עם מתילציה משונה, והיה חפיפה נכבדה ביניהם. עם זאת, רק תת‑קבוצה צנועה של גנים הראתה גם מתילציה משתנה וגם שינוי בביטוי בתוך אותו מודל, ועדיין פחות נהגו כך בשני המודלים. בחלק מהגנים המשותפים, כגון Nedd9 ו‑Ptpre, הביטוי עלה בשני המודלים, אך כיוונם של שינויים במתילציה באתרים בודדים יכל להיות מנוגד בין המודלים. בסך הכל לא נמצאה כלל פשוט של "יותר מתילציה = פחות פעילות גנים" או להיפך. ממצא זה מרמז שבמודלים אלה של אפילפסיה רוב השינויים בביטוי גנים אינם מונעים ישירות על‑ידי שינויים רחבי היקף במתילציית ה‑DNA.
מה המשמעות לכך עבור טיפולים עתידיים
למי שמקווים לטיפולים טובים יותר לאפילפסיה, הממצאים הללו מביאים גם זהירות וגם הכוונה. העבודה מראה שהתוכניות הגנטיות שמופעלות במהלך התפתחות האפילפסיה יכולות להיות תלויות מאוד במודל, ושהמתילציה של ה‑DNA היא רק חלק מתמונה רגולטורית גדולה ומורכבת יותר. מטרות גנטיות מבטיחות שזוהו במודל חייתי יחיד עשויות שלא להיות כלליות, ולכן כדאי לבחון אותן במספר מודלים לפני שמתקדמים לעבודה על בני אדם. במקביל, המעט גנים שמשתנים גם בביטוי וגם במתילציה בין המודלים עשויים לייצג נקודות פתיחה עמידות במיוחד לפיתוח טיפולים שמשנים את מהלך המחלה — לא רק להחליש פרכוסים, אלא למנוע את הופעת האפילפסיה עצמה.
ציטוט: Purnell, B.S., Hur, J., Ruskin, D. et al. Commonalities in gene expression and methylation changes across two rat models of acquired epilepsy. Sci Rep 16, 5095 (2026). https://doi.org/10.1038/s41598-026-35826-6
מילות מפתח: אפילפטוגנזה, מתילציה של DNA, ביטוי גנים, אפילפסיה של האונה הרקתית, מודלים בעכברוש