Clear Sky Science · he
מחקר כמותי של תרכובות ציטוטוקסיות באמצעות תיאורים מבוססי גרפים ולמידת מכונה
מדוע מחקר זה חשוב עבור תרופות סרטן עתידיות
תרופות סרטן ההורגות תאי גידול, הידועות כתרופות ציטוטוקסיות, לעתים קרובות הולכות על חבל דק בין הצלת חיים לבין גרימת תופעות לוואי קשות. כדי לעצב טיפולים בטוחים ויעילים יותר, מדענים זקוקים לדרכים מהירות ואמינות לחזות כיצד תרופות אלה נעים בגוף — עד כמה הן נספגות, כמה בקלות חוצות ממברנות תא והיכן הן מצטברות. מחקר זה מדגים כיצד תיאורים מתמטיים של מולקולות תרופות, בשילוב עם למידת מכונה מודרנית, יכולים להעריך במדויק מאפיין מרכזי השולט בהתנהגות זו, ובכך להאיץ את החיפוש אחר טיפולים טובים יותר לסרטן.
שטח פנים מרכזי ששולט לאן תרופות יכולות להגיע
רעיון מרכזי במאמר הוא שטח הפנים הפולרי הטופולוגי, או Top_PSA. במונחים פשוטים, זהו מספר המשקף עד כמה משטח המולקולה מורכב מאזורי "פולריים" — חלקים שאוהבים מים ויכולים ליצור קשרי מימן. מולקולות עם שטח פני פולרי גבוה מאוד מתקשות לעתים לחצות ממברנות שומניות של תאים ועלולות להיספג באופן לקוי כאשר נלקחות דרך הפה. מולקולות עם שטח פני פולרי נמוך מאוד עלולות לעבור בקלות רבה מדי מחסומים רבים, ולגרום לעתים לתופעות לוואי ברקמות רגישות כמו המוח. Top_PSA הפכה לקיצור פופולרי להערכת תכונות הובלה אלה מכיוון שניתן לחשבה במהירות מתוך שרטוט דו־ממדי של מולקולה, ללא צורך בסימולציות תלת־ממד איטיות.
הפיכת שרטוטי מולקולות למספרים
החוקרים אספו מערך מוקפד של 156 תרכובת ציטוטוקסיות שונות שנלקחו מתרופות אנטי־סרטן אמיתיות וסוכנים ניסיוניים. לאחר מכן המירו כל מולקולה ל‑58 תיאורים מכונים — מספרים הלוכדים תכונות כגון כמה אטומים יש בה, כמה טבעות, כמה גמישות יש בקשרים שלה, כמה אטומים יכולים ליצור קשרי מימן, ועד כמה חלקים שונים פולריים או חשמליים. רבים מהתיאורים הללו מגיעים מתורת הגרפים, שבה מתייחסים למולקולה כרשת של קודקודים מקושרים וקישורים. דיוקן מספרי עשיר זה של כל מולקולה שימש כקלט למודלים ממוחשבים המבקשים לחזות את ערכי ה‑Top_PSA המחושבים על ידי חבילות כימיה נפוצות.
בדיקת מסלולים שונים לחיזוי מדויק
כדי למצוא את הדרך הטובה ביותר לקשר בין התיאורים הללו ל‑Top_PSA, הצוות השווה מספר אסטרטגיות מודלינג. הם ניסו רגרסיה ליניארית סטנדרטית וכן שתי גרסאות "רגולריות" הנקראות ריד ולסו, שתוכננו להתמודד טוב יותר עם מידע רועש ומצטלב. הם גם בחנו סכמות שונות של עיבוד נתונים: התאמת מודלים ישירות לתיאורים הגולמיים, דחיסתם באמצעות ניתוח רכיבים עיקריים (PCA), קנה מידה רוּבַּסְטִי שמפחית את השפעת הערכים הקיצוניים, התאמה של ערכים חריגים וקטיעת תכונות בעלות מתאם גבוה באמצעות מדד שנקרא גורם לניפוח השונות. כל גישה הוערכה בקפדנות באמצעות ולידציה צולבת k‑fold, שיטה המחלקת את הנתונים שוב ושוב לתת‑קבוצות אימון ומבחן כדי להגן מפני התאמה מופרזת.
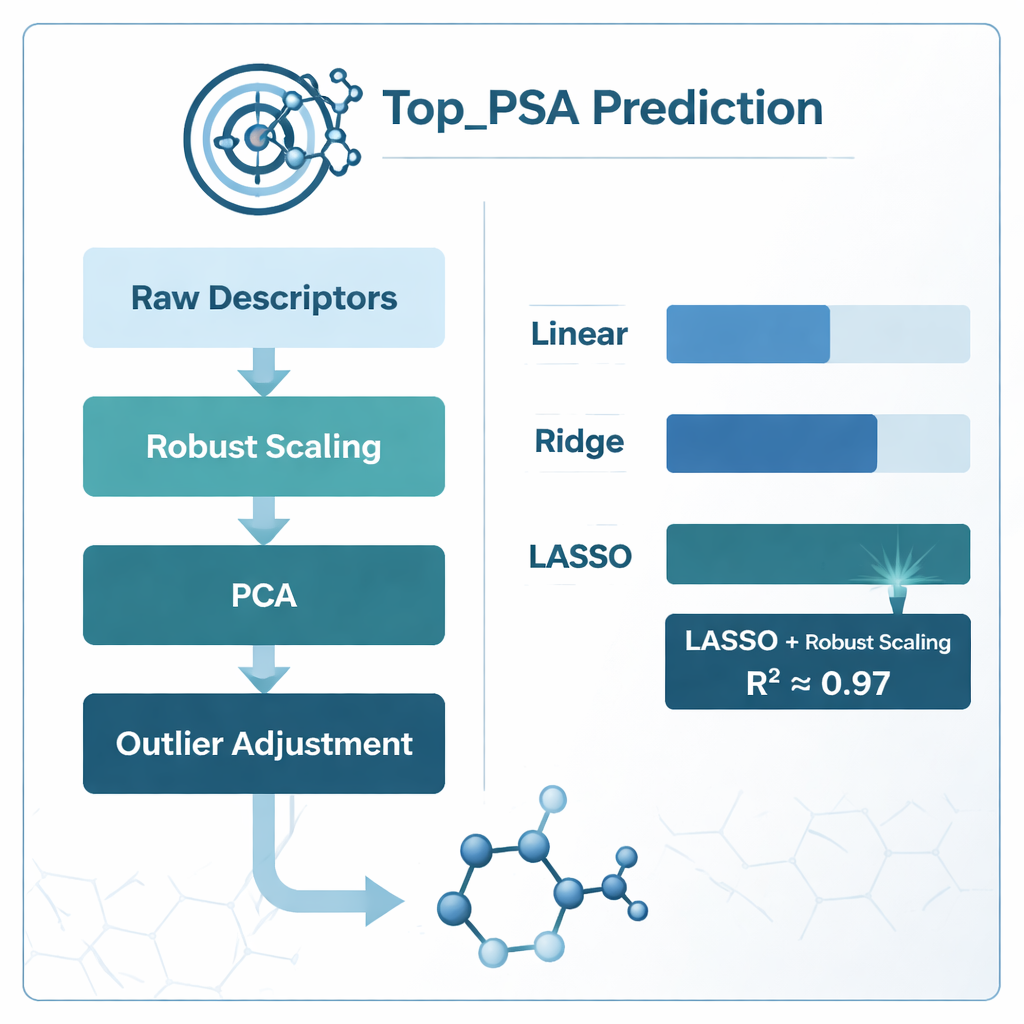
מה עבד הכי טוב ומה המודלים למדו
המנצחת הברורה הייתה השילוב של קנה מידה רובסטי עם רגרסיית LASSO, שהשיג מקדם קביעה (R²) של כ‑0.97 — כלומר הצליח להסביר בערך 97% מהשונות ב‑Top_PSA בין 156 התרופות. מודלים מבוססי PCA התקרבו בדיוק הגולמי אך היו קשים יותר לפירושים כימיים מפני שהתיאורים המקוריים נטמעו למרכיבים אבסטרקטיים. קיצוץ פשוט של תיאורים מתואמים באמצעות גורם לניפוח השונות למעשה פגע בביצועים, מה שמעיד שחלק ממדדי ההצטלבות עדיין נושאים מידע כימי שימושי. על ידי בחינת משקלות התיאורים ש‑LASSO השאירו לא־אפס, המחברים מצאו שהגורמים החשובים ביותר היו נוכחות אטומי הטרו כגון חנקן וחמצן, היכולת לתרום או לקבל קשרי מימן, ואינדקסים שעוקבים אחר האופן שבו אטומים אלקטרושליליים מסודרים על פני גרף המולקולה — כל אלה תכונות התואמות להבנה הכימית האינטואיטיבית של שטח הפנים הפולרי.
כיצד זה יכול להנחות עיצוב תרופות טוב יותר
לקוראים שאינם בתחום, המסר המרכזי הוא שחתימות מתמטיות של מולקולות שמוכנות בקפידה, כשהן משולבות עם שיטות למידת מכונה מתאימות, יכולות לספק אומדנים מהירים ואמינים של עד כמה תרופות סרטן יהיו "דביקות" או "חלקלקות" בזמן שהן נעות בגוף. המחקר מציע הנחיות מעשיות לחוקרים אחרים באשר לאופן עיבוד נתוני התיאורים, אילו גישות מודלינג להעדיף, ואילו קיצורי דרך כדאי להימנע מהם. בטווח הארוך, מודלים כאלה של Top_PSA שהם רבי־עמידות וניתנים לפירוש יכולים לסייע לכימאים לסנן ספריות וירטואליות עצומות של תרופות פוטנציאליות, ולמקד את המאמצים על תרכובות עם האיזון הנכון בין מעבר ממברנה ובטיחות — צעד חשוב לקראת טיפולים לסרטן יעילים ופחות רעילים.
ציטוט: Ahmad, S., Javed, S., Khalid, S. et al. A quantitative study of cytotoxic compounds using graph based descriptors and machine learning. Sci Rep 16, 5076 (2026). https://doi.org/10.1038/s41598-026-35728-7
מילות מפתח: תרופות ציטוטוקסיות, שטח פני פולרי, תיאורי מולקולות, למידת מכונה, חדירות תרופות