Clear Sky Science · he
השפעה פרוגנוסטית של אזורי מרחב בסרטן הערמונית
מדוע "השכונות" של הגידול חשובות
סרטן הערמונית נפוץ, אבל לא כל הגידולים מתנהגים באותו אופן. חלקם גדלים באטיות, בעוד אחרים מתקדמים במהירות ומסכנים את חיי החולה. כיום רופאים מסתמכים על סימנים כמו רמות PSA ודירוג מיקרוסקופי כדי לשער אילו גידולים מסוכנים. המחקר הזה שואל שאלה חדשה: האם המקום המדויק שבו תאי הסרטן נמצאים בתוך הגידול — הקצה החיצוני הפעיל לעומת הליבה העמוקה — יכול לעזור לחזות את סיכויי המטופל?
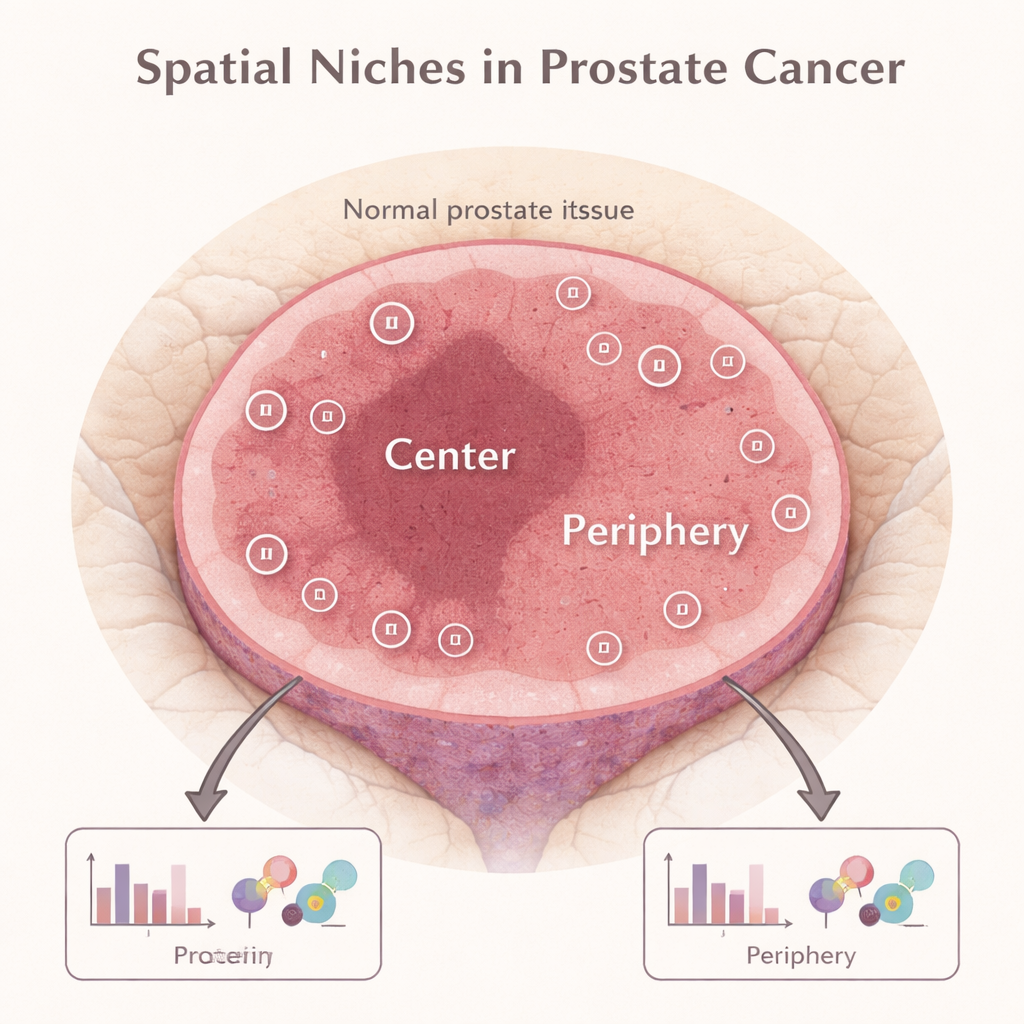
מבט על הגידול כמערכת אקולוגית קטנה
מחקר מודרני מראה שהגידול אינו כדור אחיד של תאים זהים. במקום זאת, הוא דומה יותר למערכת אקולוגית קטנה עם "שכונות" מובחנות, או אזורי מרחב. בסרטן הערמונית, ליבת הגידול והקצה החיצוני שבו הסרטן פוגש רקמה תקינה יכולים לארח תמהיל שונה של תאי סרטן, תאי חיסון ומבנים תומכים. החוקרים השתמשו בטכנולוגיה שנקראת פרופיל מרחבי דיגיטלי, שמאפשרת למדוד עשרות חלבונים ישירות בפרוסות דקות של רקמת גידול נשמרת, תוך שמירה על המידע המדויק היכן בתוך הגידול כל מדידה בוצעה.
מדידת חלבונים במרכז ובקצה הגידול
הצוות ניתח דגימות גידול מ-49 גברים עם סרטן ערמונית בסיכון גבוה שעברו ניתוח. עבור כל גידול בחרו אזורים במרכז ובפריפריה ומדדו רמות של 46 חלבונים שונים הקשורים לתאי חיסון, למוות תאי ולסיגנלים של גדילה. זה הניב עשרות אלפי נקודות נתונים. כאשר בחנו את המרכז והפריפריה בנפרד, הם איששו שאזורים אלה מתנהגים באופן שונה: חלבונים רבים, במיוחד אלה הקשורים לפעילות חיסונית, היו בשפע בקצה החיצוני של הגידול, בעוד שמווסתי מוות תאי מסוימים נמצאו ברמות גבוהות יותר במרכז.
מתי מבט נפרד אינו מספיק
החוקרים שאלו לשאלה האם תבניות חלבונים רק במרכז או רק בפריפריה יכולות לחזות כמה זמן החולים יחזיקו מעמד ללא התקדמות המחלה לאחר הניתוח. באמצעות שיטות סטטיסטיות לאשכולת חולים על בסיס תבניות חלבונים בכל מדור בנפרד, הם מצאו שתי אשכולות עיקריים גם למרכז וגם לפריפריה. עם זאת, אף אחת מהקבוצות הללו לא התאמה לאופן שבו החולים באמת התקדמו עם הזמן, ולא קישרה באופן ברור לגורמי סיכון קלאסיים כגון ציון גליסון או מוטציות גנטיות ידועות כמו BRCA1/2 ו-TP53. במילים אחרות, הסתכלות על כל "שכונה" בנפרד לא הניבה סמן פרוגנוסטי שימושי.
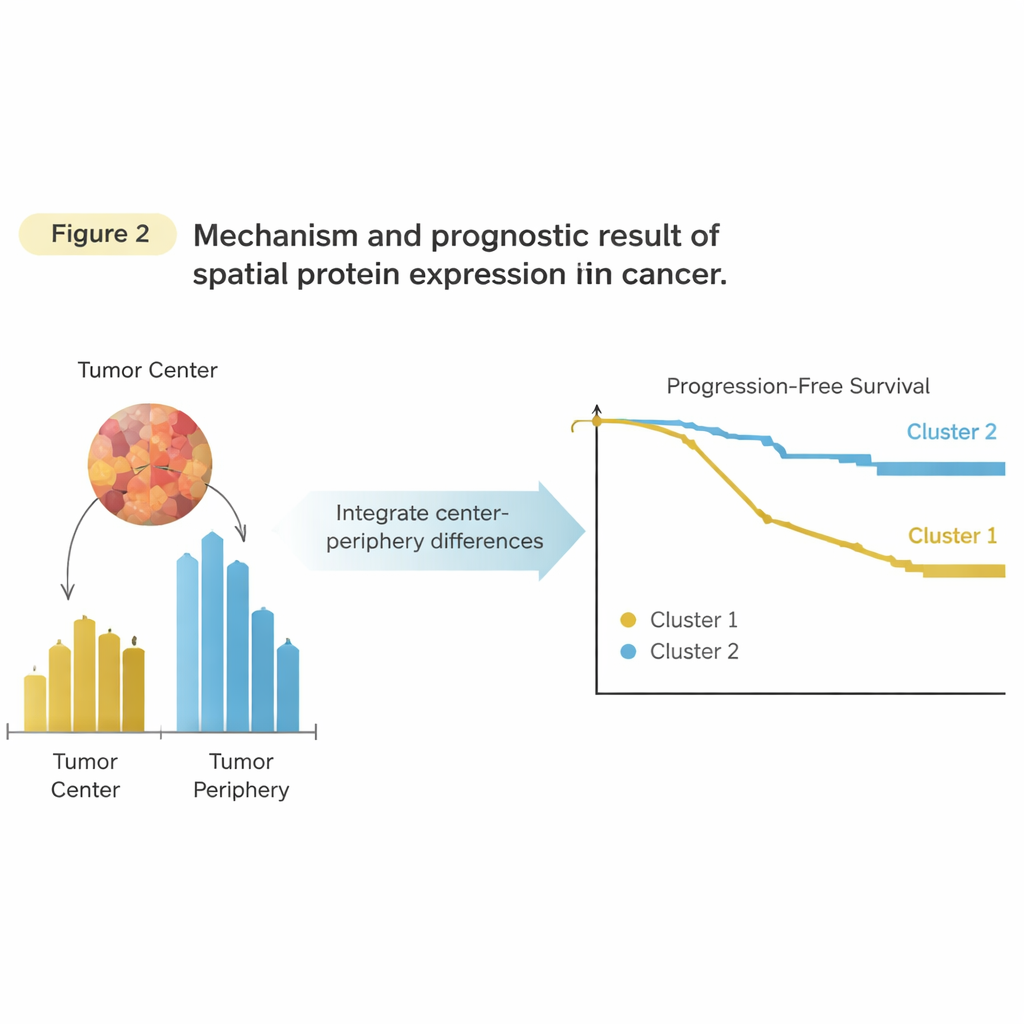
שילוב שתי השכונות חושף אות
הצעד המכריע היה לשלב מידע מהמרכז ומהפריפריה במקום לטפל בהם בנפרד. עבור כל חלבון ולכל מטופל, החוקרים חישבו כמה יותר (או פחות) החלבון מבוטא בפריפריה בהשוואה למרכז. זה הניב "ערך איזון" יחיד לכל חלבון שעדיין קלט היכן בתוך הגידול החלבון גבוה יותר. כאשר אשכולו את החולים על בסיס ערכי האיזון המרחביים האלה, נוצרו שתי קבוצות חדשות. הפעם, האשכולות ניבאו הבדל משמעותי: לקבוצה אחת היה מרווח זמן קצר בהרבה עד להתקדמות המחלה לעומת הקבוצה השנייה. חשוב לציין שכוח השיטה לא נבע מחלבון בולט יחיד אלא מהתבנית המרחבית הכוללת על פני חלבונים רבים, במיוחד אלה הקשורים לתאי חיסון ולשחזור רקמה בקצה הגידול.
מה זה יכול betekenen עבור מטופלים
עבור אנשים העומדים בפני סרטן הערמונית, הממצאים הללו מרמזים שמיקום הביטוי של חלבונים בתוך הגידול — לא רק הכמות הכוללת — עשוי להכיל רמזים חשובים לגבי התנהגות המחלה בעתיד. למרות שהמחקר קטן ומשתמש בטכנולוגיה מיוחדת ויקרה, הוא מספק הוכחת עיקרון שמדידות חלבוניות רגישות למרחב יכולות לחשוף מידע פרוגנוסטי שמבחנים סטנדרטיים מפספסים. עם אימות נוסף ושיטות מעבדה פשוטות יותר, סוג זה של סמן מרחבי עשוי בעתיד לסייע לרופאים להבחין טוב יותר אילו גידולי ערמונית בסיכון גבוה צפויים להתקדם במהירות ואילו עשויים להתנהל בצורה ניתנת לניהול, מה שיוביל להחלטות טיפול מותאמות יותר.
ציטוט: Schneider, F., Böning, S.H., Antunes, B.C. et al. Prognostic impact of spatial niches in prostate cancer. Sci Rep 16, 2598 (2026). https://doi.org/10.1038/s41598-026-35720-1
מילות מפתח: סרטן הערמונית, פרופיל מרחבי, מיקרוסביבת הגידול, סמן פרוגנוסטי, הטרוגניות בתוך הגידול